2020 浙江省嘉兴市中考化学真题及答案
一、选择题(本题有 5 小题,每小题 3 分,共 15 分.请选出一个符合题意的正确选项,不
选、多选、错选,均不给分)
1.下列物质是某食品配料中的主要成分,其中属于无机化合物的是(
)
A.淀粉
B.食盐
C.食用油
D.白砂糖
2.某兴趣小组分别用加溶质和恒温蒸发溶剂的方法,将一定质
量的硝酸钾不饱和溶液转化为饱和溶液。实验过程中,硝酸钾
溶解度的变化情况分别是(
)
A.变大 不变
B.变大 变小
C.不变 变大
D.不变 不变
3.某化合物在水中能完全电离,将该化合物配制成甲、乙、丙
三种不同浓度的水溶液,对溶液中所含阴、阳离子数目进行测
定,结果如图所示。由图可判断该化合物可能是(
)
A.CaCl2
B.Al(NO3)3
C.NaOH
D.H2SO4
4.科学研究以实验为基础,正确的操作是确保实验安全与结果可靠的前提。下列实验操作错
误的是( )
A.加热前先通氢气
B.高倍镜下调焦
C.叶片脱色
D.温度计读数
5.学习了物质分类与转化规律后,某同学绘制了部分物质间相互反应的
关系图。图中阴影部分表示相邻两类物质的反应,其中不能用于制取 ZnCl2
的是(
)
A.①
B.②
C.③
D.④
二、填空题(本题有 3 小题,6 空格,每空 2 分,共 12 分)
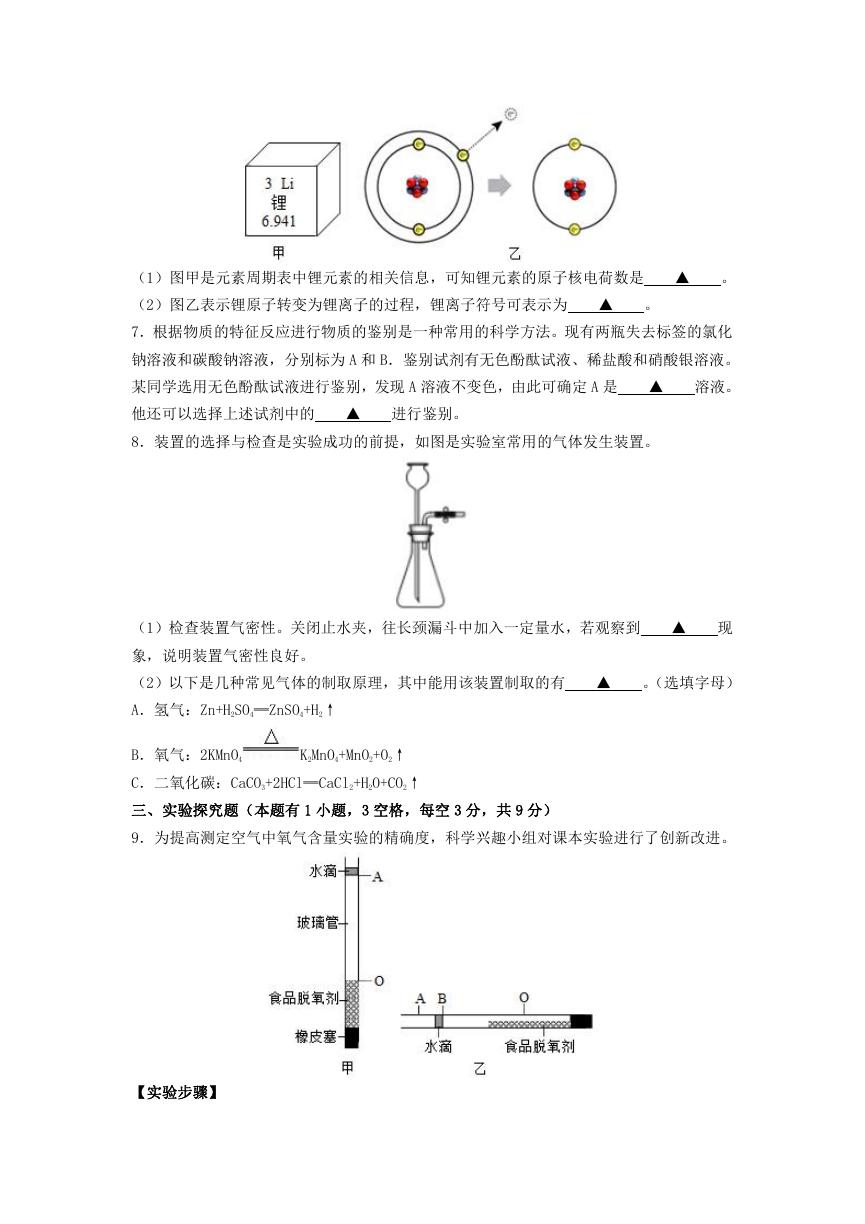
6.2019 年诺贝尔化学奖颁发给了在锂电池领域做出重大贡献的吉野彰等三位科学家。分析
回答下列问题:
�
(1)图甲是元素周期表中锂元素的相关信息,可知锂元素的原子核电荷数是
▲
。
(2)图乙表示锂原子转变为锂离子的过程,锂离子符号可表示为
▲
。
7.根据物质的特征反应进行物质的鉴别是一种常用的科学方法。现有两瓶失去标签的氯化
钠溶液和碳酸钠溶液,分别标为 A 和 B.鉴别试剂有无色酚酞试液、稀盐酸和硝酸银溶液。
某同学选用无色酚酞试液进行鉴别,发现 A 溶液不变色,由此可确定 A 是
▲
溶液。
他还可以选择上述试剂中的
▲
进行鉴别。
8.装置的选择与检查是实验成功的前提,如图是实验室常用的气体发生装置。
(1)检查装置气密性。关闭止水夹,往长颈漏斗中加入一定量水,若观察到
▲
现
象,说明装置气密性良好。
(2)以下是几种常见气体的制取原理,其中能用该装置制取的有
▲
。(选填字母)
A.氢气:Zn+H2SO4═ZnSO4+H2↑
B.氧气:2KMnO4
K2MnO4+MnO2+O2↑
C.二氧化碳:CaCO3+2HCl═CaCl2+H2O+CO2↑
三、实验探究题(本题有 1 小题,3 空格,每空 3 分,共 9 分)
9.为提高测定空气中氧气含量实验的精确度,科学兴趣小组对课本实验进行了创新改进。
【实验步骤】
�
①取一根玻璃管,用橡皮塞将一端密封;
②将食品脱氧剂粉末迅速装入玻璃管,立即向管口注入一滴水将玻璃管密封,水滴的下端
标为 A.弹动玻璃管使脱氧剂粉末分布均匀且紧密,脱氧剂的上端标为 O,如图甲所示;
③水平滚动玻璃管,使食品脱氧剂粉末平铺在玻璃管中,静置至水滴不再移动时,水滴的
右端标为 B,如图乙所示;
④用刻度尺测量出 AO 段和 AB 段的长度,井计算出 AB 与 AO 的比值,将数据记录在表格中;
⑤洗涤、干燥实验装置,重复上述实验。
实验次数
1
2
3
AO/mm
523.5
525.5
527.0
AB/mm
109.5
110.0
110.5
AB/AO
0.2092
0.2093
0.2097
【得出结论】根据表格中的实验数据,可知空气中氧气含量为
▲
。(用百分数表示)
【思考讨论】
①实验步骤③中,将食品脱氧剂粉末平铺在玻璃管中的目的是
▲
。
②实验步骤②中,如果玻璃管内的脱氧剂粉末分布不够紧密,会使实验结果偏大,其原因
是
▲
。
四、解答题(本题有 1 小题,第 10 小题 4 分)
10.随着手机、电脑等移动设备的普及,人们对充电设备的要求越来越高。最近,某品牌
氮化镓充电设备以体积小、功率大深受消费者喜爱。
(1)氮化镓(GaN)是充电设备中的核心材料。查阅资料得知:氮化镓中氮元素的化合价
与氨气(NH3)中氮元素的化合价相同。由此可知,氮化镓中镓元素的化合价为
▲
。
(2)氮化镓的制取可通过镓与氨气在高温下发生置换反应来实现,其反应的化学方程式为
▲
。
选考题
11.复方碳酸氢钠片是一种常用的抗酸剂药物,口服后能迅速中和或缓冲胃酸,减少疼痛
等症状。复方碳酸氢钠片的主要成分是碳酸氢钠(与盐酸反应的化学方程式为:NaHCO3+HCl
═NaCl+H2O+CO2↑)。
某科学兴趣小组为了测定药片中碳酸氢钠的含量做了以下实验:先将复方碳酸氢钠片
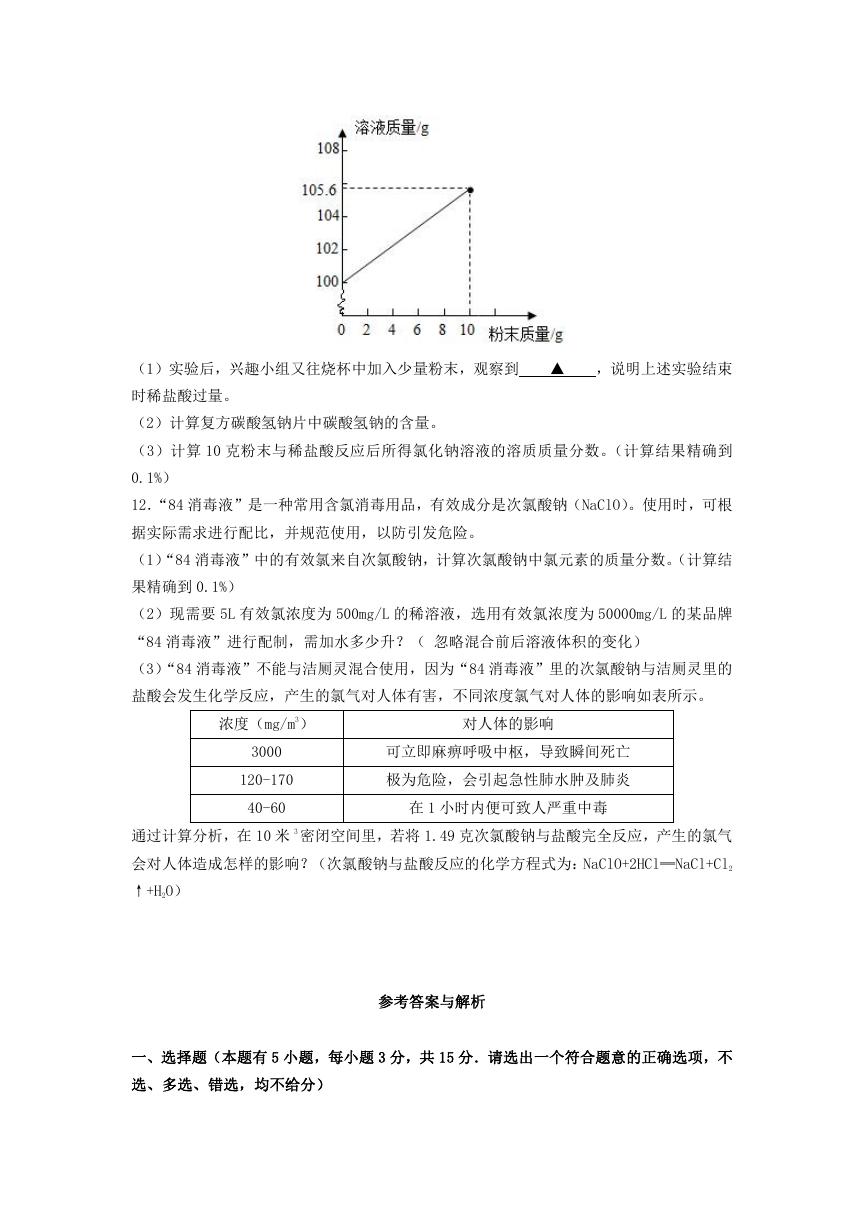
制成粉末,取 10 克分多次放入盛有 100 克稀盐酸的烧杯中充分反应。测出加入的粉末质量
和反应后的溶液质量,两者质量关系如图所示。
�
(1)实验后,兴趣小组又往烧杯中加入少量粉末,观察到
▲
,说明上述实验结束
时稀盐酸过量。
(2)计算复方碳酸氢钠片中碳酸氢钠的含量。
(3)计算 10 克粉末与稀盐酸反应后所得氯化钠溶液的溶质质量分数。(计算结果精确到
0.1%)
12.“84 消毒液”是一种常用含氯消毒用品,有效成分是次氯酸钠(NaClO)。使用时,可根
据实际需求进行配比,并规范使用,以防引发危险。
(1)“84 消毒液”中的有效氯来自次氯酸钠,计算次氯酸钠中氯元素的质量分数。(计算结
果精确到 0.1%)
(2)现需要 5L 有效氯浓度为 500mg/L 的稀溶液,选用有效氯浓度为 50000mg/L 的某品牌
“84 消毒液”进行配制,需加水多少升?( 忽略混合前后溶液体积的变化)
(3)“84 消毒液”不能与洁厕灵混合使用,因为“84 消毒液”里的次氯酸钠与洁厕灵里的
盐酸会发生化学反应,产生的氯气对人体有害,不同浓度氯气对人体的影响如表所示。
浓度(mg/m3)
对人体的影响
3000
120-170
40-60
可立即麻痹呼吸中枢,导致瞬间死亡
极为危险,会引起急性肺水肿及肺炎
在 1 小时内便可致人严重中毒
通过计算分析,在 10 米 3 密闭空间里,若将 1.49 克次氯酸钠与盐酸完全反应,产生的氯气
会对人体造成怎样的影响?(次氯酸钠与盐酸反应的化学方程式为:NaClO+2HCl═NaCl+Cl2
↑+H2O)
参考答案与解析
一、选择题(本题有 5 小题,每小题 3 分,共 15 分.请选出一个符合题意的正确选项,不
选、多选、错选,均不给分)
�
1.下列物质是某食品配料中的主要成分,其中属于无机化合物的是(
)
A.淀粉
B.食盐
C.食用油
D.白砂糖
【知识考点】有机物与无机物的区别.
【思路分析】有机物是指含有碳的化合物,一氧化碳、二氧化碳、碳酸盐等除外。
【解答过程】解:A、淀粉中含有碳元素,属于有机物,故 A 错;
B、食盐主要成分是氯化钠,不含碳元素,属于无机化合物,故 B 正确;
C、食用油中含有油脂,含有碳元素,属于有机物,故 C 错;
D、白砂糖中含有蔗糖,含有碳元素,属于有机物,故 D 错。
故选:B。
【总结归纳】解答本题关键是熟悉有机物的特点和判断方法。
2.某兴趣小组分别用加溶质和恒温蒸发溶剂的方法,将一定质量的硝酸钾不饱和溶液转化
为饱和溶液。实验过程中,硝酸钾溶解度的变化情况分别是(
)
A.变大 不变
B.变大 变小
C.不变 变大
D.不变 不变
【知识考点】固体溶解度的影响因素.
【思路分析】分析影响溶解度的因素有哪些
【解答过程】解:由题意可知,某兴趣小组分别用加溶质和恒温蒸发溶剂的方法,将一定
质量的硝酸钾不饱和溶液转化为饱和溶液。由于溶解度只随温度变化而变化,该兴趣小组
实验过程中没有改变温度,故溶解度不会发生改变。
故选:D。
【总结归纳】该题考查的是影响溶解度的因素有哪些,考查较为简单,适合基础较差的学
生。
3.某化合物在水中能完全电离,将该化合物配制成甲、乙、丙三种不同浓度的水溶液,对
溶液中所含阴、阳离子数目进行测定,结果如图所示。由图可判断该化合物可能是(
)
A.CaCl2
B.Al(NO3)3
C.NaOH
D.H2SO4
【知识考点】分子、原子、离子、元素与物质之间的关系.
【思路分析】根据溶液中所含阴、阳离子数目图可知,该溶液中阳离子和阴离子的个数比
为 1:1,进行分析判断。
【解答过程】解:由溶液中所含阴、阳离子数目图可知,该溶液中阳离子和阴离子的个数
比为 1:1。
�
A、CaCl2 中钙离子和氯离子的个数比为 1:2,故选项错误。
B、Al(NO3)3 中铝离子和硝酸根离子的个数比为 1:3,故选项错误。
C、氢氧化钠中钠离子和氢氧根离子的个数比为 1:1,故选项正确。
D、H2SO4 中氢离子和硫酸根离子的个数比为 2:1,故选项错误。
故选:C。
【总结归纳】本题难度不大,明确溶液中阳离子和阴离子的个数比为 1:1 是正确解答本题
的关键。
4.科学研究以实验为基础,正确的操作是确保实验安全与结果可靠的前提。下列实验操作错
误的是( )
A.加热前先通氢气
B.高倍镜下调焦
C.叶片脱色
D.温度计读数
【知识考点】氢气的化学性质与燃烧实验.
【思路分析】A、氢气的可燃性和还原性;
B、高倍镜下调焦正确;
C、叶片脱色后叶片会变成黄白色,酒精变成绿色;
D、温度计读数正确。
【解答过程】解:A、加热前先通氢气正确,防止氢气不纯而发生爆炸,正确但不符合题意,
故选项错误;
B、高倍镜下调焦正确,确保实验更准确,正确但不符合题意,故选项错误;
C、叶片脱色后叶片会变成黄白色,酒精应该变成绿色,错误符合题意,故选项正确;
D、温度计读数正确,温度计的下端在烧杯中,平视读数,正确但不符合题意,故选项错误;
故选:C。
【总结归纳】本考点考查了氢气的性质、高倍镜下调焦、物质的脱色、温度计的读数等,
要加强理解,综合掌握。
5.学习了物质分类与转化规律后,某同学绘制了部分物质间相互反应的关系图。图中阴影
部分表示相邻两类物质的反应,其中不能用于制取 ZnCl2 的是(
)
A.①
B.②
C.③
D.④
�
【知识考点】金属的化学性质;酸的化学性质;碱的化学性质;盐的化学性质.
【思路分析】根据金属、酸、碱与盐的性质,选择合适试剂,观察是够能够制取氯化锌。
【解答过程】解:A、①为酸碱反应,氢氧化锌与盐酸反应生成氯化锌和水,可以制得氯化
锌,A 不符合题意;
B、酸与金属反应,锌的金属活动性强于氢,所以锌与盐酸反应生成氯化锌和氢气,可以制
得氯化锌,B 不符合题意;
C、碱与盐的反应,碱为氢氧化锌,本身不易溶于,不能与盐反生复分解反应生成氯化锌,
因此 C 符合题意;
D、盐与金属反应,锌金属活动性强于铜,锌与氯化铜反应生成氯化锌和铜,可以制得氯化
锌,D 不符合题意;
故选:C。
【总结归纳】主要考察锌的金属活动性,以及复分解反应发生的条件,此题综合性较强,
解答时需要认真思考。
二、填空题(本题有 3 小题,6 空格,每空 2 分,共 12 分)
6.2019 年诺贝尔化学奖颁发给了在锂电池领域做出重大贡献的吉野彰等三位科学家。分析
回答下列问题:
(1)图甲是元素周期表中锂元素的相关信息,可知锂元素的原子核电荷数是
▲
。
(2)图乙表示锂原子转变为锂离子的过程,锂离子符号可表示为
▲
。
【知识考点】原子和离子的相互转化;元素周期表的特点及其应用.
【思路分析】(1)根据图中元素周期表可以获得的信息:左上角的数字表示原子序数,进
行分析解答。
(2)由图乙表示锂原子转变为锂离子的过程,锂原子失去 1 个电子形成锂离子,进行分析
解答。
【解答过程】解:(1)根据元素周期表中的一格可知,左上角的数字为 3,表示原子序数为
3;根据原子中原子序数=核电荷数=质子数=核外电子数,则锂元素的原子核电荷数是 3.(2)
由图乙表示锂原子转变为锂离子的过程,锂原子失去 1 个电子形成带 1 个单位正电荷的锂
离子,其离子符号为 Li+。
故答案为:(1)3;(2)Li+。
【总结归纳】本题难度不大,灵活运用元素周期表中元素的信息(原子序数、元素符号、
元素名称、相对原子质量)、原子和离子的相互转化是正确解答本题的关键。
7.根据物质的特征反应进行物质的鉴别是一种常用的科学方法。现有两瓶失去标签的氯化
�
钠溶液和碳酸钠溶液,分别标为 A 和 B.鉴别试剂有无色酚酞试液、稀盐酸和硝酸银溶液。
某同学选用无色酚酞试液进行鉴别,发现 A 溶液不变色,由此可确定 A 是
▲
溶液。
他还可以选择上述试剂中的
▲
进行鉴别。
【知识考点】酸、碱、盐的鉴别.
【思路分析】鉴别物质时,首先对需要鉴别的物质的性质进行对比分析找出特性,再根据
性质的不同,选择适当的试剂,出现不同的现象的才能鉴别。
【解答过程】解:氯化钠溶液和碳酸钠溶液分别显中性、碱性,某同学选用无色酚酞试液
进行鉴别,遇酚酞溶液分别显中性、碱性,发现 A 溶液不变色,则 A 是氯化钠溶液,B 是碳
酸钠溶液。
稀盐酸与氯化钠溶液不反应,和碳酸钠溶液反应生成氯化钠、水和二氧化碳气体,能出现
两种明显不同的现象,可以鉴别。
氯化钠溶液和碳酸钠溶液均能与硝酸银溶液反应,分别生成氯化银、碳酸银白色沉淀,不
能鉴别。
故答案为:
氯化钠溶液;稀盐酸。
【总结归纳】本题有一定难度,解答物质的鉴别题时要熟练掌握鉴别的物质的性质,然后
选择适当的试剂或方法,出现不同的现象即可鉴别。
8.装置的选择与检查是实验成功的前提,如图是实验室常用的气体发生装置。
(1)检查装置气密性。关闭止水夹,往长颈漏斗中加入一定量水,若观察到
▲
现
象,说明装置气密性良好。
(2)以下是几种常见气体的制取原理,其中能用该装置制取的有
▲
。(选填字母)
A.氢气:Zn+H2SO4═ZnSO4+H2↑
B.氧气:2KMnO4
K2MnO4+MnO2+O2↑
C.二氧化碳:CaCO3+2HCl═CaCl2+H2O+CO2↑
【知识考点】检查装置的气密性;实验室制取气体的思路.
【思路分析】(1)装置气密性检验的原理是:通过气体发生器与液体构成封闭体系,依据
改变体系内压强时产生的现象(如气泡的生成、水柱的形成、液面的升降等)来判断装置
气密性的好坏。
(2)根据图中装置属于固液常温型,进行分析解答。
【解答过程】解:(1)关闭止水夹,从长颈漏斗中注入水,当水浸没其下端管口时,然后
�














 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc