2022 年浙江绍兴中考化学试题及答案
一、选择题(本题共 3 小题,每小题 4 分,共 12 分。下列各小题中只有一个选项符合题意)
1.(4 分)春秋初期,绍兴一带是南方的一个冶铁中心,其炼铁方法是在 1000℃左右的温度
下 2O3 ) 发 生 一 系 列 的 反 应 生 成 含 较 多 杂 质 的 海 绵 铁 。 其 中 主 要 化 学 反 应 为 :
3CO+Fe2O3
2Fe+3CO2。下列说法正确的是(
)
A.海绵铁是一种纯净物
B.Fe2O3 中铁元素的化合价为+3 价
C.上述反应中涉及的氧化物只有 2 种
D.炼铁过程中,木炭只是作为燃料使用
2.(4 分)在做酸碱反应的实验时,向盛有氢氧化钠溶液的烧杯中,逐渐加入稀盐酸。烧杯
内相关物质的质量与加入稀盐酸质量的变化关系不正确的是(
)
A.
C.
B.
D.
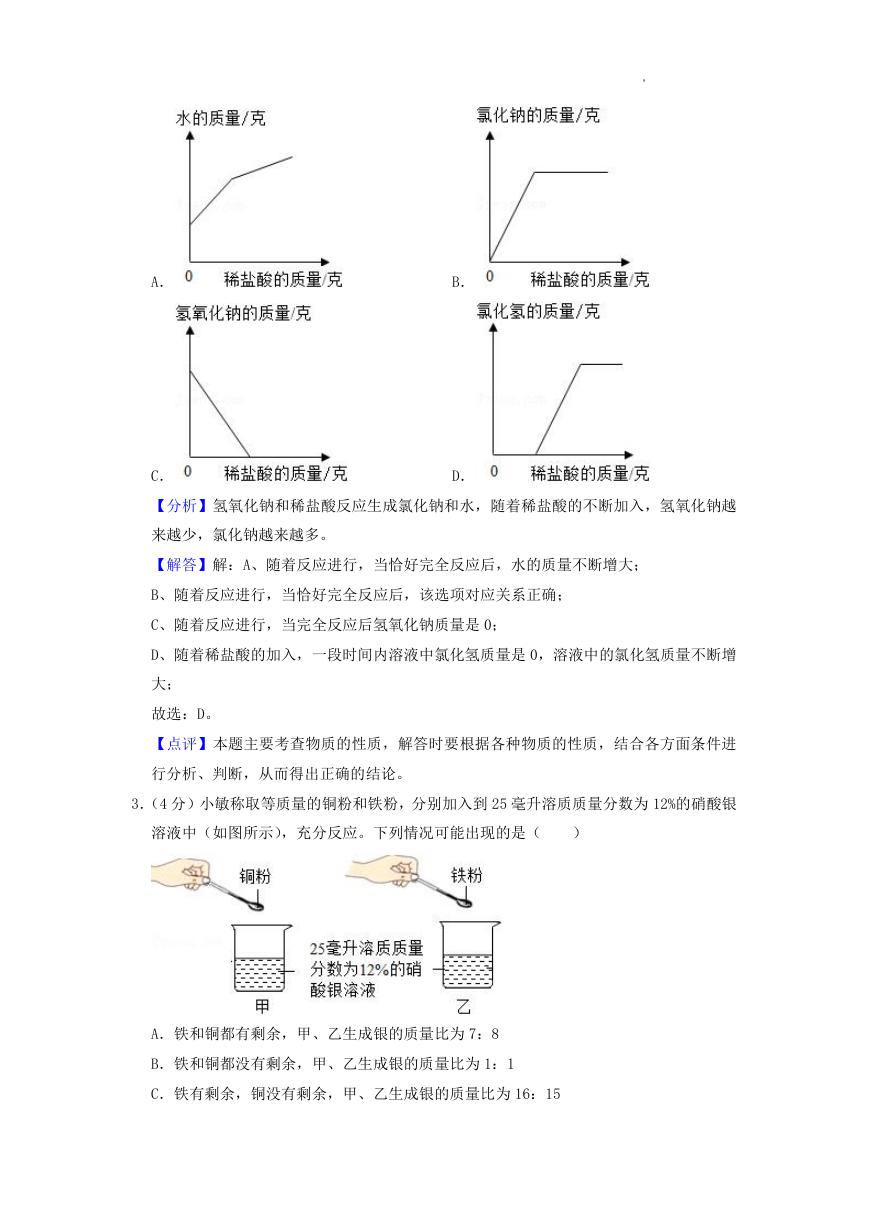
3.(4 分)小敏称取等质量的铜粉和铁粉,分别加入到 25 毫升溶质质量分数为 12%的硝酸银
溶液中(如图所示),充分反应。下列情况可能出现的是(
)
学科 网(北 京)股 份有限 公司
�
A.铁和铜都有剩余,甲、乙生成银的质量比为 7:8
B.铁和铜都没有剩余,甲、乙生成银的质量比为 1:1
C.铁有剩余,铜没有剩余,甲、乙生成银的质量比为 16:15
D.铜有剩余,铁没有剩余,甲、乙生成银的质量比为 15:14
二、填空题(本题共 2 小题,每空 2 分,共 12 分)
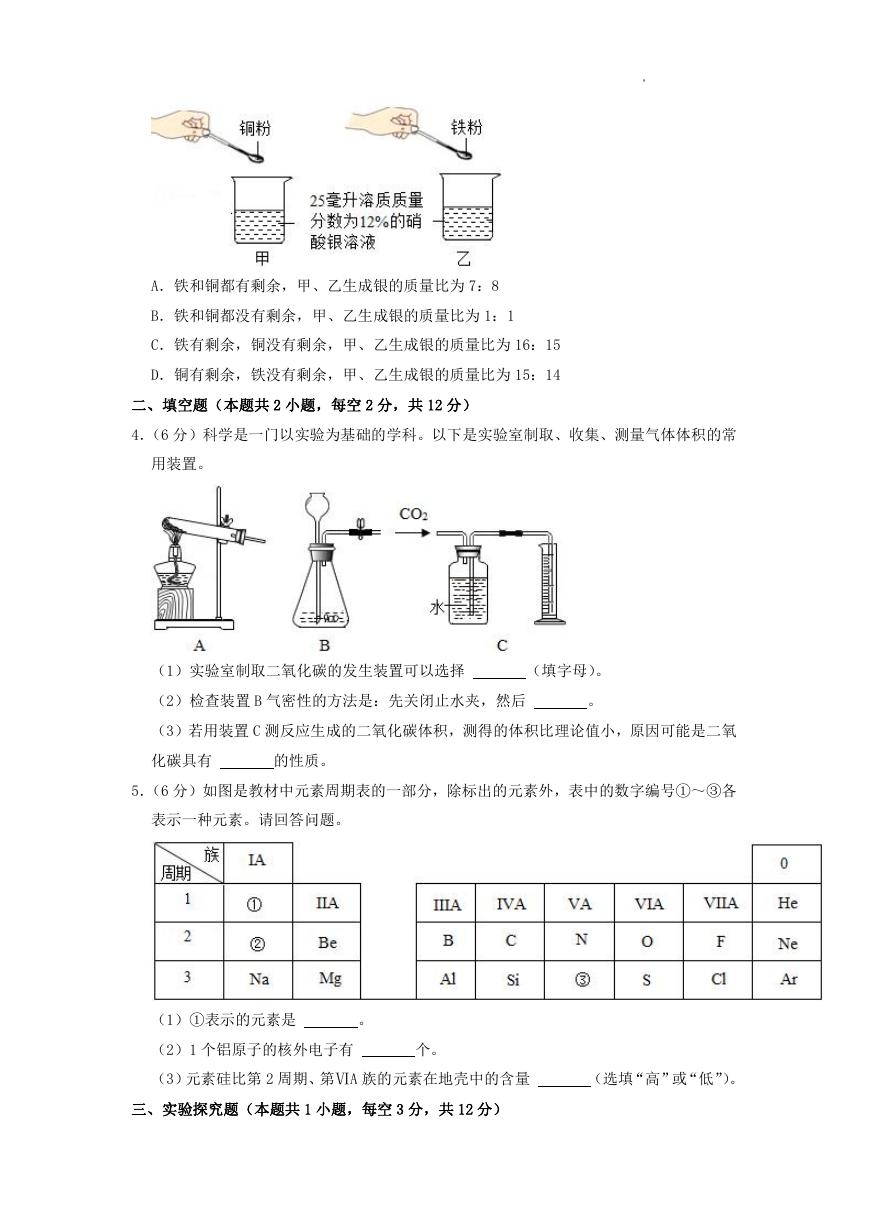
4.(6 分)科学是一门以实验为基础的学科。以下是实验室制取、收集、测量气体体积的常
用装置。
(1)实验室制取二氧化碳的发生装置可以选择
(填字母)。
(2)检查装置 B 气密性的方法是:先关闭止水夹,然后
。
(3)若用装置 C 测反应生成的二氧化碳体积,测得的体积比理论值小,原因可能是二氧
化碳具有
的性质。
5.(6 分)如图是教材中元素周期表的一部分,除标出的元素外,表中的数字编号①~③各
表示一种元素。请回答问题。
(1)①表示的元素是
。
(2)1 个铝原子的核外电子有
个。
(3)元素硅比第 2 周期、第ⅥA 族的元素在地壳中的含量
(选填“高”或“低”)。
三、实验探究题(本题共 1 小题,每空 3 分,共 12 分)
学科 网(北 京)股 份有限 公司
�
6.(12 分)如图是人类对氧化还原反应的认识过程中的三个阶段。
【阶段Ⅰ】得失氧说:物质跟氧发生的反应叫氧化反应,含氧化合物中的氧被夺取的反
应叫还原反应。
【阶段Ⅱ】化合价升降说:凡是出现元素化合价升降的化学反应都是氧化还原反应。化
合价升高的反应叫氧化反应,化合价降低的反应叫还原反应。
【阶段Ⅲ】电子转移说:化合价升降的原因是电子的转移。凡有电子转移发生的化学反
应都是氧化还原反应。失电子的反应叫氧化反应,得电子的反应叫还原反应。
(1)根据得失氧说,在 H2+CuO
Cu+H2O 化学变化中,H2 发生了
反应。
(2)电子转移是元素化合价改变的本质原因。失电子后,元素的化合价会
(选
填“升高”或“降低”)。
(3)根据化合价升降说,化学反应的四种基本类型与氧化还原反应之间的关系如图所示,
其中乙是
反应。
(4)关于氧化还原反应的认识,下列理解正确的是
。
A.氧化和还原是相互对立又辩证统一的关系
B.电子转移说是从微观视角来探析和建构氧化还原反应的概念
C.自然界中发生的氧化还原反应对人类的生活和生产都是有利的
D.人类对氧化还原反应的认识过程是一个逐步发展、延伸和完善的过程
四、解答题(本题共 3 小题,第 7 小题 6 分,第 8 小题 9 分,第 9 小题 4 分,共 19 分)
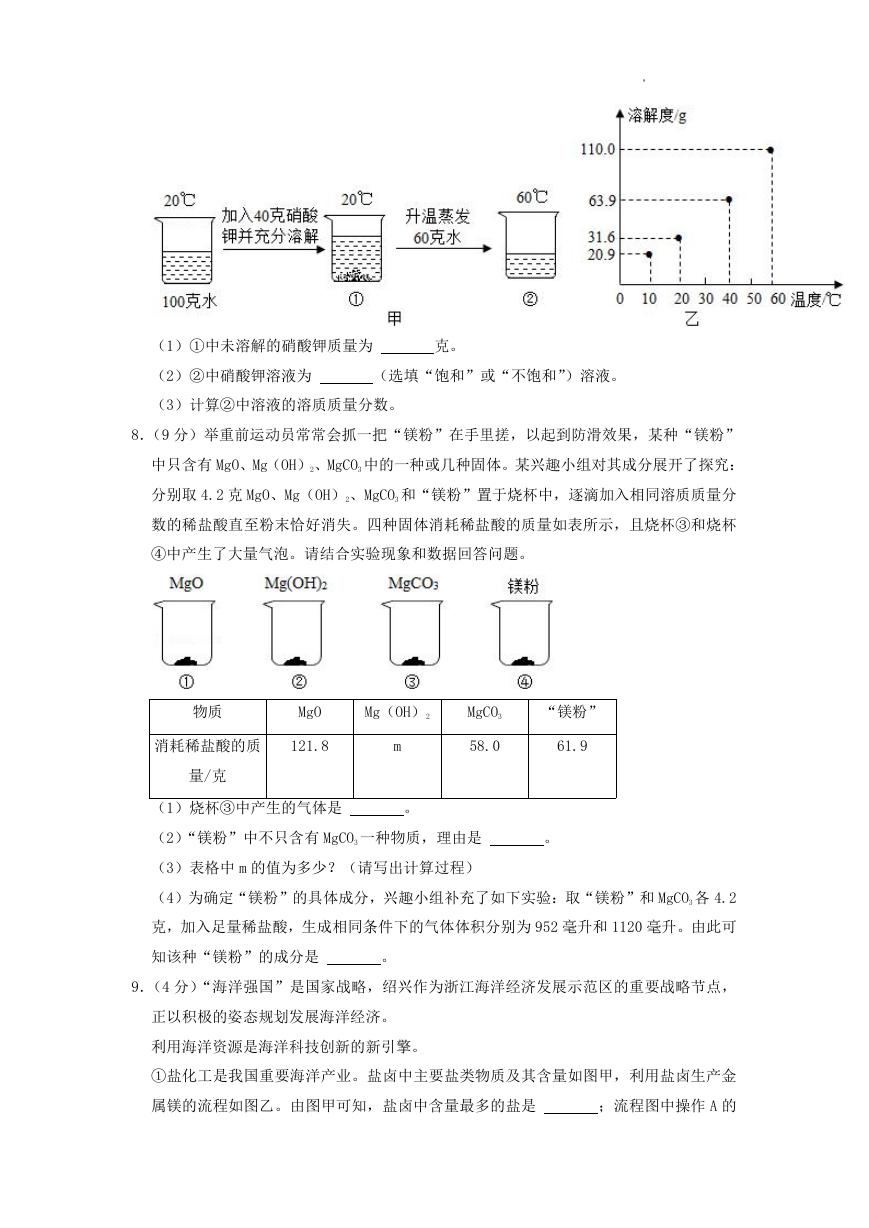
7.(6 分)某兴趣小组用硝酸钾进行了图甲所示的实验,硝酸钾溶解度与温度的关系如图乙。
学科 网(北 京)股 份有限 公司
�
(1)①中未溶解的硝酸钾质量为
克。
(2)②中硝酸钾溶液为
(选填“饱和”或“不饱和”)溶液。
(3)计算②中溶液的溶质质量分数。
8.(9 分)举重前运动员常常会抓一把“镁粉”在手里搓,以起到防滑效果,某种“镁粉”
中只含有 MgO、Mg(OH)2、MgCO3 中的一种或几种固体。某兴趣小组对其成分展开了探究:
分别取 4.2 克 MgO、Mg(OH)2、MgCO3 和“镁粉”置于烧杯中,逐滴加入相同溶质质量分
数的稀盐酸直至粉末恰好消失。四种固体消耗稀盐酸的质量如表所示,且烧杯③和烧杯
④中产生了大量气泡。请结合实验现象和数据回答问题。
物质
MgO
Mg(OH)2
MgCO3
“镁粉”
消耗稀盐酸的质
121.8
m
58.0
61.9
量/克
(1)烧杯③中产生的气体是
。
(2)“镁粉”中不只含有 MgCO3 一种物质,理由是
。
(3)表格中 m 的值为多少?(请写出计算过程)
(4)为确定“镁粉”的具体成分,兴趣小组补充了如下实验:取“镁粉”和 MgCO3 各 4.2
克,加入足量稀盐酸,生成相同条件下的气体体积分别为 952 毫升和 1120 毫升。由此可
知该种“镁粉”的成分是
。
9.(4 分)“海洋强国”是国家战略,绍兴作为浙江海洋经济发展示范区的重要战略节点,
正以积极的姿态规划发展海洋经济。
利用海洋资源是海洋科技创新的新引擎。
①盐化工是我国重要海洋产业。盐卤中主要盐类物质及其含量如图甲,利用盐卤生产金
属镁的流程如图乙。由图甲可知,盐卤中含量最多的盐是
;流程图中操作 A 的
学科 网(北 京)股 份有限 公司
�
名称是
;若生产过程中镁元素没有损失,且其他盐类中的镁元素质量可忽略不
计,则 1000 克盐卤可制备金属镁
克。
②地球表面 70%以上是海洋,各种海洋能源有待开发,你觉得开发前景广阔的能源
有
。
学科 网(北 京)股 份有限 公司
�
参考答案与试题解析
一、选择题(本题共 3 小题,每小题 4 分,共 12 分。下列各小题中只有一个选项符合题意)
1.(4 分)春秋初期,绍兴一带是南方的一个冶铁中心,其炼铁方法是在 1000℃左右的温度
下 2O3 ) 发 生 一 系 列 的 反 应 生 成 含 较 多 杂 质 的 海 绵 铁 。 其 中 主 要 化 学 反 应 为 :
3CO+Fe2O3
2Fe+3CO2。下列说法正确的是(
)
A.海绵铁是一种纯净物
B.Fe2O3 中铁元素的化合价为+3 价
C.上述反应中涉及的氧化物只有 2 种
D.炼铁过程中,木炭只是作为燃料使用
【分析】A、根据纯净物是由一种物质组成的,混合物有多种物质组成进行分析;
B、根据在化合物中正负化合价的代数和为零分析;
C、根据氧化物是由两种元素组成,其中一种是氧元素分析;
D、根据木炭不完全燃烧可以生成一氧化碳分析。
【解答】解:A、纯净物是由一种物质组成的,海绵铁含有多种物质;故 A 错误;
B、在化合物中正负化合价的代数和为零 2O3 中,氧元素为﹣3 价;故 B 正确;
C、氧化物是由两种元素组成,由化学方程式看出、氧化铁和二氧化碳;故 C 错误;
D、木炭不完全燃烧还可以生成一氧化碳,用于炼铁;故 D 错误;
故选:B。
【点评】本题主要考查了元素化合价的计算物质的分类、铁的冶炼、碳的性质等,在平
时的学习中加强识记即可解答。
2.(4 分)在做酸碱反应的实验时,向盛有氢氧化钠溶液的烧杯中,逐渐加入稀盐酸。烧杯
内相关物质的质量与加入稀盐酸质量的变化关系不正确的是(
)
学科 网(北 京)股 份有限 公司
�
A.
C.
B.
D.
【分析】氢氧化钠和稀盐酸反应生成氯化钠和水,随着稀盐酸的不断加入,氢氧化钠越
来越少,氯化钠越来越多。
【解答】解:A、随着反应进行,当恰好完全反应后,水的质量不断增大;
B、随着反应进行,当恰好完全反应后,该选项对应关系正确;
C、随着反应进行,当完全反应后氢氧化钠质量是 0;
D、随着稀盐酸的加入,一段时间内溶液中氯化氢质量是 0,溶液中的氯化氢质量不断增
大;
故选:D。
【点评】本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进
行分析、判断,从而得出正确的结论。
3.(4 分)小敏称取等质量的铜粉和铁粉,分别加入到 25 毫升溶质质量分数为 12%的硝酸银
溶液中(如图所示),充分反应。下列情况可能出现的是(
)
A.铁和铜都有剩余,甲、乙生成银的质量比为 7:8
B.铁和铜都没有剩余,甲、乙生成银的质量比为 1:1
C.铁有剩余,铜没有剩余,甲、乙生成银的质量比为 16:15
学科 网(北 京)股 份有限 公司
�
D.铜有剩余,铁没有剩余,甲、乙生成银的质量比为 15:14
【分析】根据题目中的数据解和化学方程式进行分析。
【解答】解:由于金属的活动性顺序是铁>铜>银,等质量的铜粉和铁粉,反应的质量
关系是:
Fe+2AgNO3═Fe(NO5)2+2Ag
56
Cu+8AgNO3═Cu(NO3)6+2Ag
64
216
216
A、铁和铜都有剩余时,因为硝酸银溶液的体积和溶质质量分数相同、乙生成银的质量比
为 1:5;
B、铁和铜都没有剩余,根据化学方程式,则生成银的质量比为:甲
:
=7:
8;
C、由方程式可知,每 56 份质量的铁能与 340 份质量的硝酸银溶液恰好反应,故铁有剩
余时,C 选项有可能出现;
D、等质量的铜和银,则铁一定有剩余;
故选:C。
【点评】本题考查了根据化学方程式的计算,解题时要注意根据物质的反应情况进行分
析。
二、填空题(本题共 2 小题,每空 2 分,共 12 分)
4.(6 分)科学是一门以实验为基础的学科。以下是实验室制取、收集、测量气体体积的常
用装置。
(1)实验室制取二氧化碳的发生装置可以选择 B (填字母)。
(2)检查装置 B 气密性的方法是:先关闭止水夹,然后 向长颈漏斗中加适量水,若
液面形成高度差,且一段时间后高度差不变,说明不漏气 。
(3)若用装置 C 测反应生成的二氧化碳体积,测得的体积比理论值小,原因可能是二氧
化碳具有 能溶于水且与水反应 的性质。
【分析】(1)根据制取二氧化碳的药品和反应条件选择发生装置;
学科 网(北 京)股 份有限 公司
�













 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc