2014 广西高考理科综合真题及答案
生物试题
一、选择题
1、下列有关细胞核的叙述,错误的是(
)
A.蛋白质是细胞核中染色质的组成成分
B.细胞核中可进行遗传物质的复制和转录
C.小分子物质可以通过核孔,大分子物质不能
D.有丝分裂过程中存在核膜消失和重新形成的现象
2.ATP 是细胞中重要的高能磷酸化合物。下列有关 ATP 的叙述,错误的是(
)
A.线粒体合成的 ATP 可在细胞核中发挥作用
B.机体在运动时消耗 ATP,睡眠时则不消耗 ATP
C.在有氧与缺氧的条件下细胞质基质中都能形成 ATP
D.植物根细胞吸收矿质元素离子所需的 ATP 来源于细胞呼吸作用
3、下列关于人体淋巴细胞的叙述,错误的是( )
A.在胸腺中发育成熟的 T 淋巴细胞可参与细胞免疫
B.效应 T 淋巴细胞可攻击被病原体感染的宿主细胞
C.T 淋巴细胞和 B 淋巴细胞都是由造血干细胞发育成的
D.T 细胞释放的淋巴因子不能使受到抗原刺激的 B 细胞增殖
4.某同学在①、②、③三种条件下培养大肠杆菌,这三种条件是:
①以葡萄糖为碳源的培养基,不断补充培养基,及时去除代谢产物
②以葡萄糖为碳源的培养基,不断补充培养基,不去除代谢产物
③以葡萄糖和乳糖为碳源的培养基,不补充培养基,不去除代谢产物
甲
乙
丙
A.甲、乙、丙
B.乙、丙、甲
C.丙、甲、乙
D. 丙、乙、甲
5.为验证单侧光照射会导致燕麦胚芽鞘中生长素分布不均匀这一结论,需要先利用琼脂块收集生长素,
之后再测定其含量。假定在单侧光照射下生长素的不均匀分布只与运输有关。下列收集生长素的方法(如
图所示)中,正确的是(
)
�
二、非选择题
31.(9 分)植物的光合作用受多种因素的影响。回答下列问题:
(1)右图表示了
对某种 C3 植物和某种 C4 植物
的影响。
当光照强度大于 p 时,C3 植物和 C4 植物中光能利用率高的是
植物。
通常提高光能利用率的措施有
的面积,补充
气体等。
( 2 ) 在 光 合 作 用 过 程 中 , C4 植 物 吸 收 的 CO2 被 固 定 后 首 先 形 成
化合物。
(3)C3 植物光合作用的暗反应需要光反应产生的 ATP 和 NADPH,这两种物质在叶绿体内形成的部位
是
。NADPH 的中文简称是
,其在暗反应中作为
剂,用于糖类等有机物的形成。
32.(9 分)小肠的吸收是指食物消化后的产物。水和无机盐等通过小肠上皮细胞进入血液和淋巴的过程。
0.9%的 NaCl 溶液是与兔的体液渗透压相等的生理盐水。某同学将处于麻醉状态的兔的一段排空小肠结扎成
甲、乙、丙、丁四个互不相同、长度相等的肠袋(血液循环正常),并进行实验,实验步骤和实验结果如表:
请根据实验结果回答问题:
( 1 ) 实 验 开 始 时 , 水 在 肠 腔 和 血 液 之 间 的 移 动 方 向 是 : 甲 组 从
; 丙 组
从
。在这一过程中水分子的运动方向是从容液浓度
处流向溶液浓度
处。本实验中水分子的这种移动过程称为
。
(2)比较乙和丁的实验结果,可推测小肠吸收 Na+时,需要
的参与。
33.(10 分)现有 A、B 两个密闭、透明的生态瓶,其生物组成和光照条件见下表。一段时间后,发现 A
瓶的生态系统较 B 瓶稳定。
生态瓶编号
光照 含微生物的泥沙
浮游藻类
水草
浮游动物
�
A
B
+
-
+
+
注“+”表示有,“-”表示有。
请回答:
+
+
+
+
+
+
(1)A 瓶中微生物、浮游藻类、水草和浮游动物共同组成了一个
,浮游藻类和水草的种
间关系为
。
(2)一段时间后,B 瓶中浮游藻类种群密度
,原因是
;浮游动物的种群密
度
,原因是
。
(3)生态系统中分解者的作用是
。
34.(14 分)现有 4 个小麦纯合品种,即抗锈病无芒、抗锈病有芒、感锈病无芒、感锈病有芒,已知抗锈
病对感锈病为显性,无芒对有芒为显性,且这两对相对性状各由一对等位基因控制。若用上述四个品种组
成两个杂交组合,使其 F1 均为抗锈病无芒,且这两个杂交组合的 F2 表现型及其数量比完全一致。回答问题:
(1)为实现上述目的,理论上,必需满足的条件有:在亲本中控制这两对相对性状生物两对等位基因
必须位于
,在形成配子时非等位基因要
,在受精时雌雄配子要
,
而 且 每 种 合 子 ( 受 精 卵 ) 的 存 活 率 也 要
。 那 么 。 这 两 个 杂 交 组 合 分 别 是
和
。
(2)上述两个杂交组合的全部 F2 植株自交得到 F3 种子,1 个 F2 植株上所结的全部 F3 种子种在一起,长
成的植株称为 1 个株系。理论上,在所有 F3 株系中,只表现出一对性状分离的株系有 4 种,那么,在这 4
种 株 系 中 , 每 种 株 系 的 表 现 型 及 其 数 量 比 分 别 是
,
,
和
。
2014 年普通高等学校招生全国统一考试(全国大纲卷)
理科综合能力测试化学部分
第 I 卷
6.下列叙述正确的是
A.锥形瓶可用作加热的反应器
B.室温下,不能将浓硫酸盛放在铁桶中
C.配制溶液定容时,俯视容量瓶刻度会使溶液浓度偏高
�
D.用蒸馏水润湿的试纸测溶液的 pH,一定会使结果偏低
7.NA 表示阿伏加德罗常数,下列叙述正确的是
A. lmol FeI2 与足量氯气反应时转移的电子数为 2NA
B.2 L0.5 mol • L-1 硫酸钾溶液中阴离子所带电荷数为 NA
C.1 mol Na202 固体中含离子总数为 4NA
D.丙烯和环丙烷组成的 42 g 混合气体中氢原子的个数为 6 NA
8.下列叙述错误的是
A. SO2 使溴水褪色与乙烯使 KMnO4 溶液褪色的原理相同
B.制备乙酸乙酯时可用热的 NaOH 溶液收集产物以除去其中的乙酸
C.用饱和食盐水替代水跟电石反应,可以减缓乙炔的产生速率
D.用 AgNO3 溶液可以鉴别 KC1 和 KI
9.右图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池(MH-Ni 电池)。下列有关说法
不正确的是
A.放电时正极反应为:NiOOH+H2O+e-→Ni(OH)2+OH-
B.电池的电解液可为 KOH 溶液
C.充电时负极反应为:MH+OH-→+H2O+M+e-
D.MH 是一类储氢材料,其氢密度越大,电池的能量密度越高
10.下列除杂方案错误的是
选项 被提纯的物质
杂质
除杂试剂
除杂方法
A.
B.
C.
D.
CO(g)
CO2(g)
NaOH 溶液、浓 H2SO4
NH4Cl(aq)
Fe3+(aq)
NaOH 溶液
Cl2(g)
HCl(g)
饱和食盐水、浓 H2SO4
Na2CO3(s)
NaHCO3(s)
—
洗气
过滤
洗气
灼烧
11.下 列 离 子 方 程 式 错 误 的 是
A . 向 Ba(OH)2 溶液中滴加稀硫酸:Ba2++2OH-+2H++ SO4
2- =BaS04↓+2H2O
B . 酸 性 介 质 中 KMnO4 氧化 H2O2:2MnO4
-+5H2O2+6H+ = 2Mn2++5O2↑+ 8H2O
C.等物质的量的 MgCl2、Ba(OH)2 和 HC1 溶液混合:Mg2++2OH-= Mg(OH)2↓
D.铅酸蓄电池充电时的正极反应:PbSO4 + 2H2O-2e- = PbO2+4H++SO4
2-
�
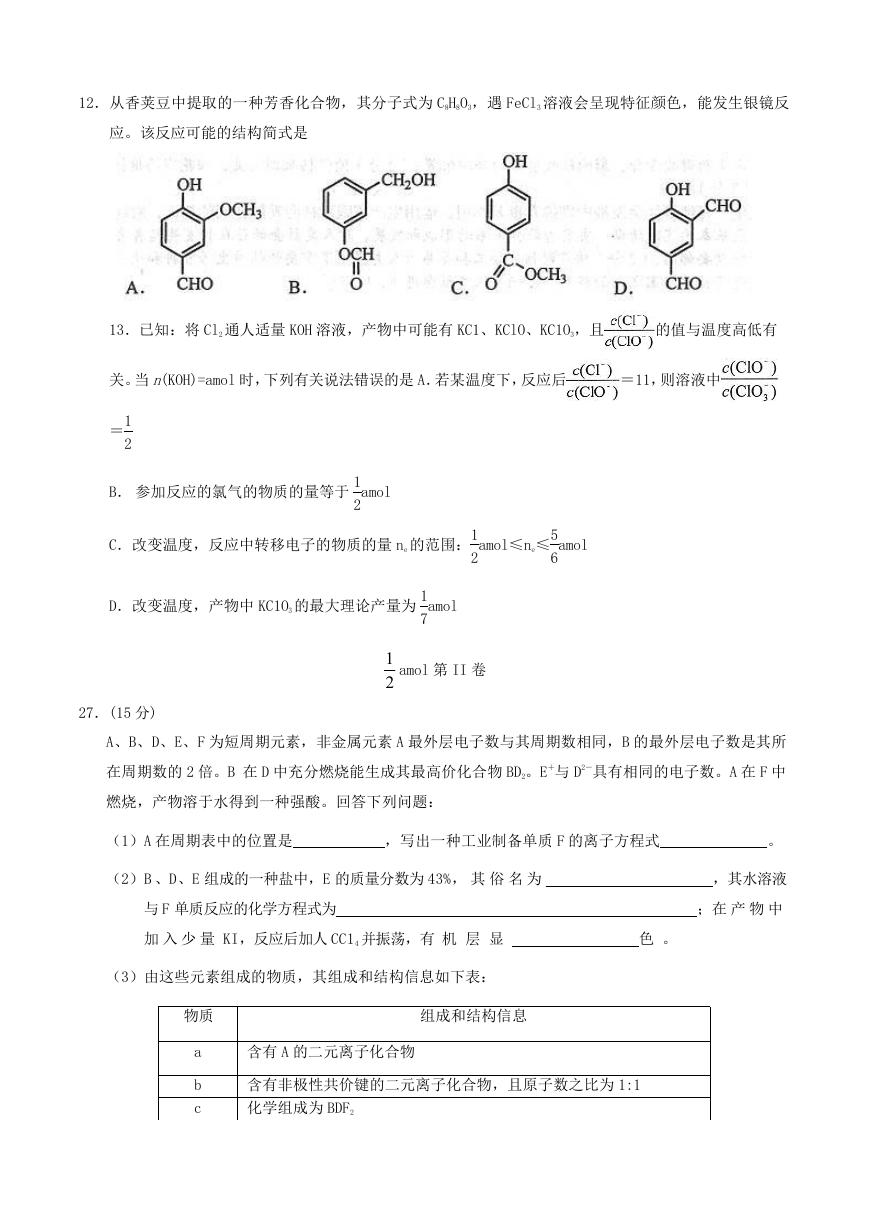
12.从香荚豆中提取的一种芳香化合物,其分子式为 C8H8O3,遇 FeCl3 溶液会呈现特征颜色,能发生银镜反
应。该反应可能的结构简式是
13.已知:将 Cl2 通人适量 KOH 溶液,产物中可能有 KC1、KClO、KC1O3,且
的值与温度高低有
关。当 n(KOH)=amol 时,下列有关说法错误的是 A.若某温度下,反应后
=11,则溶液中
1
=
2
B. 参加反应的氯气的物质的量等于
amol
1
2
C.改变温度,反应中转移电子的物质的量 ne 的范围:
1
2
5
amol≤ne≤
6
amol
D.改变温度,产物中 KC1O3 的最大理论产量为
1
amol
7
27.(15 分)
1
2
amol 第 II 卷
A、B、D、E、F 为短周期元素,非金属元素 A 最外层电子数与其周期数相同,B 的最外层电子数是其所
在周期数的 2 倍。B 在 D 中充分燃烧能生成其最高价化合物 BD2。E+与 D2-具有相同的电子数。A 在 F 中
燃烧,产物溶于水得到一种强酸。回答下列问题:
(1)A 在周期表中的位置是
,写出一种工业制备单质 F 的离子方程式
。
(2)B 、D、E 组成的一种盐中,E 的质量分数为 43%, 其 俗 名 为
与 F 单质反应的化学方程式为
,其水溶液
;在 产 物 中
加 入 少 量 KI,反应后加人 CC14 并振荡,有 机 层 显
色 。
(3)由这些元素组成的物质,其组成和结构信息如下表:
物质
a
b
c
组成和结构信息
含有 A 的二元离子化合物
含有非极性共价键的二元离子化合物,且原子数之比为 1:1
化学组成为 BDF2
�
d
只存在一种类型作用力且可导电的单质晶体
a 的化学式为
;b 的化学式为
;;c 的电子式为
;
d 的晶体类型是
。
(4)由 A 和 B、D 元素组成的两种二元化合物形成一类新能源物质。一种化合物分子通过
键构成
具有空腔的固体;另一种化合物(沼气的主要成分)分子进入该空腔,其分子的空间结构为
。
)
28.(15 分)
化合物 AX3 和单质 X2 在一定条件下反应可生成化合物 AX5。回答下列问题:
(1)已知 AX3 的熔点和沸点分别为-93.6 ℃和 76 ℃,AX5 的熔点为 167 ℃。室温时 AX3 与气体 X2 反应
生成 lmol AX5,放出热量 123.8 kJ。该反应的热化学方程式为
。
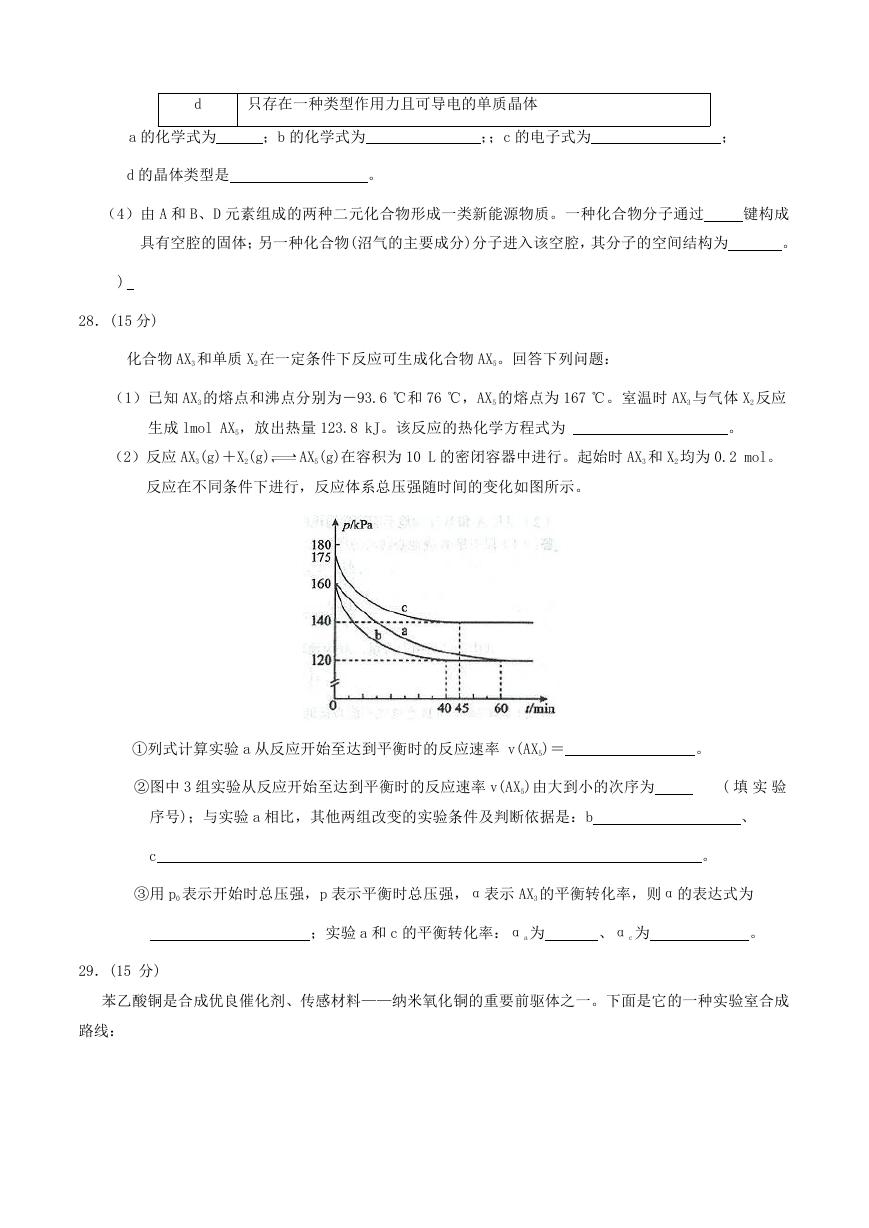
(2)反应 AX3(g)+X2(g)
AX5(g)在容积为 10 L 的密闭容器中进行。起始时 AX3 和 X2 均为 0.2 mol。
反应在不同条件下进行,反应体系总压强随时间的变化如图所示。
①列式计算实验 a 从反应开始至达到平衡时的反应速率 v(AX5)=
。
②图中 3 组实验从反应开始至达到平衡时的反应速率 v(AX5)由大到小的次序为
( 填 实 验
序号);与实验 a 相比,其他两组改变的实验条件及判断依据是:b
、
c
。
③用 p0 表示开始时总压强,p 表示平衡时总压强,α表示 AX3 的平衡转化率,则α的表达式为
;实验 a 和 c 的平衡转化率:αa 为
、αc 为
。
29.(15 分)
苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一。下面是它的一种实验室合成
路线:
�
制备苯乙酸的装置示意图如下(加热和夹持装置等略):
已知:苯乙酸的熔点为 76.5 ℃,微溶于冷水,溶于乙醇。
回答下列问题:
(1)在 250 mL 三口瓶 a 中加入 70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是
。
(2)将 a 中的溶液加热至 100 ℃,缓缓滴加 40 g 苯乙腈到硫酸溶液中,然后升温至 130 ℃继续反
应。在装置中,仪器 b 的作用是
;仪器 c 的名称是
,
其作用是
。
反应结束后加适量冷水,再分离出苯乙酸粗品。加人冷水的目的是
。下列仪器中
可用于分离苯乙酸粗品的是
(填标号)。
A.分液漏斗
B.漏斗
C.烧杯
D.直形冷凝管E.玻璃棒
(3)提纯粗苯乙酸的方法是
,最终得到 44 g 纯品,则苯乙酸的产率是
。
(4)用 CuCl2
• 2H2O 和 NaOH 溶液制备适量 Cu(OH)2 沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗
干净的实验操作和现象是
。
(5)将苯乙酸加人到乙醇与水的混合溶剂中,充分溶解后,加入 Cu(OH)2 搅拌 30min,过滤,滤液静
置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是
。
30.(15 分)
“心得安”是治疗心脏病的药物,下面是它的一种合成路线(具体反应条件和部分试剂略):
回答下列问题:
�
(1)试剂 a 是
,试剂 b 的结构简式为
,b 中官能团的名称
是
。
(2)③的反应类型是
。
(3)心得安的分子式为
(4)试剂 b 可由丙烷经三步反应合成:
反应 1 的试剂与条件为
反应 2 的化学方程式为
反应 3 的反应类型是
。
,
,
。(其他合理答案也给分)
(5)芳香化合物 D 是 1-萘酚的同分异构体,其分子中有两个官能团,能发生银镜反应,D 能被 KMnO4
酸性溶液氧化成 E( C2H4O2) 和芳香化合物 F (C8H6O4),E 和 F 与碳酸氢钠溶液反应均能放出 CO2
气体,F 芳环上的一硝化产物只有一种。D 的结构简式为
;
由 F 生成一硝化产物的化学方程式为
,
该产物的名称是
。
2014 年全国全国统一招生考试大纲卷物理部分
二、选择题:本题共 8 小题,每小题 6 分。在每小题给出的四个选项中,有的只有一项符合题目要求,有
的有多项符合题目要求。全部选对的得 6 分,选对但不全的得 3 分,有选错的得 0 分。
14.—质点沿 x 轴做直线运动,其 I/-?图像如图所示。质点在/ = 0 时位于 x = 5m 处,开始沿 x 轴正向运
动。当 k 8s.时,质点在轴上的位置为
�














 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc