2006 年四川省南充市中考化学真题及答案
(满分 70 分)
一
二
三
四
总分
总分人
题号
得分
可能用到的相对原子质量:H—1
C—12
N—14
0—16
Cl—35.5
Ca—40
得分
评分人
一、选择题(本题包括 14 个小题。每小题 2 分,共 28 分)每小题只有一
个选项符合题意。将符合题意的选项序号填入括号内。
1.在互联网上用 Coogle 搜索“中央电视台每周质量报告”时,可搜索到被曝光的事件中一
定涉及到化学变化的是
(
)
A.用毛发水、酱色、水、盐等兑制成“假酱油”
B.用工业石蜡等涂抹在瓜子表面给瓜子“美容”
C.用硫磺燃烧法熏蒸粉丝
D.用淀粉、蔗糖、奶香精等掺和成“假奶粉”
2.生活中废弃的铝质易拉罐、破铁锅、废铜线等可归为一类加以回收,它们属于 (
)
A.有机物
B.金属或合金
C.氧化物
D.非金属
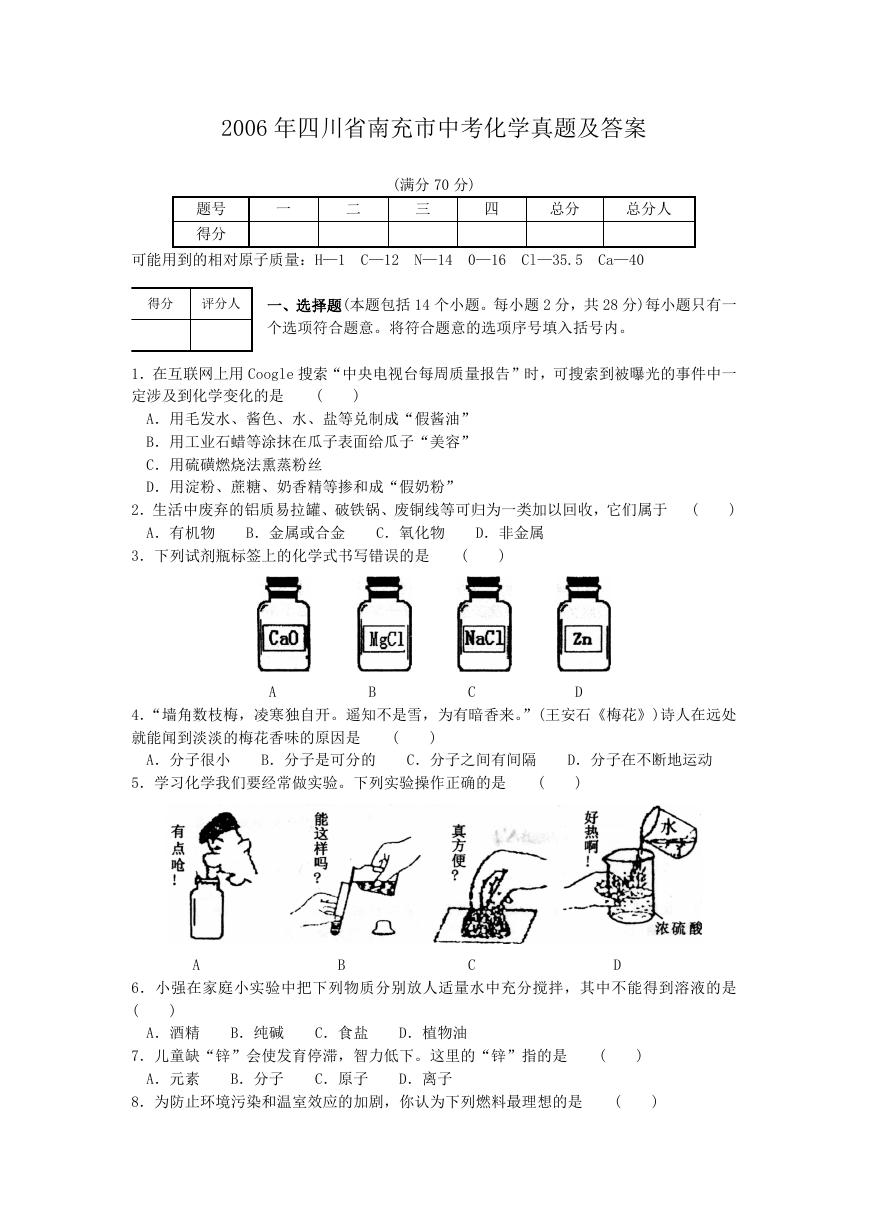
3.下列试剂瓶标签上的化学式书写错误的是
(
)
A
B
C
D
4.“墙角数枝梅,凌寒独自开。遥知不是雪,为有暗香来。”(王安石《梅花》)诗人在远处
就能闻到淡淡的梅花香味的原因是
(
)
A.分子很小
B.分子是可分的
C.分子之间有间隔
5.学习化学我们要经常做实验。下列实验操作正确的是
(
D.分子在不断地运动
)
A
B
C
D
6.小强在家庭小实验中把下列物质分别放人适量水中充分搅拌,其中不能得到溶液的是
(
)
A.酒精
B.纯碱
C.食盐
D.植物油
7.儿童缺“锌”会使发育停滞,智力低下。这里的“锌”指的是
(
)
A.元素
B.分子
C.原子
D.离子
8.为防止环境污染和温室效应的加剧,你认为下列燃料最理想的是
(
)
�
A.天然气
B.石油液化气
C.煤
D.氢气
9.芬太奴是强有力的麻醉剂,在军事上作为“非致命武器”曾被用作解救人质,其化学式
为 C20H24N2O,下列关于芬太奴的说法中不正确的是
(
)
A.芬太奴的每一个分子中含有 47 个原子
B.芬太奴是由碳、氢、氮、氧四种元素组成的物质
C.一个芬太奴分子中含有一个氮气分子
D.芬太奴中碳、氢、氮、氧元素的质量比为 60:6:7:4
lO.《美国化学会杂志》报道了中国科学家以二氧化碳和钠在一定条件下制得金刚石,其化
学方程式为 3C02+4Na
℃470
80MPa
2X+C(金刚石)。则 X 的化学式为
(
)
A.Na202
B.Na2CO3
C.Na2O
D.Na4C206
11.海水淡化可采用膜分离技术,如右图所示,对淡化膜右侧的
海水加压,水分子可以透过淡化膜进人左侧淡水池,而海水中的
各种离子不能通过淡化膜,从而得到淡水,对加压后右侧海水成
分变化进行分析,正确的是
)
(
A.溶质质量增加
C.溶剂质量减少
B.溶液质量不变
D.溶质质量分数不变
12.某些食品包装袋内有一小包物质,用来吸收氧气和水分,以防止食品腐败,常称“双吸
剂”。下列物质属于“双吸剂”的是
(
)
A.铁粉
B.炭粉
C.氯化钙
D.生石灰
13.小明想除去卫生间瓷砖上的铁锈痕迹,在用清水洗涤之前,他从家中选择了一种最合适
的物质对铁锈进行处理,这种物质是
(
)
A.汽油
B.食盐水
C.白醋
D.米酒
14.现有 X、Y、Z 三种金属,把 X、Y 分别插人 Z 的硝酸盐溶液中,X 无反应,Y 表面上析出
Z。判断这三种金属活动性由强到弱的顺序是
Y
)
D.X
B. Y X Z
A.Y Z X
C. X
(
Z
Z
Y
得分
评分人
二、(本题包括 6 个小题。共 25 分)
15.氧气、干冰、熟石灰和纯碱四种物质分别与下列图中的人类活动有关,请将他们的化学..
式.填在图下相应的括号内。
抹墙壁
急救病人
蒸馒头
人工降雨
(
)
(
)
(
)
(
16.硫酸铜是重金属盐,人误食中毒后,为减轻毒性,最好服用
)
;硫酸铜溶液
�
与石灰乳(熟石灰的悬浊液)混合,可以制得农药波尔多液。配制波尔多液发生化学反应的方
程式为
17.今年 3 月 25 日,重庆开县发生天然气井漏事故。井漏喷出的气体主要是甲烷,另外还
含有大量的硫化氢气体。硫化氢(H2S)气体是一种有臭鸡蛋气味、剧毒的无色气体,密度比
空气大,能溶于水,其水溶液显酸性,叫氢硫酸。请回答:
,其反应的基本类型是
。
(1)H2S 中硫的化合价为
价。氢硫酸与盐酸一样能与 NaOH 溶液发生中和反应,生成
硫化钠和水。写出该反应的化学方程式
。
(2)当发生井漏事故时,下列自救措施合理的是
A.逃生时应往地势高处逆风跑
C.立即用浸过水或弱碱性溶液的毛巾捂住口鼻
(3)为降低危害程度,可以将喷出的气体点燃,其中硫化氢燃烧时,生成二氧化硫和水,
;消防队员还可向空中喷
B.逃生时应往地势低处顺风跑
(填序号)。
该燃烧反应的化学方程式为
洒
,以减少空气中硫化氢的含量。
(4)违反操作规程或安全设施不完备,是引发事故的常见原因,请结合具体的化学实验,
说出避免实验事故应注意的一个问题
18.为配合南充市创建中国优秀旅游城市活动,某校在综合实践活动中开展了相关研究。
。
(1)调查了解南充市的环境现状 查阅环境质量监测报告:我市降水的 pH 年均值约为
5.07,说明我市降水显
性(选填“酸”、“碱”或“中”)。嘉陵江清泉寺饮用水
源地水质为 V 类水质,主要超标项目为总氮、粪大肠菌群。其水质污染的原因可能是
(任答一个原因)。
(2)寻觅丰富的古丝绸文化 我市自古以盛产蚕丝绸闻名,素有“千年绸都南充城”之称。
这里的“蚕丝”是指
(填序号)
A.人造纤维 B.天然纤维 C.合成纤维
(3)参与建设生态南充城 在社区调查中,居民提出了以下建议:①采取措施,减少和控
制污染气体的排放;②禁止在嘉陵江敞放鸭子,以免大量鸭粪污染母亲河;③植树造林,增
大绿化面积;④就地焚烧垃圾,减少固体污染物。你认为合理的是
19.已知:BaCl2+Na2SO4=BaS04↓+2NaCl。向一定量的 BaCl2 溶液中加入一定量的 Na2S04 溶液,
种情况,这几种情况中一定都
充分反应后过滤。你认为滤液中的溶质的组成最多有↓
含有
20.小玲通过查阅资料知道了牙膏的主要成分。她将一定比例的碳酸钙粉末和食盐倒人小烧
杯中,然后加人适量的甘油(保湿剂)、甜味剂和香精等,搅拌均匀后制得牙膏。
(1)牙膏是
(2)牙膏中的碳酸钙粉末作摩擦剂,提高洁齿效果。这种碳酸钙是将二氧化碳通人石灰水
制得的,请写出该反应的化学方程式
(选填“纯净物”或“混合物”)。
(填化学式)。
(填序号)。
。
得分
评分人
三、(本题包括 2 个小题。共 10 分)
21.已知溶液中氢离子浓度越大,溶液的酸性越强,溶液的 pH 越小。有一同学在实验室中
是这样测某溶液 pH 的:他先用蒸馏水润湿 pH 试纸,然后用
(填仪器)蘸取试样进行
检测,该同学测得的 PH 是否一定会有误差?
22.化学兴趣小组为了探究化学实验室的一种黑色粉末和一瓶标签破损的无色溶液(如右图
�
所示)可能是什么物质,大胆猜想并设计实验进行验证。
[发现问题]当把黑色粉末与无色溶液混合时即产生气泡。
[查阅资料]初中化学实验室常见的黑色粉末有 CuO、MnO:、Fe304、铁粉、炭粉等。
[提出假设]黑色粉末是
[设计实验]①向盛有少许黑色粉末的试管中加入适量的无色溶液;②检验试管中产生的气
。(只写一种假设)
,无色溶液是
体(写出操作方法)
[实验现象]
[实验结论]①该反应的化学方程式是
②此气体是
,原假设成立。
。
。
。
[讨
论]若要制取该气体,应从下图中选择发生反应的装置为
(填序号)。
A
B
得分 评分人
四、(本题包括 1 个小题.共 7 分)
23.石灰厂为了测定一批石灰石样品中碳酸钙的质量分数,取用 4 g 石灰石样品,把 20 g
稀盐酸分 4 次加人样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶于水),
充分反应后经过滤、干燥等操作,最后称量,得实验数据如下表:
稀盐酸的用量 第一次加入5 g 第二次加入5 g 第三次加入5 g 第四次加人5 g
剩余固体的质量
3 g
2 g
l g
1 g
(1)该石灰石样品中碳酸钙的质量分数是
(2)计算该稀盐酸的溶质质量分数(写出计算过程,结果精确到 0.1%)。
;
�
南充市二 00 六年高中阶段学校招生统一考试(课改区)
化学试题参考答案及评分意见
说明:
1.答案中所写化学式有错误者不给分,所书写的化学方程式未配平或未注明反应条件
及生成物状态,而其余正确者,给该方程式一半的分。
2.考生作出的其它合理答案,参照本评分意见给分。
3.本试题满分 70 分。
一、(共 28 分。每小题 2 分)
题号 l
答案 C
2
B
3
B
4
D
5
B
6
D
7
A
8
D
9
C
10
ll
12 13
14
B
C
A
C
A
二、(共 25 分)
15.Ca(OH)2
16.蛋清(1 分)
17.(1) -2(1 分)
Na2C03
C02
02
CuS04+ca(OH)2=Cu(OH)2 ↓+CaSO4(2 分) 复分解反应(1 分)
(各 1 分)共 4 分
H2S+2NaOH=Na2S+2H20 (2 分)
(2)A C
(1 分)
(3)2H2S+302
点燃
2S02+2H20 (2 分
)弱碱性溶液(或水等)(1 分)
(4)点燃氢气前一定要检验氢气的纯度等。(只要符合题意即可)
(1 分)共 8 分
18.(1)酸 生活污水(或工业废水、或农业用水等。答其它原因只要合理即可给分)
(各 1 分)
(2)B
(1 分)
(3)①②③
(1 分)共 4 分
NaCl
19. 3
20.(1)混合物
(各 1 分)共 2 分
(2)C02+Ca(OH)2===CaC03↓+H20
三、(共 10 分)
21.玻璃棒 不一定会有误差
22.假设一:
(1 分)
(2 分)共 3 分
(各 1 分)共 2 分
[提出假设]二氧化锰(或 Mn02) 双氧水(或 H2O2:)
[设计实验]用带火星的木条伸人试管中
(1 分)
(1 分)
[实验现象]带火星的木条复燃
[实验结论]①2H202
2MnO
2H20+02 ↑
(2 分)
(各 1 分)
②氧气(或 O2)
[讨 论] B
或假设二:
(1 分)
(1 分)共 8 分
稀硫酸(或稀 H2S04)
(各 1 分)
[提出假设]:铁粉(或 Fe)
[设计实验]把燃着的木条移近试管口
[实验现象]气体燃烧,火焰呈淡蓝色
[实验结论]①Fe+H2SO4=FeS04+H2↑
②氢气(或 H2)
[讨 论]B
四、(共 7 分)
23.(1)75%
(2 分)
(1 分)
(1 分)
(2 分)
(1 分)
(1 分)共 8 分
�
(2)解:由表中数据可知第三次加入 5 g 稀盐酸后,3 g 碳酸钙与 15 g 稀盐酸刚好完全
反应。
设稀盐酸中溶质的质量为 x
2HCl
CaC03 +
73
100
x
3g
100
g3
73
x
x=2.19 g
=
===
CaCl2 +
H20
+
C02 ↑
(1 分)
(1 分)
(1 分)
稀盐酸的溶质质量分数为:
19.2
g
15
g
×100%=14.6%
(2 分)共 7 分
�











 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc