2021-2022 学年辽宁省沈阳市皇姑区九年级上学期化学期末
试题及答案
相对原子质量: H.1
C.12
N.14
O.16
Fe.56
第一部分选择题(共 l5 分)
(本题有 l3 道小题,l~11 每题 l 分;l2、13 每题 2 分。每小题只有一个最符合要求的选项。)
1.下列变化中属于化学变化的是
A.石墨导电 B.酒精挥发 C.冰雪融化 D.光合作用
2.在集气瓶中装满某气体,可能是下列气体中的一种:①二氧化碳②氧气③空气④氮气。
若将燃着的小木条伸入集气瓶中观察到火焰立即熄灭,则该气体可能是
A.①或② B.②或③ C.①或④ D.③或④
3.下列物质中由原子构成的是
A.金刚石 B.氧气 C.氯化钠 D.甲烷
4.下列对实验现象的描述正确的是
A.木炭燃烧生成二氧化碳
B。铁丝在空气中燃烧生成黑色固体
C.氢氧化钠溶液与硫酸铜溶液混合产生蓝色氢氧化铜沉淀
D.加热“铜绿”时,绿色固体会逐渐变成黑色粉末,试管壁出现小水珠
5.下列物质中不属于“金属材料”的是
A.储氢合金 B.氧化铜 C.焊锡 D.硬铝
6.下列物质中属于纯净物的是
A.从空气中分离得到的稀有气体
B.经过沉淀、过滤后的矿泉水
C.部分结冰的蒸馏水
D.加热二氧化锰和氯酸钾完全分解后的剩余固体
7.规范的实验操作也是实验成功和安全的重要保证。下列实验操作中正确的是
A
B
C
D
塞紧橡皮塞
处理废弃药品
倾倒液体药品
检查装置气密性
8.下列化学符号所表示的对应关系中正确的是
A.2个铵根离子——2NH3
+
B.“
”可表示为2H
�
C.碳酸钠——NaCO3
D.钠离子的结构示意图为
9.物质发生分解反应后能够得到的物质有
A.单质
B.氧化物
C.化合物
D.以上均可能
10.下列有关金属的叙述中正确的是
A.合金中一定不含有非金属
B.不锈钢是永远不会生锈的钢铁
C.生铁和钢中碳元素的含量有所不同
D.铁与稀盐酸反应生成氯化铁和氢气
11.根据下面化学反应的微观示意图分析,得出结论正确的是
A.反应前后分子种类发生改变
B.丙物质的相对分子质量是l8g
C.反应前后各元素化合价均未发生变化
D.参加反应的物质甲与乙的分子个数比为l:1
12.2021年诺贝尔化学奖回归传统化学。得主利斯特通过实验证明了脯氨酸(C5H9NO2)可以驱
动不对称催化反应,所得产物具有不对称选择性。下列说法中正确的是
A.脯氨酸中含有一个氧气分子
B.脯氨酸中氮元素的质量分数为20%
C.腩氨酸中碳元素与氢元素的个数比为5:9
D.脯氨酸是由碳、氢、氧、氮四种元素组成的化含物
13.下列图示所指四个实验探究中不能达到实验目的的是
A.微粒不断运动 B.质量守恒定律
C.微粒间有空隙 D.蜡烛中含碳元索
第二部分非选择题(共50分)
14.(11分)氧气、二氧化碳和氢气是我们初中阶段学习化学过程中涉及的三种重要气体。
在实验室中,强强化学兴趣小组同学们利用下图所示装置制取并研究其相关性质和用途。
�
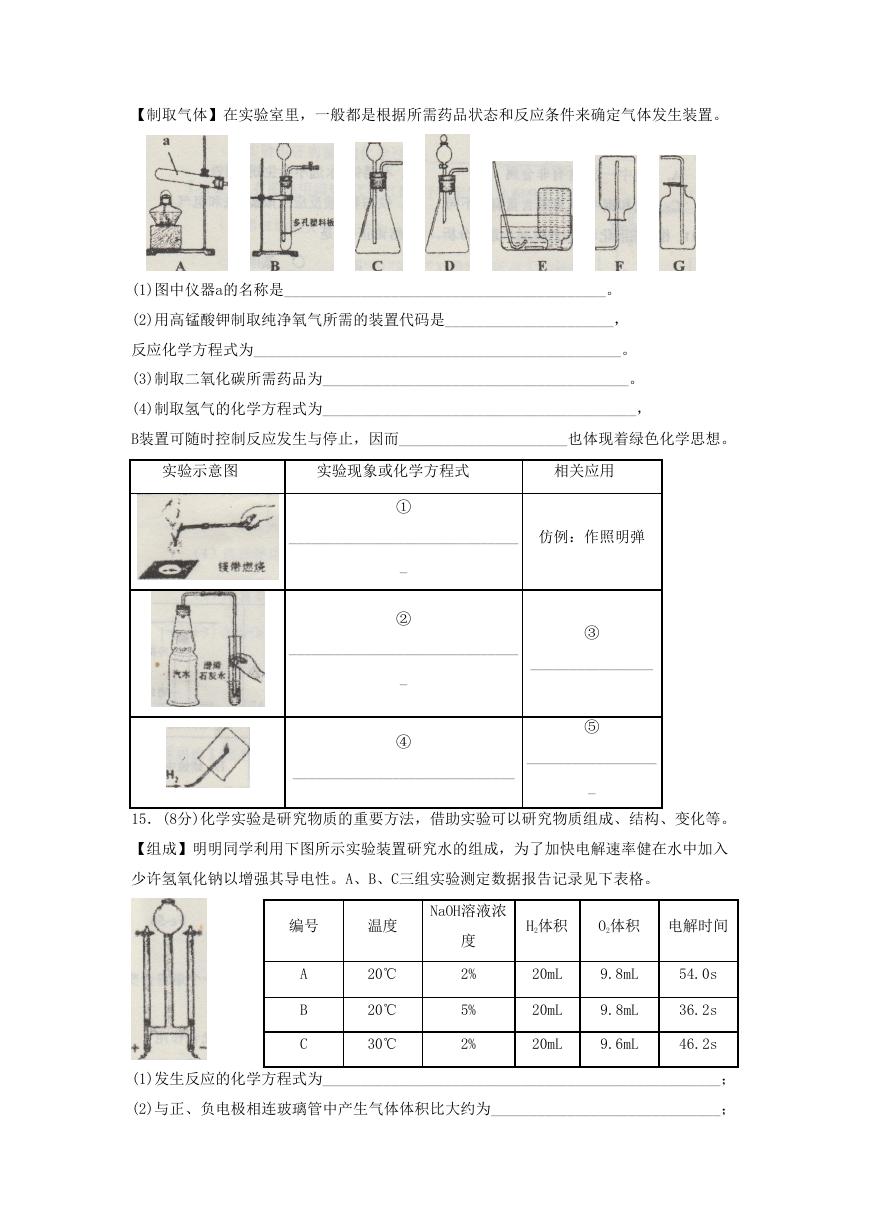
【制取气体】在实验室里,一般都是根据所需药品状态和反应条件来确定气体发生装置。
(1)图中仪器a的名称是__________________________________________。
(2)用高锰酸钾制取纯净氧气所需的装置代码是______________________,
反应化学方程式为________________________________________________。
(3)制取二氧化碳所需药品为________________________________________。
(4)制取氢气的化学方程式为_________________________________________,
B装置可随时控制反应发生与停止,因而______________________也体现着绿色化学思想。
实验示意图
实验现象或化学方程式
相关应用
①
______________________________
仿例:作照明弹
_
②
______________________________
_
④
_____________________________
③
________________
⑤
_________________
_
15.(8分)化学实验是研究物质的重要方法,借助实验可以研究物质组成、结构、变化等。
【组成】明明同学利用下图所示实验装置研究水的组成,为了加快电解速率健在水中加入
少许氢氧化钠以增强其导电性。A、B、C三组实验测定数据报告记录见下表格。
编号
温度
A
B
C
20℃
20℃
30℃
NaOH溶液浓
度
2%
5%
2%
H2体积 O2体积 电解时间
20mL
9.8mL
54.0s
20mL
9.8mL
36.2s
20mL
9.6mL
46.2s
(1)发生反应的化学方程式为____________________________________________________;
(2)与正、负电极相连玻璃管中产生气体体积比大约为______________________________;
�
(3)通过对比实验A和C,可得出的结论是__________________________________________。
【净化】亮亮同学取少量浑浊的雨后积水倒入烧杯中,先加入少量的明矾充分搅拌溶解后静
置一段时间;然后再利用右图所示的装置进行过滤,其中错误的操作是________________。
【变化】下图是法国化学家拉瓦锡研究化学反应前后质量变化时加热氧化汞的示意图。
(1)甲物质的化学式为______________________________________;
(2)从组成元素的角度分析,丙物质属于______________________________;
(3)从微观角度分析,化学反应前后质量守恒的原因是________________________________
_______________________________________________________________________________
______________________________________________________________________________。
16.(9 分)燃烧是一种发光、发热的剧烈的化学反应。在日常生活中,燃烧现象屡见不鲜。
人们对燃烧的认识也是不断发展的,现邀请你和兴趣小组一起去探究下图所示三个实验。
(1)林林同学为了探究物质燃烧的条件,设计了如图 1 所示的实验。通过对比观察①和②两
处的实验现象,能得出可燃物燃烧需要___________________________________________,
发生反应的化学方程式为_________________________________________;试着推测红磷的
着火点可能________(填“>”、“<”或“=”)80℃(不考虑热量损失)。
(2)芳芳同学认为林林同学的实验存在明显不足,她尝试进行了如图 2 所示的改进。将与图
l 中铜片上等质量的红磷和白磷分别放入两支充满空气的试管中,再将试管口系上气球后放
入图 2 所示的烧杯中。对比两处白磷产生的现象说明可燃物燃烧需要满足的条件是_______;
�
改进后实验的优点是______________。
(3)亮亮同学利用如图 3 所示的装置模拟面粉爆炸实验。具体的实验操作步骤依次为:点燃
蜡烛;用塑料盖盖住金属筒;用打气筒压入空气。发现塑料盖被掀起。实验中鼓入空气的作
用是________________________________________。
①实验说明“面粉爆炸”是因为发生剧烈燃烧,且又发生在______________________。
②实验也说明影响面粉燃烧速率的因素为______________________________________。
③在汽油加油站、面粉加工厂和煤矿坑道等场所,为防止爆炸事故发生,应该杜绝_____。
17.(12 分)金属材料发展突飞猛进,其对人类生产、生活和社会发展有着极其重要作用。
人类制得并利用金属历史悠久,研究金属发展过程为:存在形式→冶炼方法→性质应用。
【存在形式】金属化合物在自然界中以矿物的形式存在。现有①铝土矿②磁铁矿③黄铜矿三
种矿石,其中可用来冶炼金属铜的是________________。
【冶炼方法】(1)电解熔融氯化镁可得到镁和氯气的化学方程式为_____________________。
(2)《淮南万毕术》中有“曾青得铁则化为铜”的记载,其化学方程式为
_________________________________,基本反应类型是______________。
(3)下图为工业高炉炼铁剖面图和实验室模拟工业炼铁的部分仪器与装置。
①工业炼铁时所需原料有___________________________________________。
②模拟炼铁时,A 装置 a 口需要与 B 装置的(填字母)_______________口相连接,
模拟炼铁的化学反应方程式为_______________________。
③实验产生的尾气不能直接排放,你选择的处理装置是____________________。
④若用含氧化铁 240 t 的赤铁矿石为原料进行炼铁,理论上可得到含杂质 4%的生铁
质量为________________________。
【性质用途】(1)用铁制锅铲需要加上木柄或塑料柄,这是因为铁具有_______________。
(2)在常温下,铝能“自我保护”的原因是___________________________。
18.(10 分)冬冬兴趣班小组“测定空气中氧气体积分数”实验探究方案如下面三图所示。
【实验一】右图是教材中“测定空气中氧气体积分数”实验装置。
(1)当集气瓶冷却至室温时,打开止水夹,可观察到的现象是________________________。
(2)实验也证明氮气的化学性质是________________________________________________。
�
【实验二】右图是用蜡烛来代替红磷进行测定氧气体积分数实验。
(1)蜡烛燃烧文字表达式为___________________________________________________。
(2)实验___________(填“可”或“否”)得出接近事实的结论,理由是____________。
【实验三】“测定空气中氧气体积分数”成功的关键在于装置的密闭性和药品的合理选择。
下图所示为兴趣小组同学对用“暖贴”实验可行性的探究方案。将装有过量铁粉的暖贴吊在
集气瓶中,在装置的上方连接了氧气传感器,电脑实时读数,同时绘制出浓度变化曲线。
(1)选择使用铁粉实验的理由是___________________________________。
(2)用食盐水浸滤纸包的目的是___________________________________。
(3)在实验过程中,氧气浓度变化的趋势为_________________________;
反应前装置内氧气浓度为 21.1%,35min 时氧气浓度读数约为___________________。
通过观察发现:若用铁粉实验时间会稍长,但消耗氧气更彻底,所得数据会更接近于事实。
【拓展思维】综上研究,请你另谈一点对教材上“空气中氧气含量测定”实验的具体改进
意见是_______________________________________________________________________。
参考答案:
1.D
2.C 3.A
4.D
5.B
6.C 7.D
8.D
9.D
10.C
11.A
12.D
13.B
14.(1)试管(或大试管)
�
(2)AE
2KMnO4
△ K2MnO4+MnO2+O2↑
(3)石灰石(或大理石)和稀盐酸
(4)Zn+H2SO4=ZnSO4+H2↑
节约药品
①2Mg+O2
点燃 2MgO(或:镁带剧烈燃烧,发出耀眼白光,放出大量热,产生一缕白烟,
生成白色粉末状固体。)
②CO2+Ca(OH)2=CaCO3↓+H2O(或:澄清石灰水变浑浊)
③检验二氧化碳气体
④2H2+O2
点燃 2H2O(或:产生淡蓝色火焰,放出大量热,火焰上罩一干冷烧杯,烧杯
上有水雾出现。)
⑤氢气作燃料
15.【组成】(1) 2H2O 通电 2H2↑+O2↑
(2)1:2
(3)NaOH 溶液浓度相同时温度越高,水电解速率越快。
【净化】没用玻璃棒引流
【变化】(1)HgO
(2)单质
(3)在化学反应前后,原子的种类、数目、质量均没有改变。
16.(1)温度达到着火点
4P+5O2
点燃 2P2O5
˃
(2)可燃物要与氧气(空气)接触
密闭性好,产生的有毒物质不会逸出,污染小
(3)增大面粉与氧气(空气)接触面积
①有限空间内
②面粉与氧气的接触面积
③一切火源
17. 【存在形式】黄铜矿(或③)
【冶炼方法】(1)MgCl2
通电 Mg+O2↑
(2)Fe+CuSO4=FeSO4+Cu
置换反应
(3)①铁矿石、焦炭、石灰石、热空气
②c
Fe2O3+3CO 点燃 2Fe+3CO2
③C 或 D
④175t
【性质用途】(1)导热性
(2)常温下,铝在空气(氧气)中形成一层致密的氧化铝薄膜,隔绝氧气
�
和水
18.【实验一】(1)水进入集气瓶约占集气瓶容积的五分之一
(2)不燃烧不支持燃烧
【实验二】(1)石蜡+氧气 点燃→水+二氧化碳
(2)否
石蜡燃烧虽然消耗氧气,但产生二氧化碳气体,使集气瓶内气压变化不大
【实验三】(1)铁生锈消耗氧气且生成物为固体
(2)加快铁生锈的速率
(3)氧气浓度逐渐减小
1%
【拓展思维】在密闭容器中,使用白磷代替红磷,并用放大镜点燃白磷的方法来测定空气
中氧气含量。
�















 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc