2020-2021 学年上海市闵行区九年级上学期化学 12 月月考
试题及答案
相对原子质量:H-1
O-16
C-12
S-32
Cu-64
一、选择题(第 1-14 题单选,每题 1 分,第 15-17 题不定项,每题 2 分,共 20 分)
1. 春有百花秋有月、夏有凉风冬有雪是我县濒胡公园的生动写照,下列说法正确的是
A. 春天的公园花香四溢,沁人心脾,说明分子是由原子构成的
B. 将赤东湖水经沉降、过滤、吸附,灭菌等净化操作后,可供人们生活用水
C. 用肥皂水不可以区分公园人工湖内的水是硬水和软水
D. 水体有一定的自净功能,部分工业污水可直接向人工湖内排放
【答案】B
【解析】
【分析】
【详解】A、由分子的性质可知,花香四溢的主要原因是分子在不断的运动,与由原子构成
无关,故错误;
B、将黄河水经沉降、过滤、吸附、灭菌等净化操作后,可供人类生活用水,故正确;
C、肥皂水能够区分软水和硬水,遇肥皂水泡沫多浮渣少的是软水,复杂多泡沫少的是硬水,
故错误;
D、水体自净能力有限,工业污水会污染水,不能直接排放,故错误。
故选:B。
2. 2018 年 11 月 8 日,美国加州发生特大型山火,历时半月才将其基本扑灭。下列关于森
林火灾应急处理措施或原因不合理的是(
)
A. 砍掉或清理大火面前的干枯树枝、树叶等可燃物,达到隔离可燃物的目的
B. 用大量沙子灭火,达到隔绝空气的目的
C. 紧急疏散火灾周围地区的人群及贵重物品,达到减少损失的目的
D. 飞机播撒干冰,达到降低可燃物着火点的目的
【答案】D
【解析】
【分析】
根据灭火的原理:(1)清除可燃物或使可燃物与其他物品隔离,(2)隔绝氧气或空气,(3)
�
使温度降到可燃物的着火点以下解答。
【详解】A、砍掉或清理大火面前的干枯树枝、树叶等可燃物,可以使可燃物与火源隔离,
从而达到灭火的目的,正确;
B、用大量沙子覆盖灭火,达到隔绝空气的目的,正确;
C、森林火灾时紧急疏散火灾周围地区的人群及贵重物品,达到减少损失的目的,正确;
D、可燃物的着火点不能降低,故错误。故选 D。
3. 有关碳及其化合物说法中错误的是(
)
A. 金刚石和石墨物理性质有很大差异,是因为由不同的原子构成
B. 活性炭包可放在冰箱中除异味
C. CO2 会造成温室效应,CO 易与血液中的血红蛋白结合引起中毒
D. 工业上利用大理石生产生石灰和二氧化碳
【答案】A
【解析】
【分析】
【详解】A、金刚石和石墨物理性质有很大差异,是因为碳原子的排列方式不同,故选项 A
说法不正确;
B、活性炭具有吸附性,能吸附色素和异味,所以活性炭包可放在冰箱中除异味,故选项 B
说法正确;
C、CO2 排放过多会造成温室效应,CO 有毒,易与血液中的血红蛋白结合引起中毒,故选项 C
说法正确;
D、大理石在高温条件下分解生成氧化钙和二氧化碳,所以工业上利用大理石生产生石灰和
二氧化碳,故选项 D 说法正确。
故选 A。
【点睛】本题难度不大,掌握二氧化碳和一氧化碳的化学性质、物理性质、用途等是正确解
答本题的关键。
4. 实验方案设计合理的是(
)
选项 目的
方案
A
除去木炭粉中的少量氧化铜
在空气中充分灼烧
�
B
C
D
鉴别二氧化碳和一氧化碳
通过氢氧化钙溶液
除去二氧化碳中的一氧化碳
点燃
鉴别氢气和甲烷
点燃,火焰上罩一个干冷的烧杯
B. B
C. C
D. D
A. A
【答案】B
【解析】
【分析】
【详解】A、木炭与氧气充分反应生成二氧化碳,所以将混合物在空气中充分灼烧,会把木
炭除掉,不符合除杂的原则,故 A 实验设计不合理;
B、二氧化碳通入氢氧化钙溶液反应,溶液变浑浊,一氧化碳通入氢氧化钙溶液中无明显现
象,现象不同,可以鉴别,故 B 实验设计合理;
C、二氧化碳不能支持燃烧,所以在大量的二氧化碳中一氧化碳是不能燃烧的,所以难以通
过此方法除去一氧化碳,故 C 实验设计不合理;
D、甲烷完全燃烧生成二氧化碳和水,氢气燃烧水,所以点燃后,在火焰上方各罩一个干冷
的烧杯,烧杯内壁都出现水雾,现象相同,不能鉴别,故 D 实验设计不合理。
故选 B。
5. 如下图所示,先在 a、c 两支相同的大试管中充满红棕色的 NO2 气体,然后分别向 a、c
试管中加入质量相等的足量的石墨和活性炭,迅速塞上带导管的胶塞,经过一段时间后,打
开弹簧夹,所观察到的现象(
)
A. a、c 两试管都无明显变化
B. a、c 两试管的颜色都消失,水往两试管流
C. a 试管中的颜色消失,水往 a 试管流,c 试管无明显变化
D. c 试管中的颜色消失,水往 c 试管流,a 试管无明显变化
�
【答案】D
【解析】
【详解】因为活性炭具有较强的吸附性,而石墨没有吸附性,所以 c 试管中的颜色消失,当
活性炭吸附 NO2 后,试管内压强减小,打开弹簧夹,大气压将水压入 c 试管,而 a 无明显变
化。
故选:D。
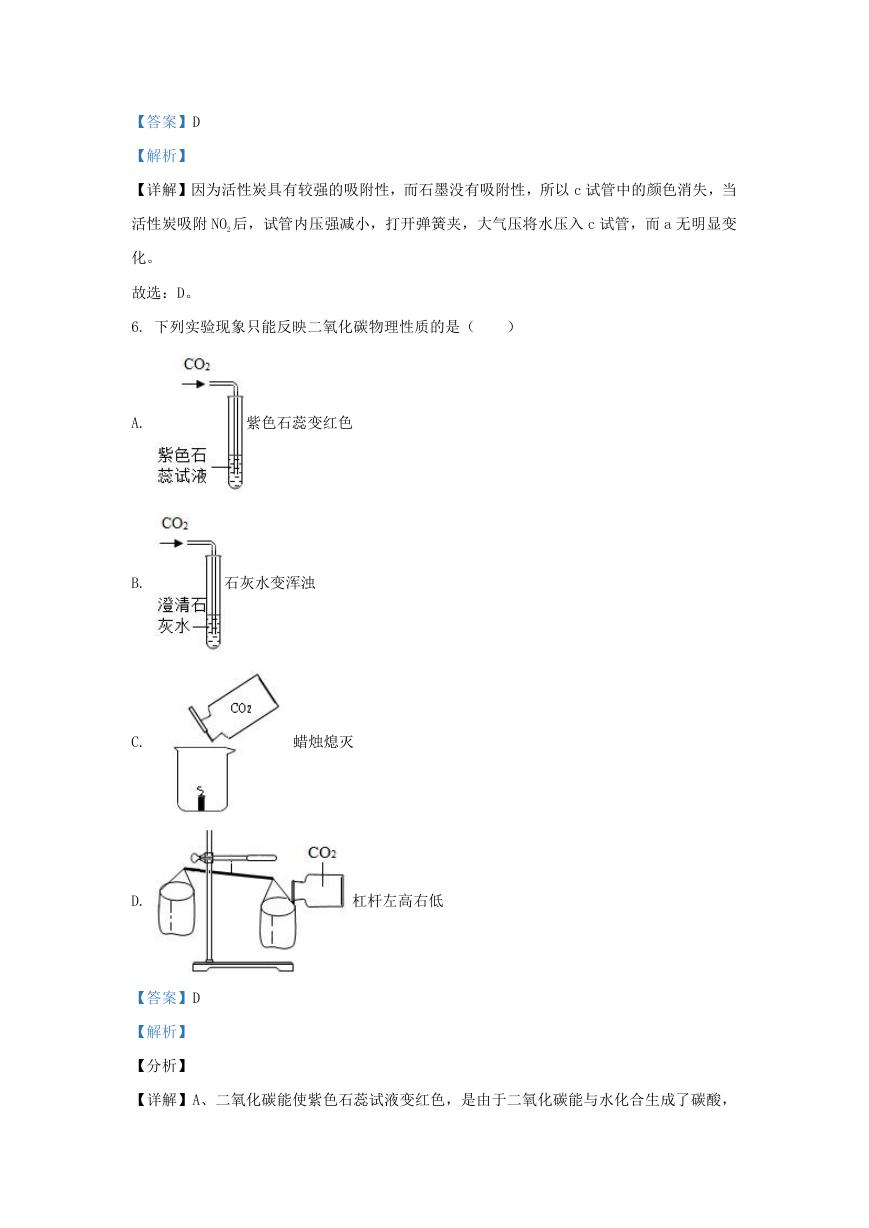
6. 下列实验现象只能反映二氧化碳物理性质的是(
)
A.
紫色石蕊变红色
B.
石灰水变浑浊
蜡烛熄灭
杠杆左高右低
C.
D.
【答案】D
【解析】
【分析】
【详解】A、二氧化碳能使紫色石蕊试液变红色,是由于二氧化碳能与水化合生成了碳酸,
�
反映二氧化碳的化学性质,故 A 不符合题意;
B、二氧化碳能使石灰水变浑浊,是由于二氧化碳能与氢氧化钙反应生成了碳酸钙沉淀和水。
反映二氧化碳的化学性质,故 B 不符合题意;
C、蜡烛熄灭,是由于二氧化碳不燃烧不支持燃烧,密度比空气大,既反映二氧化碳的化学
性质又反映了二氧化碳的物理性质,故 C 不符合题意;
D、杠杆左高右低,是由于二氧化碳的密度比空气大,只反映了二氧化碳的物理性质,故 D
符合题意。
故选:D。
7. 按如图进行实验分析或结论正确的是(
)
A. 导管口刚有气泡冒出说明反应开始
B. 给酒精灯加网罩,目的是使火焰集中并提高温度
C. 实验结束应立即倒出粉末
D. 固体减少的质量一定等于生成二氧化碳质量
【答案】B
【解析】
【详解】A、导管口刚有气泡冒出不能说明反应开始,因为刚开始排出的是试管内的空气,
故选项说法错误。
B、给酒精灯加网罩,目的是使火焰集中并提高温度,故选项说法正确。
C、实验结束不能立即倒出粉末,因为铜在温度高的条件下能与氧气反应生成氧化铜,故选
项说法错误。
D、根据质量守恒定律,固体减少的质量等于氧化铜中失去的氧元素的质量和参加反应的碳
元素的质量的总和,反应中可能生成一氧化碳,所以固体减少的质量不一定等于生成二氧化
碳质量,故选项说法错误。
故选:B。
�
8. 关于二氧化碳的说法错误的是(
)
A. 生活中不可用大量的澄清石灰水来吸收二氧化碳,缓解温室效应
B. 大气中的二氧化碳是植物进行光合作用必需的物质
C. 实验室用大理石与稀硫酸反应制取二氧化碳
D. 将二氧化碳气体通入紫色石蕊试液中,溶液变为红色
【答案】C
【解析】
【分析】
【详解】A、氢氧化钙在水中的溶解度较小,吸收二氧化碳的能力有限,则生活中不可用大
量的澄清石灰水来吸收二氧化碳,缓解温室效应,故 A 正确;
B、植物利用二氧化碳和水在光的作用下生成糖类和氧气,则大气中的二氧化碳是植物进行
光合作用必需的物质,故 B 正确;
C、碳酸钙和稀硫酸反应生成微溶的硫酸钙,覆盖在大理石表面阻止反应的进行,则不能用
大理石与稀硫酸反应制取二氧化碳,故 C 不正确;
D、将二氧化碳气体通入紫色石蕊试液中,二氧化碳和水反应生成碳酸,显酸性,使紫色石
蕊试液变红色,则溶液变为红色,故 D 正确。故选 C。
9. 为了验证二氧化碳与水反应生成碳酸,小赵做了以下实验,不合理的是( )
B. 步骤②
C. 步骤③
D. 步骤④
A. 步骤①
【答案】C
【解析】
【分析】
【详解】二氧化碳与水生成碳酸,能使紫色石蕊变红,不能使无色酚酞变色;加热时碳酸分
解,石蕊试液由红色变成紫色,所以实验中不合理的步骤是步骤 3,故选 C。
10. 实验室制取某些气体的装置如下图所示。下列说法正确的是
�
A. 装置①和③组合可以用来制取氢气
B. 装置②和③组合可以用来制取氧气
C. 装置②和⑤组合可以用来制取二氧化碳
D. 装置②可以控制反应的随时发生随时停止
【答案】B
【解析】
【分析】
【详解】A、实验室采取锌和稀硫酸制取氢气,属于固液不加热型,发生装置选①,由于氢
气密度比空气小,需要用向下排空气法收集,收集装置不能选③,故 A 选项错误;
B、实验室制取氧气可以采取过氧化氢分解法,用二氧化锰做催化剂,属于固液不加热型,
发生装置选②,由于氧气密度比空气大,可以选择向上排空气法收集,收集装置选③,故 B
选项正确;
C、实验室采用碳酸钙与稀盐酸制取二氧化碳,属于固液不加热型,因此发生装置选②,由
于二氧化碳溶于水,因此收集装置不能选择⑤,故 C 选项错误;
D、装置②中固体与液体接触后不能进行分离,不能控制反应的随时发生随时停止,故 D 选
项错误。
故本题选 B。
11. 图中表示一定量的木炭和氧化铜固体混合物受热过程中,某变量 随加热时间的变化趋
势,其中纵坐标 表示(
)
�
A. 固体的质量
B. 固体中氧化铜的质量 C. 二氧化碳的质量
D. 固体中
铜元素的质量分数
【答案】D
【解析】
【分析】
【详解】根据图像可知,纵坐标表示的物质或元素开始不变,再逐渐增加,反应停止后不变,
结合各物质即元素在反应中的变化情况来分析;通过分析 C+2CuO
2Cu+CO2↑可知:
高温
A、氧化铜和碳反应生成铜和二氧化碳,固体质量逐渐减小,错误;
B、氧化铜的质量逐渐减小到零,错误;
C、二氧化碳的质量应该从零开始不断增加,错误;
D、铜元素质量不变,固体质量逐渐减小,所以固体中铜元素的质量分数逐渐增加,然后不
变,故 D 正确。
故选 D。
12. 下列反应属于氧化还原反应的是(
)
高温
A. C+H2O
CO+H2
高温
C. CaCO3
CaO+CO2↑
【答案】A
【解析】
B. CaCO3+2HCl=CaCl2+H2O+CO2↑
D. H2O+CO2=H2CO3
【详解】A、有单质参加,和有单质生成,一定有化合价变化,属于氧化还原反应,正确;
B、反应前后钙元素的化合价都为+2,氢元素为+1,氧元素为-2,碳元素为+4,没有化合价
的变化,不属于氧化还原反应,错误;
�















 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc