2002 年浙江普通高中会考化学真题及答案
考生须知:
1.全卷分试卷Ⅰ、Ⅱ和答卷Ⅰ、Ⅱ,试卷共 6 页,有 4 大题,40 小题,满分为 100 分。
考试时间 90 分钟。
2.本卷答案必须做在答卷Ⅰ、Ⅱ的相应位置上,做在试卷上无效。
3.请用钢笔或蓝、黑色圆珠笔将姓名、准考证号分别填写在答卷Ⅰ、Ⅱ的相应位置上,
并沿裁剪线将答卷Ⅱ裁下。
4.本卷可能用到的相对原子质量数据:
H-1,C-12,N-14,O-16, Mg-24,Al-27, Fe-56。
试
卷
Ⅰ
请用铅笔将答卷Ⅰ上的准考证号和学科名称所对应的括号或方框涂黑;如果你选定本学科
为“考查”科目,请将“考查”对应的方框涂黑(此处不涂黑即表示你选“考试”);分流教
育学校的考生还需将“分流”对应的方框内涂黑(非分流教育学校的考生此处不得涂黑),然
后再开始答题。
一、 选择题(本题有 32 小题,每小题 2 分,共 64 分。每小题只有 1 个选项符合题意,
不选、多选、错选均不给分。)
1.下列物质在常温下呈气态的是
A.乙烷
B. 乙醇
C. 苯
D. 四氯化碳
2. 通常状况下,不跟..水反应的物质是
A. CO2
B. NO2
C. Na2O
D. SiO2
3. 常温下,能被浓硝酸钝化的金属是
A. Mg
B. Fe
C. Cu
D. Ag
4. 下列物质中,可以跟甲烷发生化学反应的是
A. 氯气
B. 稀盐酸
C. 烧碱溶液
D. 高锰酸钾溶液
5. 氧化镁的主要用途是
A. 制轻金属
B. 制耐火材料
C. 制导线
D. 制合金
6. 能使 FeCl3 溶液呈紫色的是
A. 乙醇
B. 苯酚
C. 乙醛
D. 乙酸
7. 实验室用 Al2(SO4)3 制取 Al(OH)3,最合适的试剂是
�
A. NaOH
B. H2SO4
C. NH3•H2O
D. KOH
8. 与乙烷互为同系物的是
A. C6H6
B. C6H10
C. C6H12
D. C6H14
9. 下列物质不能..与镁反应的是
A. Cl2
B. Ar
C. N2
D. CO2
10. 下列物质属于纯净物的是
A. 铁红
B. 玻璃
C. 石油
D. 煤
11. 既有氧化性,又有还原性的粒子是
A. Fe
B. Fe2+
C. Fe3+
D. Cu2+
12. 下列各类烃中,完全燃烧后生成的 H2O 和 CO2 的物质的量之比为 1∶1 的是
A. 烷烃
B. 烯烃
C. 炔烃
D. 二烯烃
13. 实验室进行下列实验时,必须在反应液中加入碎瓷片以防止暴沸的是
A. 制溴苯
B. 制硝基苯
C. 制乙烯
D. 制酚醛树脂
14. 下列关于苯酚的描述错误..的是
A. 无色晶体,具有特殊气味
B. 常温下易溶于水
C. 暴露在空气中呈粉红色
D. 有毒,有强烈的腐蚀性
15. 在标准状况时密度为 2.5 g/L 的是
A. C4H8
B. C2H4
C. C2H2
D. CH4
16. 过量的铁粉与稀硫酸反应后,溶液中存在较多的阳离子是
A. Fe3+
B. Fe2+
C. H+
D. Fe3+ 和 Fe2+
17. 下列哪种物质,不是..炼铁的主要原料
A. 铁矿石
B. 焦炭
C. 石灰石
D. 石英
18. 下列各组物质互为同分异构体的是
A. 苯酚和苯甲醇
B. 2-甲基丙烯和 1,3-丁二烯
C. 乙苯和邻二甲苯
D. 2,2-二甲基丙烷和新戊烷
19. 有机物甲能发生银镜反应,甲经催化加氢还原为乙,1mol 乙与足量钠反应产生氢气
22.4L(标准状况下),据此推断乙可能是
A. CH3—CH2—OH
B. CH3—CH2—CH2—OH
C. HO—CH2—CH2—CH2—OH
D.
�
20. 下列关于碳和硅的叙述不正确...的是
A. 地壳中硅元素的含量比碳元素高
B. 自然界中碳元素的化合物种类比硅元素多
C. 金刚石和晶体硅都是原子晶体
D. 碳和硅的最高价氧化物都是分子晶体
21. 通常用于检验酒精中是否含有水的试剂是
A. 生石灰
B. 金属钠
C. 硫酸铜晶体
D. 无水硫酸铜
22. 下列各组混合气体中,含碳量比乙烯高的是
A. 甲烷和丙烯
B. 乙烷和乙烯
C. 乙烯和丙烯
D. 乙炔和丙烯
23. 人们生活中使用的化纤地毯、三合板、油漆等化工产品,会释放出某种污染空气的气
体,该气体是
A. 甲醛
B. 二氧化硫
C. 甲烷
D. 乙醇
24. 某有机物结构为:
CH2=CH—
,它可能具有的性质是
—OH
O
O—C—CH3
①能使 KMnO4 酸性溶液褪色
②能与 NaOH 溶液反应
③能发生聚合反应
④能与 Ag(NH3)2OH 溶液发生银镜反应
A.只有①②
B. 只有②③
C. 只有①②③
D. ①②③④
25. 目前没有列入....“城市空气质量日报”报道项目中的是
A.二氧化硫
B. 氮氧化物
C. 二氧化碳
D. 悬浮颗粒
26. 烧烤肉类时会产生强烈的刺激性致癌物质 3, 4-苯并芘,结构简式为:
。
其分子式为
A. C20H12
B. C20H34
C. C22H12
D. C30H36
27. 做乙醛被 Cu(OH)2 氧化实验时,有以下步骤:①加入 0.5 mL 乙醛溶液;②加入 2% 硫
酸铜溶液 4 到 5 滴;③加入 10% NaOH 溶液 2 mL;④加热至沸腾。其正确的操作顺序是
A. ①②③④
B. ③②①④
C. ②③①④
D. ①③②④
28. 下列化学方程式书写正确的是
A. 2Fe + 6HCl = 2FeCl3 +3H2↑
B. FeO+2HNO3 = Fe(NO3)2 + H2O
�
C. Al2O3+2NaOH = 2NaAlO2 + H2O
D. AlCl3 + 4NH3•H2O = NH4AlO2 +3NH4Cl+2H2O
29. 在无色透明的酸性溶液中,能大量共存的一组离子是
A. Mg2+、Na+、Cl-、NO3
-
B. Ba2+、Al3+、SO4
2- 、NO3
-
C. K+、OH-、Fe3+、SO4
2-
D. K+、Na+、SiO3
2-、Br-
30. 合成结构为
的高聚物,其单体为
A.
C.
B.
CH2 = C—CH=C—CH2—CH3
CH3
CH3
D.
31. 甲醛、乙醛、丙醛组成的混合物中,氢元素的质量分数为 9%,则氧元素的质量分数为
A. 16%
B. 37%
C. 54%
D. 无法确定
32. C8H18 在一定条件下受热裂化可生成 CH4、C2H4、C2H6、C3H6、C4H8 等 5 种混合气体,
则混合气体的平均相对分子质量为
A. 22.8
B. 38
C.57
D.114
试
卷
Ⅱ
请将本卷的答案用钢笔或蓝、黑色圆珠笔写在答卷Ⅱ上。
二、填空题(本题有 4 小题,共 16 分。)
33.写出下列反应的化学方程式:
(1)红热的铁跟水蒸气反应
(2)乙醇跟氢溴酸混合加热
。
。
(3)氯化铁溶液跟氨水反应(写离子方程式)
。
34.某金属 A 及其化合物之间有如下的转化关系:
Cl2
Δ
盐酸
A
B
A
D
NaOH 溶液
C(红褐色)
NaOH 溶液
置于空气中
E(白色)
�
请写出 A、B、C 的化学式:A
、B
、C
。
35.已知羟基与烯键碳原子相连接时,易发生如下变化:
现有下列转化关系:
(C4H6O2)n
加聚
稀硫酸
A
B
新制 Cu(OH)2
C
写出 A 的结构简式
。
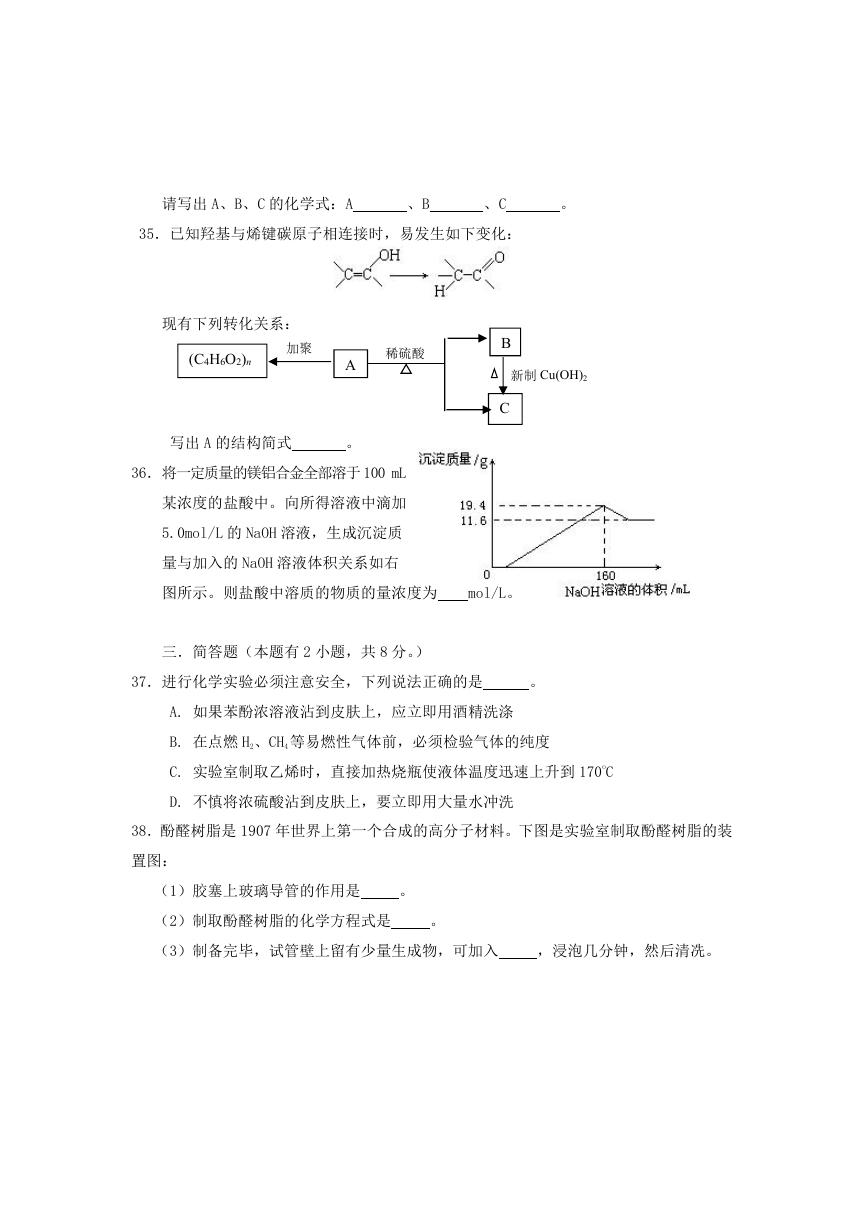
36.将一定质量的镁铝合金全部溶于 100 mL
某浓度的盐酸中。向所得溶液中滴加
5.0mol/L 的 NaOH 溶液,生成沉淀质
量与加入的 NaOH 溶液体积关系如右
图所示。则盐酸中溶质的物质的量浓度为
mol/L。
三.简答题(本题有 2 小题,共 8 分。)
37.进行化学实验必须注意安全,下列说法正确的是
。
A. 如果苯酚浓溶液沾到皮肤上,应立即用酒精洗涤
B. 在点燃 H2、CH4 等易燃性气体前,必须检验气体的纯度
C. 实验室制取乙烯时,直接加热烧瓶使液体温度迅速上升到 170oC
D. 不慎将浓硫酸沾到皮肤上,要立即用大量水冲洗
38.酚醛树脂是 1907 年世界上第一个合成的高分子材料。下图是实验室制取酚醛树脂的装
置图:
(1)胶塞上玻璃导管的作用是
。
(2)制取酚醛树脂的化学方程式是
。
(3)制备完毕,试管壁上留有少量生成物,可加入
,浸泡几分钟,然后清冼。
�
四.计算题(本题有 2 小题,共 12 分。)
39.某液态醇的蒸气密度是相同状况下的氢气的 23 倍,4.6 g 这种醇完全燃烧时生成
8.8 g CO2 和 5.4 g H2O。通过计算写出这种醇的结构简式。
40.氧化铁和铁粉的混合物 19.2 g,恰好溶于 150 mL 某浓度的稀硫酸,并收集到 3.36 L
(标准状况下)的气体。向反应后的溶液中滴加硫氰化钾溶液,不显血红色。求:
(1) 原混合物中铁粉的质量。
(2) 稀硫酸中溶质的物质的量浓度。
2002 年浙江普通高中会考化 学 参 考 答 案 和 评 分 标 准
说明:本卷最小采分点为 1 分,没有 0.5 分。
一、选择题(每小题 2 分,共 64 分,不选、多选、错选均不给分。)
12
题号 1
答案 A
B
28
题号 17
答案 D
C
6
B
22
D
7
C
23
A
8
D
24
C
2
D
18
C
3
B
19
C
9
B
25
C
10
A
26
A
4
A
20
D
5
B
21
D
11
B
27
B
13
C
29
A
14
B
30
D
15
A
31
B
16
B
32
B
二、填空题(本大题共 16 分。)
题 号
参
考
答
案
分数
评分意见
高温
(1) 3Fe + 4H2O ===
Fe3O4 +4H2↑
(2) CH3CH2OH + HBr C2H5Br + H2O
(3) Fe3+ + 3NH3•H2O = Fe(OH)3↓+3NH4
+
A. Fe
B. FeCl3
C. Fe(OH)3
CH3COOCH=CH2
33
34
35
化学符 号写
错不给分,条件错或
未配平给 1 分。
⑶中写化学方程
式不给分。
每空 2 分
2
2
2
6
2
�
36
8
2
三、简答题(本大题共 8 分)
题号
参
考
答
案
分 数
评分意见
37
A、B
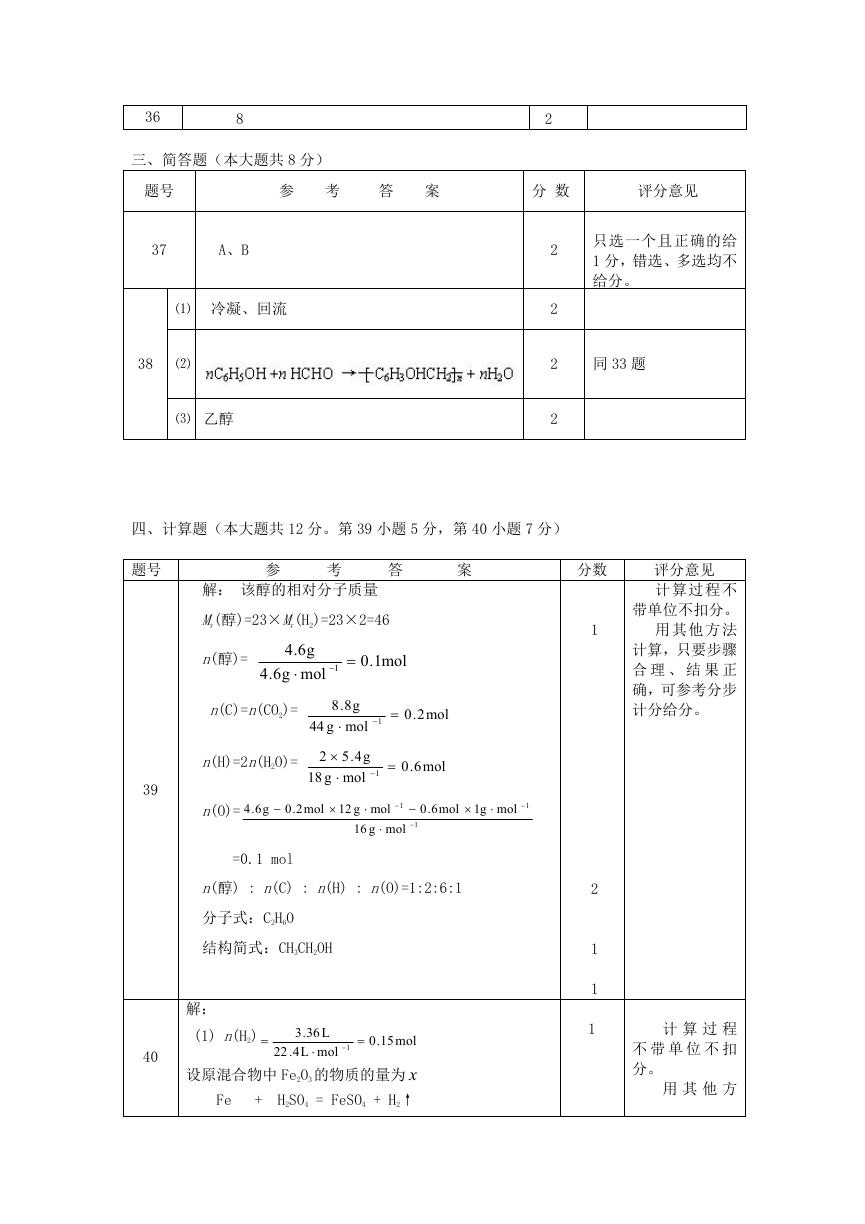
⑴ 冷凝、回流
38
⑵
⑶ 乙醇
只选一个且正确的给
1 分,错选、多选均不
给分。
同 33 题
2
2
2
2
四、计算题(本大题共 12 分。第 39 小题 5 分,第 40 小题 7 分)
题号
参
考
答
案
分数
解: 该醇的相对分子质量
Mr(醇)=23×Mr(H2)=23×2=46
n(醇)=
g6.4
mol
g6.4
1
1.0
mol
n(C)=n(CO2)=
n(H)=2n(H2O)=
g8.8
mol
g44
2
g18
g4.5
mol
1
2.0
mol
1
6.0
mol
n(O)=
g6.4
2.0
mol
=0.1 mol
g12
g16
mol
1
mol
6.0
mol
g1
mol
1
1
n(醇) : n(C) : n(H) : n(O)=1:2:6:1
分子式:C2H6O
结构简式:CH3CH2OH
解:
(1) n(H2)
L36.3
mol
L4.22
1
15.0
mol
设原混合物中 Fe2O3 的物质的量为 x
H2SO4 = FeSO4 + H2↑
Fe
+
39
40
1
2
1
1
1
评分意见
计 算过 程 不
带单位不扣分。
用 其他 方 法
计算,只要步骤
合 理 、 结 果 正
确,可参考分步
计分给分。
计 算 过 程
不 带 单 位 不 扣
分。
用 其 他 方
�
法计算,只要步
骤合理、结果正
确,可参考分步
计分给分。
0.15 mol
0.15 mol
0.15 mol
3H2SO4 = Fe2(SO4)3 + 3H2O
Fe2O3 +
3 x
x
Fe2(SO4)3 + Fe =
x
( x +0.15 mol)×56 g/mol + x ×160 g/mol =19.2 g
x
3FeSO4
x
x =0.05 mol
m(Fe)=(0.15 mol+0.05 mol) ×56 g/mol=11.2 g
(2)c(H2SO4)=
05.03
15.0
mol
L15.0
mol
=2.0 mol/L
2
2
2
�














 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc