2006 年广东省广州市中考化学真题及答案
本试卷分为选择题和非选择题两部分;第一部分 1 至 4 页,第二部分 5 至 8 页,共 8 页,满
分 100 分。考试时间 80 分钟。
注意事项:
1.答卷前,考生务必在答题卡第 1 面和第 3 面上用黑色字迹的钢笔或签字笔填写自己的考生
号、姓名;同时填写考场试室号、座位号,再用 2B 铅笔把对应这两个号码的标号涂黑。
2.选择题每小题选出答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号;不能答在试卷上。
3.非选择题必须用黑色字迹钢笔或签字笔作答,答案必须写在答题卡各题目指定区域内的相
应位置上;如需改动,先划掉原来的答案,然后再写上新的答案,改动的答案也不能超出指
定的区域;不准使用铅笔、圆珠笔和涂改液。不按以上要求作答的答案无效。
4.考生必须保持答题卡的整洁,考试结束时,将本试卷和答题卡一并交回。
5.全卷共三大题 29 小题,请考生检查题数。
可能用到的相对原子质量:
H: l
O: 6
Na: 23
Mg: 24
Al: 27
Ca: 40
第一部分 选择题 (共 40 分)
一、选择题 (本题包括 20 小题,每小题 2 分,共 40 分)
注意,每道选择题有四个选项,其中只有一项符合题意。请用铅笔在答题卡上作答。选
错、不选、多选或涂改不清的,均不给分。
1.下列变化属于化学变化的是
A.夜幕降临,珠江两岸霓虹灯通电后发出美丽的亮光
B.“侯氏制碱法”用空气、水、食盐生产纯碱和化肥
C.青铜受热融化后浇铸成各种形状的工艺品
D.自来水通过蒸馏变成可饮用的瓶装蒸馏水
2.地壳里含量最多的金属元素是
A.氧
B.硅
C.铝
D.铁
3.化石燃料是不可再生的能源。下列不属于化石燃料的是
A.天然气
B.煤
C.石油
D.乙醇
4.下列实验操作可能会引发事故的是
�
A.稀释浓硫酸时,将水沿烧杯壁慢慢倒入浓硫酸中,并用玻璃棒不断搅拌
B.用镊子取出白磷在水中切割
C.做一氧化碳还原氧化铜的实验时,先通-氧化碳再加热
D.用灯帽盖灭酒精灯火焰
5.我省某著名风景区附近是大型的陶瓷生产基地,工厂排放的气体使景区内酸雨频频。风
景区内受酸雨影响最小的是
A.山上的树木
B.小桥的铁栏杆
C.路灯的玻璃罩
D.大理石雕像
6.下列结构示意图所表示的粒子属于稀有气体元素的是
7.人类每年从自然界中提取大量的金属铁,下列关于铁的说法正确的是
A.炼铁的过程是把单质铁变成氧化铁
B.钢是很纯的铁
C.生铁是含少量碳的铁合金
D.被腐蚀的铁制品属于不可回收垃圾
8.下列反应属于化合反应的是
A.锌片投入稀硫酸中
B.高温锻烧石灰石
C.甲烷在空气中燃烧
D.在氧气中点燃铝箔
9.按酸、碱、盐、氧化物的分类,下列各组物质属于同一类别的是
A.氯化钠和碳酸钙
B.氢氧化钠和硝酸钾
C.氧化镁和氯化氢
D.氧化钙和氢氧化钙
10.有机合成材料的出现是材料发展史上的一次重大突破。下列物质属于有机合成材料的是
A.棉花
B.蛋白质
C.维生素
D.塑料
11.有一种气体,可能是 H2 或 CO,下列方法能够鉴别它们的是
A.观察气体是否无色
B.闻气味是否具有刺激性
�
C.通入氧化铜中,加热,观察黑色粉末是否变红色
D.点燃,在火焰上罩一个内壁附着有澄清石灰水的烧杯,观察石灰水是否变浑浊
12.下列液体能够导电的是
A.澄清石灰水
B.蒸馏水
C.蔗糖水
D.乙醇
13.下列化学方程式朽写工确的是
A.氧化汞加热分解:
HgO
Hg+O2↑
B.铁花氧气中燃烧:
3Fe+2O2
Fe304
C.铝片投入稀硫酸中: Al+H2SO4=AlSO4+H2↑
D.碳在氧气中燃烧:
C+O2= CO2
14.下列物品需采取防锈措施的是
A.铁制防盗网
B.不锈钢菜刀
C.铝合金窗
D.金戒指
15。只用一种试剂就能把氢氧化钠溶液、稀盐酸和澄清石灰水鉴别开来,这种试剂是
A.氯化钡溶液
C.酚酞溶液
B.碳酸钠溶液
D.石蕊溶液
16.我国南方一些地区,农民有时会向农出撒些熟石灰,以调节土壤的 pH。这些地区土壤
的 pH 可能是
A. =7
C. <7
B.>7
D. 无法确定
17.对某无色溶液进行下列实验,根据实验现象得出的结论中,不正确...的是
A.滴入紫色石蕊溶液,颜色变红,则该溶液显酸性
B.滴入酚酞溶液,溶液保持无色,则该溶液显酸性
C.加入 Mg 粉,有气泡产生,则该溶液显酸性
D.加入 CaCO3 固体,有气泡产生,则该溶液显酸性
18.甲、乙、丙、丁四瓶溶液分别是 K2CO3、Ba(NO3)2、H2S04、K2S04 中的一种,其中
甲分别能与乙、丙、丁发生反应,甲是
A.K2SO4
C.Ba(NO3)2
B.H2S04
D.K2CO3
19.有 X、Y、Z 三种金属,把 Y 投入 X(N03)2 溶液中,Y 表面有 X 析出, 把 X 投入 Z(N03)2
�
溶液中,X 表面有 Z 析出。X、Y、Z 三种金属的活动性由强到弱的顺序是
A.Z>Y>X
C.X>Y>Z
B.Y>X>Z
D.X>Z.Y
20.质量相同的 Na、Mg、AI、Ca 四种金属,含原子数最少的是
A.Na
C.Al
B.Mg
D.Ca
第二部分 非选择题 (共 60 分)
二、本题包括 5 小题,共 31 分。
21,(6 分)右图是部分物质的溶解度曲线,根据
该曲线图回答问题:
(1)下列说法中错误的是
(填 A、
B、C 符号)
A.硝酸钾的溶解度大于氯化钠的溶解度
B.0°C 时物质的溶解度都为 0g
C.图中所列物质的溶解度都随温度的升高
而增大
(2)10°C 时,100 g 水中溶解
g 硝酸钠才能
形成饱和溶液,该饱和溶液中溶质的质量分数是
(精确到 0·1%)。
22.(9 分)(1)用化学用语表示下列物质:
2 个氢原子
硫酸钠
,硝酸根离子
,铝离子
,氢氧化钾
(2)写出下列反应的化学方程式:
①电解水
②二氧化碳通入水中
23.(4 分)由 C、CuO、Fe 三种物质组成的混合物,放在试管中,如图所示高温加热。
当观祭到澄清石灰水变浑浊时,停止加热,密封冷却至室
温;然后往试管中加入稀硫酸,观察到有气泡冒出,且红
色物质明显增加。请根据这些信息,推断红色物质产生和
增加的可能的原因(用化学万程式表)
�
24.(6 分)X 和白色沉淀 I、II 都是含有镁元素的化合物,Z 是一种会使地球产生"温室
效应"的气休,A 是一种碱。它们的有关变化如下图所示 (该实验条件下,微溶物以
沉淀形式拙现):
(1)写出下列物质的化学式:
A 是
,B 是
白色沉淀 I 是
,Z 是
(2)X 跟 C 反应的化学方程式是
25.(6 分)A、B、C、D、E、F、G 都是初中化学中常见物质。其中 A 是酸,C 和 D 是
盐,E 和 F 是碱,它们相互可以发生如下变化:
①A+E→D+G
②2A+B→C+H2↑
③2E+C→F↓+2D
根据上述信息,回答:
(1)在化合物 C 中,元素 B 呈现的化合价是
含有 B 元素的化合物除了 C 外还
有
(填 A、B、C、D、E、F、G 等符号)。
(2)A 的化学式是
,G 的化学式是
。
(3)写出符合反应③的一个化学方程式
三、本题包括 4 小题,共 29 分。
26.(4 分)右图为过滤装置,写出下列仪器、用品的名称:
A
C
,B
D
27.(8 分)空气是一种宝贵的门然资源。空气中主要含
有了如图所示装置,测定空气里氧气的含量。
实验时先在集气瓶里加入少量水,做上记号。
�
用弹簧夹夹紧乳胶管。点燃燃烧匙内的红磷
后,立即仲入瓶中并把塞子塞紧。待红磷熄
灭后,发现红磷还有剩余,冷却,打开弹簧
夹,烧杯中的水倒流迸集气瓶中,液面上升到图中 A 位置。
(1)从上述实验现象可知:氧气约占空气总体积的 1/5,氮气约为 4/5。能够得到该结
论主要是运用了氮气的有关性质,请写出其中两点:
①
②
(2)红磷燃烧的化学方程式是
(3)实验室有一瓶 CO 和 CO2 的混合气体,某同学计划用上图装置(无燃烧匙)测定该混合气体
中 CO 和 CO2 的体积比。烧杯中应装入
(填化学式)溶液。
28.(9 分)实验室用分解高锰酸钾的方法制取氧气。
(1)用高锰酸钾制取氧气的化学方程式是
(2)现有下图所示的仪器,要制备并收集氧气,还需要补充的一种仪器是
(3)实验开始前如图所示检查装置气密性,如果
说明气密性良好。
(4)分解过氧化氢溶液也可制得氧气。过氧化氢的相对
分子质量是
,其中氢元索与氧元素的质量比是
。34g 过
氧化氢中氧元素的质量 m1=
g,34g 过氧化氢完全分解后,放出氧气的质量 m2=
g 。请回答,根据质量守恒定律,(m1-m2)能表示什么物质的质量?
29.(8 分)实验室一烧杯中盛有含少量 NaCl 的 CaCl2 溶液。请设计实验除去其中的 NaCl,
以得到纯净的 CaCl2 溶液。然后根据设计将相关内容填写在下面实验报吉的空格内(有
的空格可以不填)
�
实验步骤
实验现象
有关的化学方程式
1·向混合溶液中加入过量
溶液。
的
2·
3·
参考答案
1 B
2 C
3 D
4 A
5C
6A
7C
8D
9A
10 D
11 D
12 A
13 B
14 A
15B
16 C
17 B
18 C
19 B 20 D
21.(1)ABC (2) 80
44.4%
22. (1) 2H
-
NO3
Al3+
Na2SO4
KOH
(2)① 2H2O
2H2 ↑ +
O2↑粉 ② H2O + CO2 =H2CO3
23.
CuO+H2SO4 =CuSO4+H2O
CuSO4+Fe=FeSO4+Cu
24. (1)
NaOH
HCl
Mg(OH)2
MgCO3
(2) MgCl2+ Na2CO3 == MgCO3 +2NaCl
25. (1) +2
B、F
(2) HCl
H2Ol
(3) 2NaOH + MgCl2==Mg(OH)2+2NaC
26. 玻璃棒
滤纸
滤斗
烧杯
27. (1)氮气难溶于水;氮气不支持燃烧;氮气不能燃烧等
�
(2)4P+5O2
2P2O5(3)NaOH
28.(1)2KMnO4
K2MnO4+ MnO2 +O2↑
(2)酒精灯
(3)用手握住试管如果导气管口有气泡冒出,松开手后导气管中有一段水柱
(4)1:16
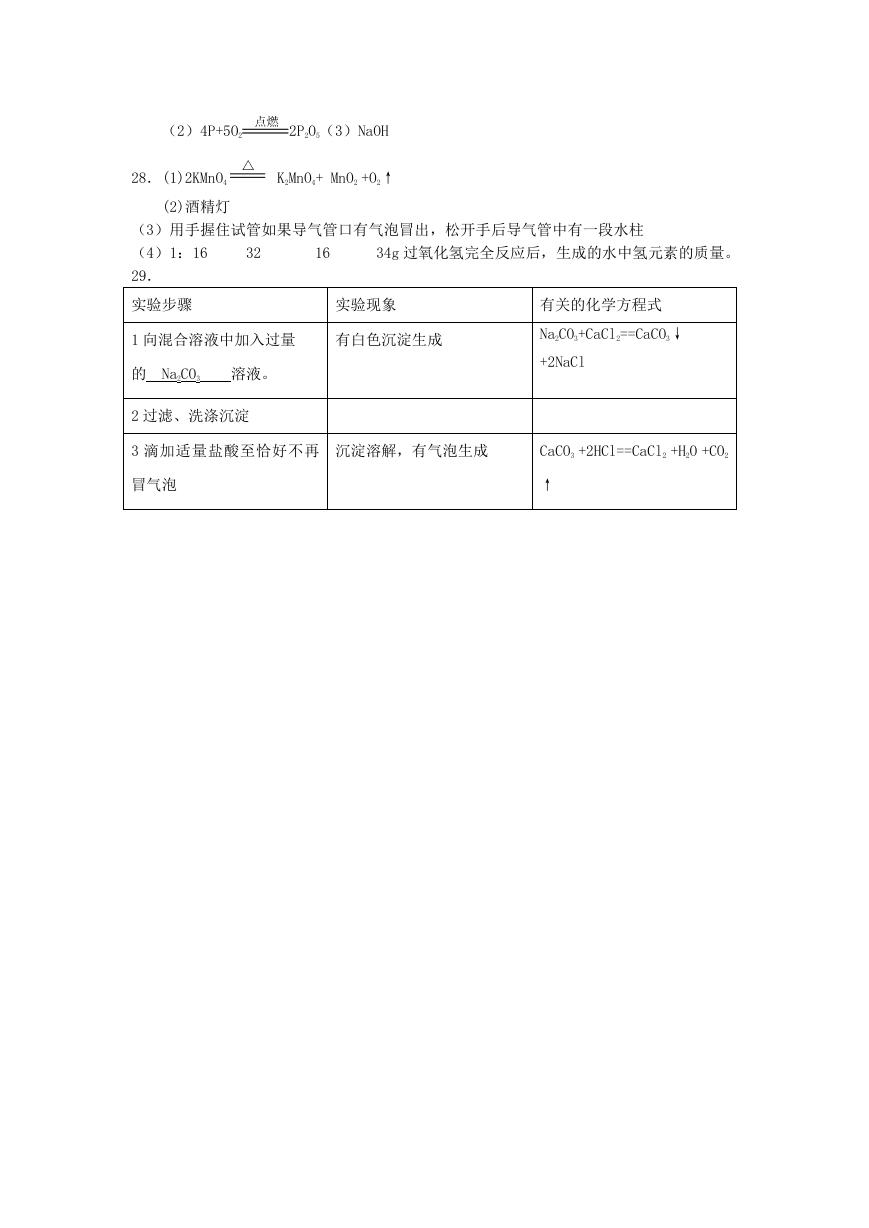
29.
32
16
34g 过氧化氢完全反应后,生成的水中氢元素的质量。
实验步骤
实验现象
有关的化学方程式
1 向混合溶液中加入过量
有白色沉淀生成
的 Na2CO3
溶液。
2 过滤、洗涤沉淀
Na2CO3+CaCl2==CaCO3↓
+2NaCl
3 滴加适量盐酸至恰好不再
沉淀溶解,有气泡生成
CaCO3 +2HCl==CaCl2 +H2O +CO2
冒气泡
↑
�















 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc