2009 年湖南普通高中会考化学真题及答案
本卷可能用到的相对原子质量数据:H1
C12
O16
S32
Cl35.5
Na23
Mg24
Fe56
一、选择题(本题包括 22 小题,每小题 2 分,共 44 分,每小题只有一个选项符合题意)
1.我国政府实施了《中国营养改善行动计划》。其中为改善营养性贫血,常在酱油中加入含某种元素的营
养强化剂,这种元素是
A.铜
B.铁
C.碘
D.锌
2.我们常在公共场所见到下列标志,其中属于回收标志的是
A
B
C
D
3.改革开放以来,人民生活水平不断提高,更加讲究合理膳食。下列饮食习惯科学的是
A.多吃肉,少吃蔬菜水果
B.多饮纯净水,少饮矿泉水
C.多食用含防腐剂的食品
D.注意饮食的合理搭配
4.胶体在人们日常生活中随处可见。下列分散系属于胶体的是
A.矿泉水
B.可乐饮料
C.豆浆
D.白酒
5.下列物质既属于钠盐,又属于硫酸盐的是
A.NaCl
B.Na2SO4
C.CuSO4
D.KNO3
6.下列气体遇到空气时,会发生颜色变化的是
A.N2
B.NH3
C.CO2
D.NO
7.在人们步入“3G”时代时,以光导纤维为基础的高速信息通道尤为重要。制造光导纤维的材料是
A.铜合金
B.橡胶
C.聚乙烯
D.二氧化硅
8.为维持生命活动,人需要不断地补充能量。下列物质中不能..为人补充能量的是
A.水
B.糖类
C.油脂
D.蛋白质
9.下列化学用语的书写,不正确...的是
A.葡萄糖的分子式:C6H12O6
B.氯气的电子式:Cl︰Cl
+16 2 8 6
C.乙醇的结构简式:CH3CH2OH
D.硫原子的结构示意图:
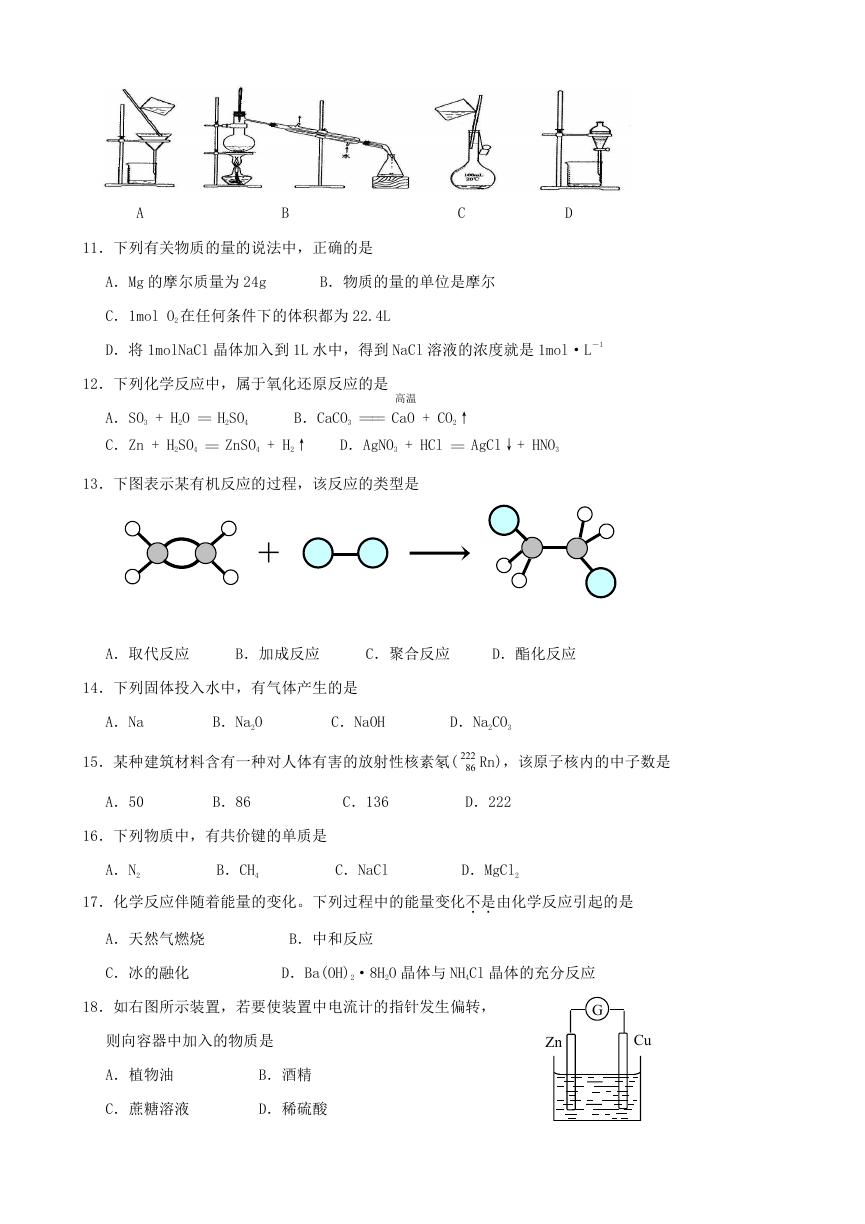
10.下列实验操作中,用于配制一定物质的量浓度的溶液的操作是
�
A
B
C
D
11.下列有关物质的量的说法中,正确的是
A.Mg 的摩尔质量为 24g
B.物质的量的单位是摩尔
C.1mol O2 在任何条件下的体积都为 22.4L
D.将 1molNaCl 晶体加入到 1L 水中,得到 NaCl 溶液的浓度就是 1mol·L―1
12.下列化学反应中,属于氧化还原反应的是
高温
A.SO3 + H2O == H2SO4
B.CaCO3 ==== CaO + CO2↑
C.Zn + H2SO4 == ZnSO4 + H2↑
D.AgNO3 + HCl == AgCl↓+ HNO3
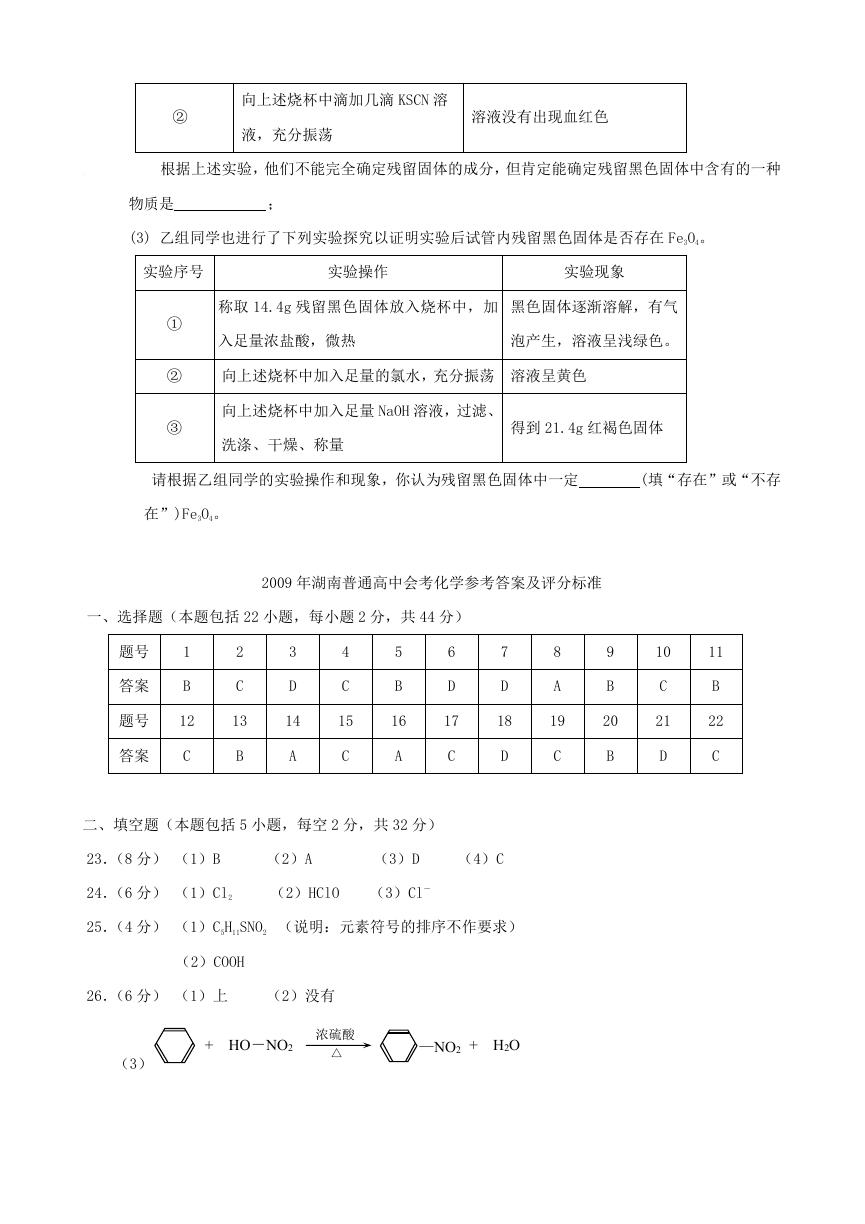
13.下图表示某有机反应的过程,该反应的类型是
+
A.取代反应
B.加成反应
C.聚合反应
D.酯化反应
14.下列固体投入水中,有气体产生的是
A.Na
B.Na2O
C.NaOH
D.Na2CO3
15.某种建筑材料含有一种对人体有害的放射性核素氡( 222
86 Rn),该原子核内的中子数是
A.50
B.86
C.136
D.222
16.下列物质中,有共价键的单质是
A.N2
B.CH4
C.NaCl
D.MgCl2
17.化学反应伴随着能量的变化。下列过程中的能量变化不是..由化学反应引起的是
A.天然气燃烧
B.中和反应
C.冰的融化
D.Ba(OH)2·8H2O 晶体与 NH4Cl 晶体的充分反应
18.如右图所示装置,若要使装置中电流计的指针发生偏转,
则向容器中加入的物质是
A.植物油
B.酒精
C.蔗糖溶液
D.稀硫酸
G
Zn
Cu
�
19.下列有关化学反应速率与化学反应限度的叙述中,错误..的是
A.化学反应速率是表示化学反应快慢的物理量
B.一般情况下,升高温度能加快化学反应速率
C.可逆反应达到化学反应限度时,反应就静止不动了
D.可逆反应达到化学反应限度时,正反应速率等于逆反应速率
20.下列离子方程式的书写正确的是
A.铁和稀硫酸反应
2Fe + 6H+ == 2Fe3+ + 3H2↑
B.向硫酸钠溶液中滴加氯化钡溶液
Ba2+ + SO4
2― == BaSO4↓
C.氯水加入到溴化钾溶液中
Br―+ Cl2 == Br2 + Cl―
D.碳酸钙溶于稀盐酸
CO3
2― + 2H+ == H2O + CO2↑
21.实验室可用如图所示装置来进行的实验是
A.制取氧气
B.制取氨气
C.碳酸氢钠受热分解
D.制取乙酸乙酯
22.将 13.7g Na2CO3 和 NaHCO3 的混合物充分加热,共收集
到标准状况下的气体 1.12L,则混合物中 Na2CO3 和 NaHCO3 的物质的量之比为
A.1︰1
B.2︰1
C.1︰2
D.3︰1
二、填空题(本题包括 5 小题,每空 2 分,共 32 分)
23.(8 分) 近年来,湖南省围绕“资源节约型和环境友好型”这一主题,积极谋求社会的和谐发展。请
你根据这一主题和题意,用下列选项的字母代号....进行填空。
A.二氧化硫
B.二氧化碳
C.开发新能源
D.沉淀法
(1) 造成温室效应和全球气候变暖的主要物质是
;
(2) 以煤炭为主的能源结构易导致酸雨的形成,形成这类酸雨的主要物质是
;
(3) 水 体 污 染 加 剧 了 水 资 源 的 短 缺 。 处 理 含 有 Hg2+ 等 重 金 属 离 子 的 废 水 常 用 的 一 种 方 法
是
;
(4) 石 油 是 一 种 重 要 能 源 , 人 类 正 面 临 着 石 油 短 缺 的 难 题 。 解 决 能 源 短 缺 问 题 的 一 种 方 法
是
。
24.(6 分) 新制氯水中含有 Cl2、H2O、HClO、H+、Cl―等粒子,根据下列性质选择恰当的粒子进行填空。
(1) 使新制氯水呈现浅黄绿色的物质是
;
(2) 能起杀菌消毒作用,光照易分解的弱酸是
(3) 能与硝酸银溶液作用生成白色沉淀的离子是
25.(4 分)青霉素是最重要的抗生素。青霉素在人体内经酸性
;
。
CH3
CH3―C―CH―COOH
SH
NH2
�
水解后,得到青霉素氨基酸,其结构简式如右图所示。
(1) 青霉素氨基酸的化学式为
(2) 分子中羧基的结构简式为“―
;
”。
26.(6 分) 苯是一种重要的化工原料,也是一种重要的溶剂。请回答下列问题:
(1) 把苯加入到盛有溴水的试管中,液体会出现分层现象,充分振荡、静置,出现橙红色液体的一层
在
层(填“上”或“下”);
(2) 把苯加入到盛有少量酸性高锰酸钾溶液的试管中,振荡后,酸性高锰酸钾溶液不褪色,说明苯分
子中
(填“有”或“没有”)碳碳双键;
(3) 在 浓 硫 酸 作 用 下 , 苯 在 50 ~ 60 ℃ 可 以 与 浓 硝 酸 反 应 生 成 硝 基 苯 , 反 应 的 化 学 方 程 式
. . . . .
为
。
27.(8 分)下表是元素周期表的一部分,其中每个数字序号代表一种短周期元素。
①
④
② ③
⑤
⑥
请按要求回答下列问题:
(1) 写出②的元素名称..
;
(2) 将④、⑤和⑥三种元素相比较,金属性最强的是
(3) 元素③的最高价氧化物对应的水化物的化学式...为
(填元素符号....);
;
(4) 元素③和元素⑥的氢化物均极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,相互接近时,可
看到大量的白烟,写出产生该现象的化学方程式
.....
。
三、推断题(本题每空 2 分,共 8 分)
28.(8 分) 已知 A 是由两种阳离子和一种阴离子组成的盐,且常用作净水剂,B 是一种常见的两性氢氧化
物。试根据下列转化关系回答有关问题:
白色沉淀 B
NH3·H2O
NaOH 溶液
HCl 溶液
溶液 D
溶液 E
A
溶
液
Ba(NO3)2 溶液
溶液 C
白色
沉淀 F
HNO3 沉淀 F
不溶解
焰色反应
紫色(透过蓝色钴玻璃观察)
�
(1) 试判断: B 为
,F 为
;
(2) 写出沉淀 B 与盐酸反应的离子方程式
.....
;
(3) 根据上述关系写出盐 A 的化学式...
。
四、实验题(本题包括 2 小题,每空 2 分,共 16 分)
29.(8 分) 为了达到下表中的实验要求,请从“供选择的化学试剂及方法”栏中,选择正确选项的字母..
代号..填入对应的空格中。
序号
实验要求
答案
供选择的化学试剂及方法
(1) 检验酒精中是否含有水
A.向试液中滴加酚酞试液
(2) 检验淀粉是否完全水解
B.向试液中加入无水 CuSO4
(3) 证明 NaHCO3 溶液呈碱性
C.加入饱和 Na2CO3 溶液,分液
(4) 除去乙酸乙酯中的少量乙酸
D.向试液中滴加 I2 溶液
30.(8 分)某研究性学习小组对还原铁粉与水蒸气的反应及产物进行科学探究,其反应原理为:3Fe + 4H2O(g)
Fe3O4 + 4H2
Fe3O4 + 8HCl(浓)
FeCl2 + 2FeCl3 + 4H2O
根据下图所示实验装置,同学们进行了还原铁粉与水蒸气反应的实验。学科网
学
网
试回答下列问题:
(1) 实验中使用肥皂液检验的产物是
;学科网
图中湿棉花的作用是
;
(2) 甲组同学为了进一步确定反应是否发生,对实验后试管内残留黑色固体的成分进行了下列实验
探究:学科网
实验序号
实验操作
实验现象
取少量残留黑色固体放入烧杯
黑色固体逐渐溶解,有气泡产
①
中,加入足量浓盐酸,微热
生,溶液呈浅绿色。
�
向上述烧杯中滴加几滴 KSCN 溶
②
液,充分振荡
溶液没有出现血红色
根据上述实验,他们不能完全确定残留固体的成分,但肯定能确定残留黑色固体中含有的一种
物质是
;
(3) 乙组同学也进行了下列实验探究以证明实验后试管内残留黑色固体是否存在 Fe3O4。
实验序号
实验操作
实验现象
①
②
③
称取 14.4g 残留黑色固体放入烧杯中,加
黑色固体逐渐溶解,有气
入足量浓盐酸,微热
泡产生,溶液呈浅绿色。
向上述烧杯中加入足量的氯水,充分振荡 溶液呈黄色
向上述烧杯中加入足量 NaOH 溶液,过滤、
得到 21.4g 红褐色固体
洗涤、干燥、称量
请根据乙组同学的实验操作和现象,你认为残留黑色固体中一定
(填“存在”或“不存
在”)Fe3O4。
2009 年湖南普通高中会考化学参考答案及评分标准
一、选择题(本题包括 22 小题,每小题 2 分,共 44 分)
题号
答案
1
B
题号 12
答案
C
2
C
13
B
3
D
14
A
4
C
15
C
5
B
16
A
6
D
17
C
7
D
18
D
8
A
19
C
9
B
20
B
10
C
21
D
11
B
22
C
二、填空题(本题包括 5 小题,每空 2 分,共 32 分)
23.(8 分) (1)B
(2)A
(3)D
(4)C
24.(6 分) (1)Cl2
(2)HClO
(3)Cl―
25.(4 分) (1)C5H11SNO2 (说明:元素符号的排序不作要求)
(2)COOH
26.(6 分) (1)上
(2)没有
+ HO-NO2
浓硫酸
△
—NO2
+ H2O
(3)
�
(说明:没有写反应条件的扣 1 分,其它合理答案也给分)
27.(8 分)(1)碳 (2)Na
(3)HNO3 (4)NH3 + HCl == NH4Cl
三、推断题(本题每空 2 分,共 8 分)
28.(1)氢氧化铝或 Al(OH)3
硫酸钡或 BaSO4
(2)Al(OH)3 + 3H+
== Al3+ +
3H2O
(3)KAl(SO4)2 或 K2SO4﹒Al2(SO4)3
(说明:带结晶水的化学式也给分)
四、实验题(本题包括 2 小题,每空 2 分,共 16 分)
29.(8 分)(1)B
(2)D (3)A (4)C
30.(8 分)(1)氢气或 H2 提供水蒸气
(2)铁或 Fe
(3)存在
�












 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc