2017 浙江省丽水市中考化学真题及答案
一、选择题(共 3 小题,第 1 小题 4 分,第 2、3 小题 3 分,满分 10 分)
1.(4 分)如图为某文化衫图案,你的美(Mg)偷走我的心(Zn)能发生,是由于镁的(
)
A.延展性好 B.导电性好
C.导热性好 D.金属活动性比锌强
2.(3 分)科技人员成功研制出一种新型催化剂,可将二氧化碳转化成液体燃料,反应的微
观示意图如下,有关该反应的说法正确的是(
)
A.该反应属于化合反应
B.反应前碳元素的化合价为+2 价
C.生成物的化学式可用 C2H2O 表示
D.参加反应的两物质的质量比为 1:1
3.(3 分)实验室有一瓶标签脱落的固体试剂,现分别取少量的该固体进行下列实验,根据
实验现象判断,该固体最可能是(
)
实验操作
取该固体于试管中,加水、振荡
实验现象
固体不溶解
取该固体于试管中,加盐酸、振荡
固体溶解,无气泡产生
一氧化碳通过炽热的该固体,称固体质量、检测
固体质量减轻,尾气中只检测到 CO 与
尾气
CO2
A.碱 B.盐 C.金属单质 D.金属氧化物
二、填空题(共 6 小题,每空 2 分,满分 42 分)
�
4.(4 分)家庭厨房就是一个科学小世界,其中包含着许多科学知识.
(1)大米、小麦为人体提供的主要营养素是
.
(2)味精主要成分是谷氨酸钠,其鲜味与溶液的酸碱度有关,当 pH 为 6﹣7 时鲜味最强:
鲜味还与温度有关,当烧菜时温度长时间在 120℃以上,不仅鲜味消失,而且会生产焦谷氨
酸钠.则下列认识正确的是
A.在碱性较强的条件下使用味精鲜味最强
B.谷氨酸钠在加热条件下生产焦谷氨酸钠是物理变化
C.起锅时加入味精比菜刚入锅时加入味精的鲜味更强.
5.(6 分)许多科学家发现从重视微小差异开始,科学家瑞利和拉姆塞正是重视氮气密度的
微小差异,才最终发现了稀有气体氮气.
材料一:1892 年瑞利发现,在相同条件下,由空气中除去氧气、二氧化碳、水蒸气和灰尘
后获得的氮气,其密度为 1.2572 克/升;由含氮化合物反应并除去水蒸气后获得的氮气
(NH4NO2≜ N2↑+2H2O),其目的为 1.2505 克/升.两者密度差值虽小,却完全超出了实验误
差范围.
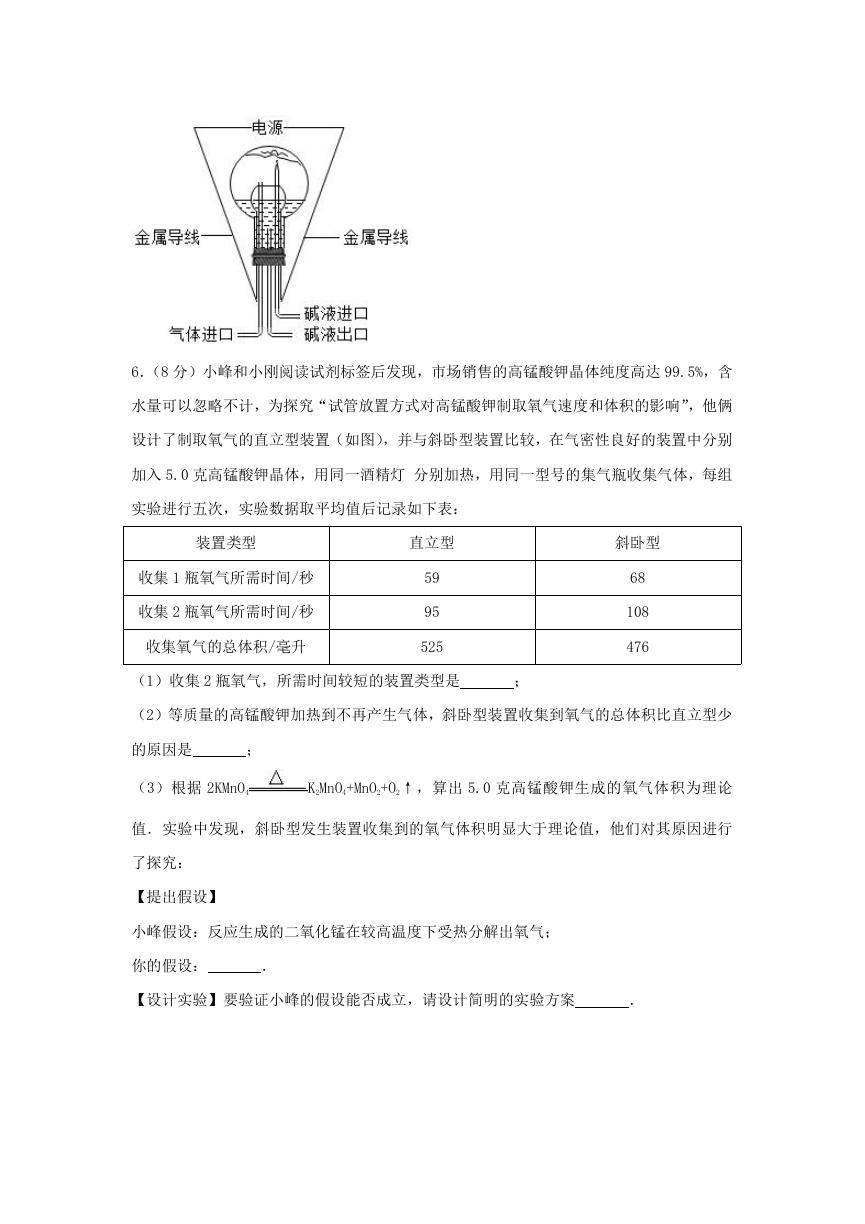
材料二:1984 年 4 月瑞利和拉姆塞开始用如图装置进行“清除空气中氮气”的实验研究:
在倒立圆底烧瓶内引入两根金属导线,通电使瓶中空气中的氧气和氮气生成氮的氧化物,
用碱液来吸收生成的氮的氧化物和原有的二氧化碳气体.并从气体进口不断向瓶内补充氧
气,使反应持续进行.
材料三:瑞利和拉姆塞又设计了另一实验装置,将上述实验所得的气体干燥后,通过红热
的铜粉来除去其中的氧气,得到少量的剩余气体.对剩余气体做光谱分析得知,这是一种
未知的气体,并测得其密度约是氮气的 1.5 倍.1894 年 8 月 13 日他们共同宣布:发现了一
种未知气体,并命名为氮气.
材料四:1989 年拉姆塞等人利用不同物质沸点不同,又发现了氪气、氖气、氩气.
根据上述材料,回答下列问题:
(1)与纯净氮气密度值更接近的是由
获得的氮气密度值(填“空气中”或“含氮
化合物反应”);
(2)实验中不断向瓶内补充氧气的目的是
;
(3)在当时实验条件下,很难利用化学反应除去氩气,获知“未知气体”中还有其他气体
存在,其理由是
.
�
6.(8 分)小峰和小刚阅读试剂标签后发现,市场销售的高锰酸钾晶体纯度高达 99.5%,含
水量可以忽略不计,为探究“试管放置方式对高锰酸钾制取氧气速度和体积的影响”,他俩
设计了制取氧气的直立型装置(如图),并与斜卧型装置比较,在气密性良好的装置中分别
加入 5.0 克高锰酸钾晶体,用同一酒精灯 分别加热,用同一型号的集气瓶收集气体,每组
实验进行五次,实验数据取平均值后记录如下表:
装置类型
直立型
斜卧型
收集 1 瓶氧气所需时间/秒
收集 2 瓶氧气所需时间/秒
收集氧气的总体积/毫升
59
95
525
68
108
476
(1)收集 2 瓶氧气,所需时间较短的装置类型是
;
(2)等质量的高锰酸钾加热到不再产生气体,斜卧型装置收集到氧气的总体积比直立型少
的原因是
;
(3)根据 2KMnO4
K2MnO4+MnO2+O2↑,算出 5.0 克高锰酸钾生成的氧气体积为理论
值.实验中发现,斜卧型发生装置收集到的氧气体积明显大于理论值,他们对其原因进行
了探究:
【提出假设】
小峰假设:反应生成的二氧化锰在较高温度下受热分解出氧气;
你的假设:
.
【设计实验】要验证小峰的假设能否成立,请设计简明的实验方案
.
�
7.(7 分)儿童缺锌会引起食欲不振、发育不良等症状.如图为某补锌口服液说明书的部分
信息,回答下列问题:
(1)葡萄糖酸锌由
种元素组成;
(2)葡萄糖酸锌中碳、氢元素的质量比为
;
(3)要满足儿童身体正常发育的需要,在某一时间段需要适量补锌.若儿童 1 千克体重每
日需要 0.5 毫克锌,每天从食物中只能摄入所需锌的一半.体重为 20 千克的儿童,理论上
一天还需服该口服液多少支?
8.(8 分)2017 年 5 月 18 日,国土资源部发布消息,在南海北部 1266 米深的神弧海域,
中国首次海域“可燃冰”试采成功.
查阅资料发现,古代低等生物遗骸大量沉积,经过漫长的地质年代形成石油及天然气,海
底的天然气与水在高压低温条件下形成的类冰状的固体物质即“可燃冰”.“可燃冰”为甲
烷的水合物,遇火即可燃烧且热值高,是一种环保、高效的新能源.
(1)若甲烷的水合物化学式为 CH4•8H2O,它的相对分子质量是 160,则 CH4•8H2O 中 CH4 的质
量分数为
;
(2)可燃冰储存的巨大的化学能最终来自于古代绿色植物通过
固定的太阳能;
(3)可燃冰燃烧时把自己的热量释放出去,就不会再次自动聚集起来供人类重新利用,这
说明能量的转化具有
性;
(4)人类正面临常规能源枯竭的危机,下列有关能源的认识正确的是
.
A.提高能源利用效率
�
B.积极寻找替代常规能源的新能源
C.自然界的能量虽然守恒,但还是要节约能源.
9.(9 分)BaCl2 是一种重金属盐,其水溶液具有很强的毒性,若误服了 BaCl2 溶液,可立即
服用 MgSO4 溶液解毒,为测定某 BaCl2 溶液的溶质质量分数,现取 100 克 BaCl2 溶液,不断
加入 MgSO4 溶液,反应过程中溶液总质量与加入 MgSO4 溶液的质量关系如图所示,请回答:
(1)P 点时溶液的溶质名称是
;
(2)反应生成沉淀的最大质量为
克;
(3)求原 BaCl2 溶液的溶质质量分数.
�
2017 年浙江省丽水市中考化学试卷
参考答案与试题解析
一、选择题(共 3 小题,第 1 小题 4 分,第 2、3 小题 3 分,满分 10 分)
1.(4 分)(2017•丽水)如图为某文化衫图案,你的美(Mg)偷走我的心(Zn)能发生,是
由于镁的(
)
A.延展性好 B.导电性好
C.导热性好 D.金属活动性比锌强
【分析】镁比锌活泼,能和硫酸锌反应生成硫酸镁和锌.
【解答】解:你的美(Mg)偷走我的心(Zn)能发生,是由于镁的金属活动性比锌强,能
和硫酸锌反应生成硫酸镁和锌,反应的化学方程式为:
Mg+ZnSO4=MgSO4+Zn.
故选:D.
2.(3 分)(2017•丽水)科技人员成功研制出一种新型催化剂,可将二氧化碳转化成液体燃
料,反应的微观示意图如下,有关该反应的说法正确的是(
)
A.该反应属于化合反应
B.反应前碳元素的化合价为+2 价
C.生成物的化学式可用 C2H2O 表示
D.参加反应的两物质的质量比为 1:1
�
【分析】根据题目信息结合微观示意图排除未反应的分子的干扰可写出反应的方程式为:
CO2+H2
H2CO2,据此分析物质的类别、反应的类型等.
【解答】解:据题目信息结合微观示意图排除未反应的分子的干扰可写出反应的方程式为:
CO2+H2
H2CO2
A、由上述反应可知,该反应符合“多合一”的特点,属于化合反应,故正确;
B、反应前二氧化碳中碳元素的化合价为+4 价,故错误;
C、由微粒的构成可知,得到的液体燃料化学式为:H2CO2,故错误;
D、上述反应可知,参加反应的两物质的质量比为(12+16×2):(1×2)=22:1,故错误.
答案:A.
3.(3 分)(2017•丽水)实验室有一瓶标签脱落的固体试剂,现分别取少量的该固体进行下
列实验,根据实验现象判断,该固体最可能是(
)
实验操作
取该固体于试管中,加水、振荡
实验现象
固体不溶解
取该固体于试管中,加盐酸、振荡
固体溶解,无气泡产生
一氧化碳通过炽热的该固体,称固体质量、检测
固体质量减轻,尾气中只检测到 CO 与
尾气
CO2
A.碱 B.盐 C.金属单质 D.金属氧化物
【分析】根据题意,取该固体于试管中,加水、振荡,固体不溶解,说明该固体难溶于水;
取该固体于试管中,加盐酸、振荡,固体溶解,无气泡产生,说明该固体能与稀盐酸反应,
且没有气体生成;一氧化碳通过炽热的该固体,称固体质量、检测尾气,说明该固体能与
一氧化碳反应,一氧化碳夺取了固体中的氧,进行分析判断.
【解答】解:取该固体于试管中,加水、振荡,固体不溶解,说明该固体难溶于水;取该
固体于试管中,加盐酸、振荡,固体溶解,无气泡产生,说明该固体能与稀盐酸反应,且
没有气体生成;一氧化碳通过炽热的该固体,称固体质量、检测尾气,说明该固体能与一
氧化碳反应,一氧化碳夺取了固体中的氧,应为金属氧化物,因为金属氧化物能与盐酸反
应生成盐和水,能与一氧化碳反应生成金属和二氧化碳.
A、碱不一氧化碳反应,故选项错误.
B、盐不与一氧化炭反应,故选项错误.
�
C、能与稀盐酸反应的金属单质,与稀盐酸反应会生成氢气,故选项错误.
D、由上述分析,该固体最可能是金属氧化物,故选项正确.
故选:D.
二、填空题(共 6 小题,每空 2 分,满分 42 分)
4.(4 分)(2017•丽水)家庭厨房就是一个科学小世界,其中包含着许多科学知识.
(1)大米、小麦为人体提供的主要营养素是 糖类 .
(2)味精主要成分是谷氨酸钠,其鲜味与溶液的酸碱度有关,当 pH 为 6﹣7 时鲜味最强:
鲜味还与温度有关,当烧菜时温度长时间在 120℃以上,不仅鲜味消失,而且会生产焦谷氨
酸钠.则下列认识正确的是 C
A.在碱性较强的条件下使用味精鲜味最强
B.谷氨酸钠在加热条件下生产焦谷氨酸钠是物理变化
C.起锅时加入味精比菜刚入锅时加入味精的鲜味更强.
【分析】(1)根据常见的食物中含有的营养素进行分析;
(2)根据味精的特性进行分析.
【解答】解:(1)大米、小麦中含有较多的淀粉,淀粉属于糖类;
(2)A、由于味精的鲜味与溶液的酸碱度有关,当 pH 为 6﹣7 时鲜味最强,故 A 正确;
B、由于味精长时间加热,会生成对人体有害的焦谷氨酸钠.有新物质生成,属于化学变化.故
B 错误;
C、由于味精长时间加热,会发生变化,生成对人体有害的物质焦谷氨酸钠,故 C 正确.
故填:(1)糖类;(2)C.
5.(6 分)(2017•丽水)许多科学家发现从重视微小差异开始,科学家瑞利和拉姆塞正是重
视氮气密度的微小差异,才最终发现了稀有气体氮气.
材料一:1892 年瑞利发现,在相同条件下,由空气中除去氧气、二氧化碳、水蒸气和灰尘
后获得的氮气,其密度为 1.2572 克/升;由含氮化合物反应并除去水蒸气后获得的氮气
(NH4NO2≜ N2↑+2H2O),其目的为 1.2505 克/升.两者密度差值虽小,却完全超出了实验误
差范围.
材料二:1984 年 4 月瑞利和拉姆塞开始用如图装置进行“清除空气中氮气”的实验研究:
�















 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc