2017 山东省济南市中考化学真题及答案
(考试时间:50 分钟 满分:60 分)
可能用到的相对原子质量 H 1
C 12
N 14
O 16
Na 23
Mg 24
Al 27
Si 28
P 31
S 32
Cl 35.5
K 39
Ca 40
Mn 55
Fe 56
Cu 64
Zn 65
Ag 108 Ba 137
Au 197
第Ⅰ卷(选择题 共 22 分)
一、选择题(本题包括 11 个小题,每小题 2 分,共 22 分.每小题只有一个选项符合题意)
1.赏中华诗词,品生活之美.下列诗词中,不涉及化学变化的是(
).
A.爆竹声中一岁除,春风送暖入屠苏
B.北国风光,千里冰封,万里雪飘
C.人间巧艺夺天工,炼药燃灯清昼同
D.野火烧不尽,春风吹又生
2.泉城济南,有“四面荷花三面柳,一城山色半城湖”的美誉.保护碧水蓝天,是我们每
个公民的责任.下列做法中,有利于环境保护的是(
).
A.种植花草树木,增加绿地面积
B.随意丢弃快递包装等垃圾
C.把废旧电池埋入水中处理
D.工业污水直接排入小清河
3.化学是一门以实验为基础的自然学科.下列实验操作中,正确的是(
).
A.加热液体
B.稀释浓硫酸
C.点燃酒精灯
D.过滤
4.化学与我们的健康、生产、生活息息相关.下列说法中,不正确的是(
).
A.变质食品中常含霉菌毒素,不可食用
B.室内放置一盆水,不能防止煤气中毒
C.夜间室内煤所泄漏,立即开灯检查
D.工业生产中储运烧碱,可用铁桶盛装
5.如图是钠原子结构示意图及在元素周期表中的部分信息,下列判断中,不正确的是
(
).
�
A.钠原子核内有 11 个质子
B.钠原子和钠离子电子层数不相同
C.钠元素在化合物中常显﹣1 价
D.钠的相对原子质量为 22.99
6.下列说法中,不正确的是(
).
A.溶液中有晶体析出时,溶质质量减小,则溶质质量分数一定减小
B.将钢铁制成合金是有效减缓钢铁制口锈蚀的方法之一
C.碱溶液中都含有氢氧根离子,因此碱具有相似的化学性质
D.自然界中二氧化碳的循环平衡,对地球生命有重要意义
7.宏观辨识与微观探析是化学学科的重要核心素养.如图为某化学反应的微观模拟示意图,
下列说法中,正确的是(
).
A.反应前后氧元素的化合价没有改变
B.生成的丙、丁两物质的分子个数比为 2:1
C.该反应属于复分解反应
D.参加反应的甲、乙两物质的质量比为 13:16
8.以下实验方案设计中,不能达到实验目的的是(
).
A.除去 N2 中混有的少量 O2:通过灼热的铜网
B.检验 Na2CO3 中是否混有 NaCl:先加足量稀硝酸,再加入 AgNO3 溶液,观察现象
C.鉴别 NaOH 固体和 NH4NO3 固体:加水溶解,观测现象
D.除去 CaO 中混有的少量 CaCO3:加入足量水,过滤
9.某无色溶液 X 是稀盐酸、稀硫酸、NaOH 溶液、Na2CO3 溶液中的一种,取三份等质量的 X
溶液,向其中分别加入酚酞试液、Fe2O3 粉末、BaCl2 溶液,产生的现象如下表所述.根据现
象判断,无色溶液 X 是(
).
加入的物质
酚酞试液
Fe2O3 粉末
BaCl2 溶液
实验现象
无明显现象
固体逐渐溶解,溶液变黄
无明显现象
A.稀盐酸
C.NaOH 溶液
B.稀硫酸
D.Na2CO3 溶液
10.将未知金属 M 和金属镁的粉末状混合物共 ag,加入一定质量的 Cu(NO3)2、Fe(NO3)2 的混
合溶液中,充分反应后过滤,得到滤液和滤渣.下列有关判断中,正确的是(
).
�
A.若滤渣中含有 Cu、Fe,则滤液一定为无色溶液
B.滤渣的质量一定大于 ag
C.若向滤渣中加入稀盐酸没有气泡产生,则滤渣中一定只含有 Cu
D.若滤液中金属离子只含有 Mg2+,则金属活动性由强到弱的顺序有可能为 Mg﹥Fe﹥M﹥Cu
11.烧杯中盛有一定质量的 MgO 和 Mg(OH)2 的固体混合物,向其中加入氢元素质量分数为
10%的稀硫酸 100g,恰好完全反应,得到 106g 该温度下的不饱和溶液.下列数据中,与原
固体混合物中 Mg(OH)2 的质量分数最接近的是(
).
A.53.7%
B.59.2%
C.62.5%
D.67.2%
一、非选择题(本题包括 7 个小题,共 38 分)
第Ⅱ卷(非选择题 共 38 分)
12.(4 分)按要求从氧化钙、氢气、氢氧化铜、硫酸、碳酸钠、二氧化硫中选取合适的物
质,将其化学式写在下列横线上.
(1)一种可燃性气体________.
(2)一种非金属氧化物________.
(3)一种难溶性的碱________.
(4)一种不易挥发的酸________.
13.(4 分)争创文明城市,共建美丽泉城,保护生态环境,倡导健康生活.
(1)2017 年 1 月,摩拜单车人驻济南,解决了市民出行“最后一公里”的问题.摩拜单车
的实体轮胎,采用的最新型 PU 材料,具有缓冲好、免充气、不怕扎、可回收等优点.甲苯
二异氰酸酯是一种合成新型 PU 材料的单体,其分子式为 C9H6N2O2,在该物质中,碳、氢两种
元素的质量比为________(填写最简整数比).
(2)茶,一片树叶的技艺.这片神奇的东方树叶,曾伴随丝绸之路的驼铃和大航海时代的
货船,远赴西亚和欧洲.喝茶有益身体健康,茶叶中的茶多酚,有较好的抗癌、防治心血
管病和抗辐射作用.EGCG(分子式:C22H23O11)是茶多酚中的一种主要成分,C22H23O11 属于
________(填“混合物”“氧化物”“无机物”或“有机物”之一).
�
(3)“珍爱生命、远离烟草、拒绝毒品”是一种健康向上的生活理念.甲基苯丙胺俗称“冰
毒”,其分子式为 C13H11N,是一种危害极大的毒品.在________g 甲基苯丙胺中含有 60g 碳
元素(计算结果精确至 0.1g).
(4)保护生态环境,倡导健康生活,文明与我同行.下列说法中与之相符合的是________
(填“A”“B”“C”或“D”之一).
①近距离出行尽量步行或骑单车
②儿童不能盲目吃各种营养补品
③公共场所吸烟不影响他人健康
④拒绝毒品就是保护自己和家人
A.只有①④
C.只有①③④
B.只有①②④
D.只有②③
14.(4 分)2017 年 4 月,天舟一号货运飞船发射成功,并完成与天宫二号的首次推进剂在
轨补加试验,也正式宣告中国航天迈进“空间站时代”.中国航天工程的大发展离不开化学
科学的支持.
(1)偏二甲肼(C2H8H2)是早期“长征二 F”运载火箭的一种燃料.其燃烧的化学方程式为
C2H8H2+2N2O4
点燃
3X+2CO2+4H2O,则 X 的化学式为________.
(2)发射“天舟一号”的“长征七号遥二”运载火箭采用液氧和煤基航天煤油作推进剂.煤
基航天煤油是新型高能燃料,分子式可用 CH3(CH2)nCH3 来表示(式中 n=8~16).下列有关说
法正确的是________(填“A”“B”“C”或“D”之一).
①液氧变成氧气,分子种类发生改变
②液氧(O2)与臭氧(O3)组成的物质属于单质
③煤基航天煤油燃烧,需要温度达到其着火点
�
④煤基航天煤油燃烧时化学能转化为热能
⑤煤基航天煤油 CH3(CH2)nCH3,当 n 的数值不同时,性质有所差异
A.只有①②
C.只有③④⑤
B.只有②③⑤
D.只有②③④⑤
(3)航天工程中需要大量的金属材料.我国是最早掌握“湿法炼铜”的国家,西汉时期的
《淮南万毕术》中,就有“曾青得铁则化为铜”的记载.请你写出用铁和硝酸铜为原料进
行湿法炼铜的化学方程式:______________________________________________,该反应
属于________反应(填“化合”“分解”“置换”或“复分解”之一).
15.(5 分)南海是我国的固有领海,蕴含着丰富的海洋资源,2017 年 5 月 18 日,我国南
海神狐海域的可燃冰试采取得到圆满成功,实现历史性突破.
(1)可燃冰的主要成分是甲烷,试写出甲烷在空气中燃烧的化学方程式
______________________________.
(2)可燃冰被科学家誉为“未来能源”“21 世纪能源”,原因是
_____________________________________.
(3)1926 年我国著名化学家侯德榜先生创立了侯氏制碱法,促进了世界制碱技术的发展.侯
氏制碱法以食盐为主要原料制取纯碱,制得的纯碱中常含有少量氯化钠.Na2CO3 和 NaCl 的
溶解度曲线如图所示,试回答下列问题:
①t1℃时,NaCl 的溶解度________ Na2CO3 的溶解度(填“大于”“等于”或“小于”之一);
②t1℃时,50g 水中加入 10gNa2CO3,经充分溶解,所得溶液中溶质与溶液的质量之比为
________ (填最简整数比);
③t1℃时,将不同质量的碳酸钠饱和溶液和氯化钠饱和溶液均升温到 t2℃,此时所得碳酸钠
溶液溶质质量分数________ 氯化钠溶液溶质质量分数(填“大于”“等于”或“小于”或
“无法判断”之一).
�
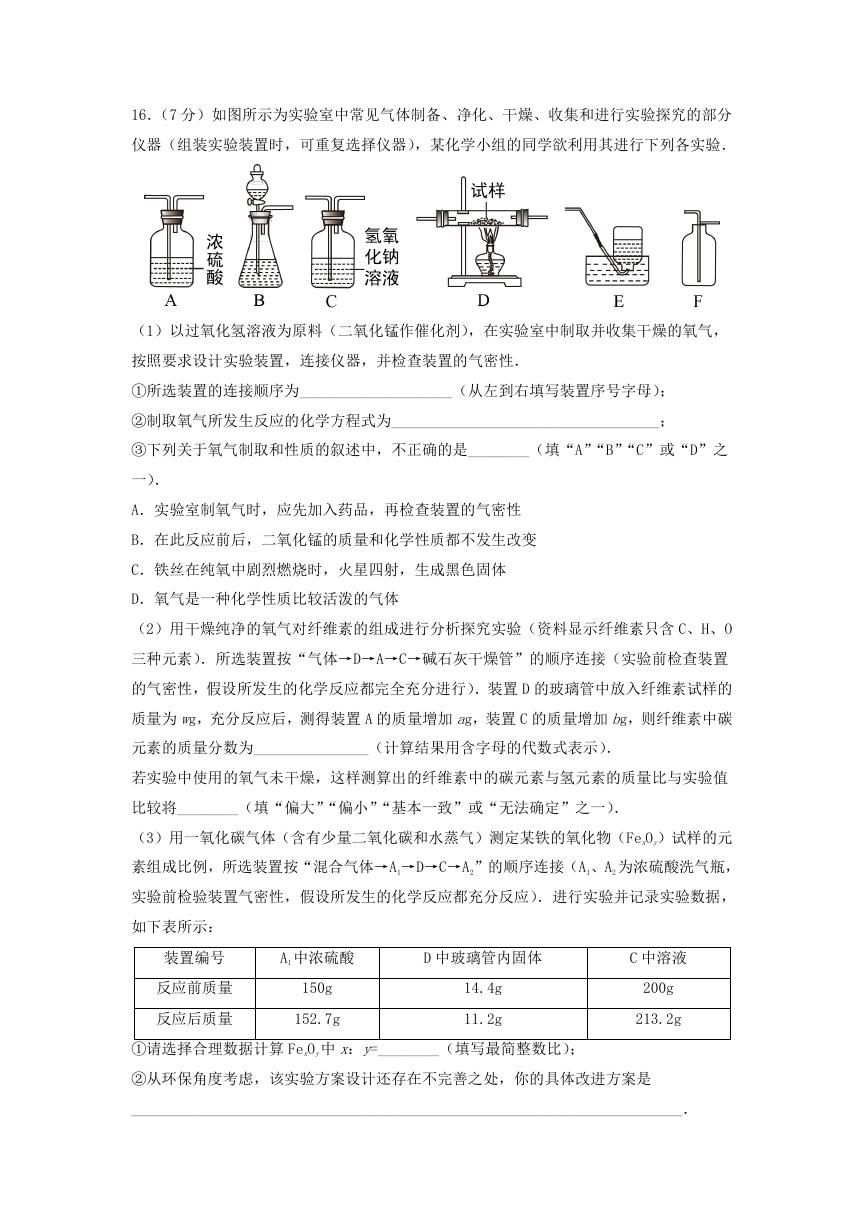
16.(7 分)如图所示为实验室中常见气体制备、净化、干燥、收集和进行实验探究的部分
仪器(组装实验装置时,可重复选择仪器),某化学小组的同学欲利用其进行下列各实验.
(1)以过氧化氢溶液为原料(二氧化锰作催化剂),在实验室中制取并收集干燥的氧气,
按照要求设计实验装置,连接仪器,并检查装置的气密性.
①所选装置的连接顺序为____________________(从左到右填写装置序号字母);
②制取氧气所发生反应的化学方程式为___________________________________;
③下列关于氧气制取和性质的叙述中,不正确的是________(填“A”“B”“C”或“D”之
一).
A.实验室制氧气时,应先加入药品,再检查装置的气密性
B.在此反应前后,二氧化锰的质量和化学性质都不发生改变
C.铁丝在纯氧中剧烈燃烧时,火星四射,生成黑色固体
D.氧气是一种化学性质比较活泼的气体
(2)用干燥纯净的氧气对纤维素的组成进行分析探究实验(资料显示纤维素只含 C、H、O
三种元素).所选装置按“气体→D→A→C→碱石灰干燥管”的顺序连接(实验前检查装置
的气密性,假设所发生的化学反应都完全充分进行).装置 D 的玻璃管中放入纤维素试样的
质量为 wg,充分反应后,测得装置 A 的质量增加 ag,装置 C 的质量增加 bg,则纤维素中碳
元素的质量分数为_______________(计算结果用含字母的代数式表示).
若实验中使用的氧气未干燥,这样测算出的纤维素中的碳元素与氢元素的质量比与实验值
比较将________(填“偏大”“偏小”“基本一致”或“无法确定”之一).
(3)用一氧化碳气体(含有少量二氧化碳和水蒸气)测定某铁的氧化物(FexOy)试样的元
素组成比例,所选装置按“混合气体→A1→D→C→A2”的顺序连接(A1、A2 为浓硫酸洗气瓶,
实验前检验装置气密性,假设所发生的化学反应都充分反应).进行实验并记录实验数据,
如下表所示:
装置编号
A1 中浓硫酸
D 中玻璃管内固体
反应前质量
150g
反应后质量
152.7g
14.4g
11.2g
C 中溶液
200g
213.2g
①请选择合理数据计算 FexOy中 x:y=________(填写最简整数比);
②从环保角度考虑,该实验方案设计还存在不完善之处,你的具体改进方案是
________________________________________________________________________.
�
17.(7 分)已知某固体样品 A 可能是 NH4NO3 和 MgCO3 或两者之一,另有一固体样品 B,其中
可能含有 Na2SO3、BaCl2、CuSO4、KCl 四种物质中的一种或多种,按下图所示进行探究实验,
出现的现象如图中所述(设计过程中所有发生的反应都恰好完全反应
...................).
试根据实验过程和发生的现象,填写以下空白.
(1)将气体 C 通入紫色石蕊试液,试液变________色.
(2)沉淀 F 的化学式为_______________.
(3)溶液 D 中,一定存在的阳离子是________(填写离子符号).
(4)写出步骤③中生成沉淀 I 的化学方程式__________________________________.
(5)在溶液 H 中,肯定存在的阴离子有________种.
(6)固体样品 B 中,一定不存在的物质是________(填写化学式),得出此结论的理由是
___________________________________________________________.
18.(7 分)海水中蕴藏着丰富的资源,海水“晒盐”过程中可得到粗盐和卤水.粗盐中常
含有多种杂质,必须对其进行分离和提纯,才能用于生产和生活;卤水经常用作工业制镁
的原料.
(1)实验室除去粗盐中不溶性杂质的步骤为:溶解、过滤、蒸发结晶.在三步中都要用到
的一种玻璃仪器是________.
(2)若要除去食盐固体中含有的少量 CaCl2 杂质,得到较为纯净的食盐固体.请简述实验
操作步骤
_______________________________________________________________________.
(3)在一烧杯中盛有 Mg(OH)2 和 MgCl2 的固体粉末 6g,向其中加入 20g 水,经充分溶解后,
再逐滴加入溶质质量分数为 10%的稀盐酸.烧杯中溶质的总质量与加入稀盐酸的质量关系如
图所示.请回答下列问题:
�
①当滴入稀盐酸 30g 时(即图中 A 点时),烧杯内溶液中的溶质是________(填写化学式);
②当滴入稀盐酸 73g 时(即图中 B 点时),试通过计算,求此温度时所得不饱和溶液中溶质
的质量(计算结果精确至 0.1g).
�















 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc