2003 年上海市中考化学真题及答案
(满分 120 分,考试时间 120 分钟)
相对原子质量(原子量):
H-1, C-12, O-16, Na-23, S-32, Cl-35.5, Fe-56, Cu-64, Ba-137
A.白醋
一、单项选择题(共 12 分)
1.将白醋、食用油、食盐、酒精分别放入水中,不能形成溶液的是………………(
D.酒精
2.碳的单质中,质地较软,常用作电极的是…………………………………………(
D.石墨
3.不会加剧酸雨、臭氧层空洞、温室效应等环境问题的是…………………………(
B.活性炭
A.金刚石
B.食用油
C.炭黑
C.食盐
A.使用太阳能淋浴器
C.超音速飞机尾气排放
B.燃烧煤
D.使用氟利昂作制冷剂
4.下列物质中属于无机化合物的是……………………………………………………(
D.甲烷
5.钾肥可以增加农作物的抗倒伏能力,目前农村常用的钾肥是……………………(
B.胆矾
C.蔗糖
A.锌
)
)
)
)
)
A.尿素
B.碳铵
C.硫铵
D.草木灰
6.氮化硅是一种新型陶瓷材料的主要成分,能承受高温,可用于制造业、航天业等领域。
已知氮、硅的原子结构示意图依次为 N
Si
请推测,氮化硅的
化学式(分子式)为………………(
)
A.Si3N4
B.Si4N3
D.Si7N3
7.距地球 15~35km 处,有一个臭氧层。关于臭氧的叙述不正确的是………………(
B.臭氧和氧气的性质完全相同
D.臭氧转化成氧气,发生了化学变化
8.下列有关实验现象的描述正确的是……………………………………………………
A.臭氧是一种单质
C.臭氧和氧气混合后形成的是混合物
C.Si3N7
)
)
(
A.铁丝在空气中被点燃,火星四射
B.氧化铁放入氢氧化钠溶液中,生成红褐色沉淀
C.点燃氢气和一氧化碳的混合气体,发生猛烈爆炸
D.氯化铜溶液中滴入氢氧化钠溶液,产生蓝色沉淀
9.在滴有石蕊试液的碳酸钠溶液中,加入过量盐酸,加盐酸前后溶液的颜色依次为…
(
)
A.紫色、红色
D.红色、无色
10.水煤气的组成是一氧化碳和氢气,它们可由水蒸气和灼热的焦炭反应制得。在该反
B.红色、紫色
C.蓝色、红色
应中,还原剂是………………………(
)
�
A.氢气
C.水蒸气
D.焦炭
11.往 5.6g 混有少量铜粉的铁粉中加入少量稀硫酸,产生氢气的质量………………(
B.一氧化碳
)
A.大于 0.2 克
B.等于 0.2 克
C.小于 0.2 克
D.无法确定
12.在一定温度下,将少量生石灰放入一定量的饱和石灰水中,搅拌并冷却到原来温度,
下列说法正确的是……………………………………………………(
A.溶剂质量不变
B.溶质质量增加
C.溶液浓度不变
)
D.溶解度增大
二、填空题(共 12 分)
13.维生素 C (C6H8O6)可促进人体生长发育,增加人体对疾病的抵抗力。维生素 C 是由
_______种元素组成的,每个维生素 C 分子是由_________个原子构成的。
14.纳米材料和纳米技术的应用涉及现代生产和生活的各个方面。用纳米级的某种氧化
物作催化剂,使汽车尾气中 CO 和 NO 反应,并转化为两种气体,其中一种可参与植
物 的 光 合 作 用 , 另 一 种 是 空 气 中 含 量 最 多 的 气 体 , 这 两 种 气 体 是 ________ 和
_________。
15.某地区发生水灾,为了解决当地居民缺乏洁净的生活用水问题,支援灾区的上海医
疗队员们挨家挨户的发放固体净水剂并标明用量,其中一包是漂粉精,其作用是杀
菌消毒;另一包是明矾,其作用是___________。
16.氢气是一种绿色能源,以它为燃料的电池正逐渐被应用到人们的生活中,有许多方
法可以得到氢气,请写出其中一种方法(用化学方程式表示),并指出该反应的基本
反应类型:_________________________,_____________________________。
17.“非典”肆虐时期,过氧乙酸(C2H4O3)是被人们广泛使用的消毒剂,它无色且有辛辣味;
具有强氧化性,温度稍高即分解放出氧气并生成醋酸(C2H4O2)。请写出过氧乙酸分解
的化学方程式______________________________________________________。
18.在硝酸银溶液中加入盐 A 的溶液,产生白色沉淀。过
滤后在滤渣中滴加稀硝酸,沉淀不溶解;在滤液中再
加入钠盐 B 的溶液,又产生白色沉淀。过滤后在滤渣
中的加稀硝酸,沉淀不溶解。则 A 为____________;B
为____________。
19.右图是病人输液时用的一瓶葡萄糖注射液标签,请根
据标签给出的数据计算该溶液中含水__________g,溶
液的密度约为_________g/cm3。
三、简答题(共 21 分)
20. 化学家舍勒和普利斯特里早在 18 世纪就先后独立地发现了氧气,但由于受“燃
素理论”的影响(即认为一切可以燃烧的物质都是由灰和“燃素”组成的,物质燃
烧后剩下的是灰,而燃素本身变成了光和热,散逸到空中去了),使他们放弃了自己
的研究成果。
根据“燃素理论”推知,燃烧后物质的质量应当减轻,但法国化学家拉瓦锡在
研究磷以及一些金属燃烧时,做了大量定量实验,实验结果都与“燃素理论”相违
�
背。他大胆质疑,尊重实验事实,进行深入研究,克服重重阻力,击破了“燃素理
论”,真正发现了氧气。
请回答:
⑴ 拉 瓦 锡 之 所 以 成 为 氧 气 的 真 正 发 现 者 , 应 该 归 功 于 拉 瓦 锡 具 有
________________________________________________的科学精神。
⑵拉瓦锡推翻“燃素理论”的实验事实是:__________________________________。
⑶ 用 学 过 的 理 论 解 释 磷 燃 烧 时 质 量 的 变 化 情 况 :
________________________________。
⑷ 写 出 实 验 室 制 备 氧 气 的 化 学 方 程 式 :
________________________________________。
⑸实验室可用____________法来收集氧气。
⑹用⑷⑸中的方法制备和收集氧气时,需要的玻璃仪器是(填编号):__________。
a.试管
b.漏斗 c.酒精灯
d.导管 e.胶头滴管 f.集气瓶
g.量筒
21.某金属冶炼厂的管道烟泥中含有某些金属,随
机取样对烟泥进行分析。由右表中的数据可知,
在烟泥中含有相当量的铜、锌以及能造成污染
的硫。因此从效益和环保角度出发,应考虑把
铜、锌回收利用,并对硫进行适当的处理。
[设计方案]
烟 泥 ( 含
Cu、Zn、
S 等)
通空气加热
①
固体
稀硫酸
固体混
②
合物
过滤
③
液体
硫酸锌
溶液
硫酸锌
⑤
固体
混合
溶液 A
④
铜
滤渣
(水洗后作建筑材料)
⑴写出步骤①②中含铜元素的物质发生反应的化学方程式:
①________________________________、②____________________________。
⑵写出本方案中处理废气的方法(用化学方程式表示):___________________。
⑶步骤⑤中所用的操作方法是:___________。
⑷在步骤④中,可选用试剂___________从混合溶液 A 中得到铜。
22.用下图中的装置 A 可进行气体和固体反应。
⑴请在下表中写出三组不同的反应物(三组中气体必须各不相同)。
�
⑵请在上述三组中,挑选出有气体产物生成的一组,先在方框 B 中填入组别编号,
然后画出检验该气体产物所需的装置,并指明所画仪器中盛放药品的名称。
23.⑴实验室制取大量 CO2 气体,是否能用稀硫酸和大理石为原料?______(填“是”或
“否”)为什么?_____________________________________________________
⑵右图是实验室制备 CO2 的装置图。该装置的特点是:打
开弹簧夹,大理石和盐酸接触,发生反应;关闭弹簧夹后,
盐酸被反应产生的 CO2 气体压回长颈漏斗,与大理石分离,
停止反应。用该装置制备 CO2 可起到节约药品和取用方便
的效果。下图装置中哪些可以起到与右图装置相同的效
果?_________(填写编号)
⑶某同学设计了一个有关 CO2 的探究实验,以下是实验报告的一部分,请仔细阅读后
填写实验目的及有关仪器名称。
[实验目的]________________________________
[仪器和试剂]_______________________________、玻璃管、CO2、气体、肥皂水。
实验步骤
现象及结论
1.将标有“A”和“B”的两个空量筒(200mL)
放在实验桌上,往 B 量筒中充满 CO2 气体。
2.用玻璃管蘸取少量肥皂水,在两个量筒上
方分别吹出一个肥皂泡(两个肥皂泡大小相
仿,内含空气),使其缓缓落入两个量筒中,
并观察现象。
A 量筒中的肥皂泡不久即沉入底部,
而 B 量筒中的肥皂泡基本不下沉,
悬浮在中间。说明二氧化碳密度比
空气大。
�
四、计算题(共 5 分)
24.在一定温度下,将 200g 硫酸钠溶液与 100g 氯化钡溶液混合,恰好完全反应。过滤
得到滤液 276.7g,往滤液中加入 83.7g 该滤液的溶质并恢复到原温度,溶液恰好饱
和。
求:⑴原硫酸钠溶液中溶质的质量
⑵滤液中的溶质在该温度下的溶解度为多少?
�
参考答案
说明:
1. 本试卷每格 1 分(除 50(1)、51(2)外)。
2. 物质名称、仪器名称和概念名称有错(包括错别字)不得分。
3. 化学方程式中化学式(分子式)有错不得分;配平、反应条件、气体或沉淀符号等有
错误,在每大题中共扣 1 分
一、单项选择题(共 12 分)
题号 1
答案 B
2
D
3
D
4
B
5
D
6
B
7
B
8
D
9
C
10
D
11
C
12
C
二、填空题(共 12 分)
13.3;20。
14.二氧化碳(或 CO2);氮气(或 N2)。
15.吸附(或凝聚、絮凝、沉降)
16.2H2O 通电
2H2↑+O2↑;分解反应。(或 Zn+H2SO4→ZnSO4+H2↑;置换反应)(合理均
给分)
17.2C2H3O3→2C2H4O2+O2↑
18.氯化钡(或 BaCl2);硫酸钠(或 Na2SO4)
19.237.5;1
三、简答题(共 21 分)
20.⑴大胆质疑,尊重实验事实,勇于探究、敢于创新。(合理均给分)
⑵磷以及一些金属燃烧后物质的质量增加。
⑶磷燃烧增重的质量等于参加反应的氧气的质量,符合质量守恒定律。(合理均给分)
⑷①2KClO3
2MnO
2KCl+3O2↑
(或②2KMnO4
K2MnO4+MnO2+O2↑、③2H2O2 2MnO
2H2O+O2↑)
⑸排水集气(或向上排空气)
⑹若⑷中写反应①或②:a,c,d,f。(全对得 1 分)
若⑷中写反应③:a,d,f。(全对得 1 分)
21.⑴2Cu+O2
2CuO;CuO+H2SO4→CuSO4+H2O
⑵2NaOH+SO2→Na2SO3+H2O(合理均给分)
⑶蒸发结晶(或蒸发、浓缩、结晶)
⑷Zn
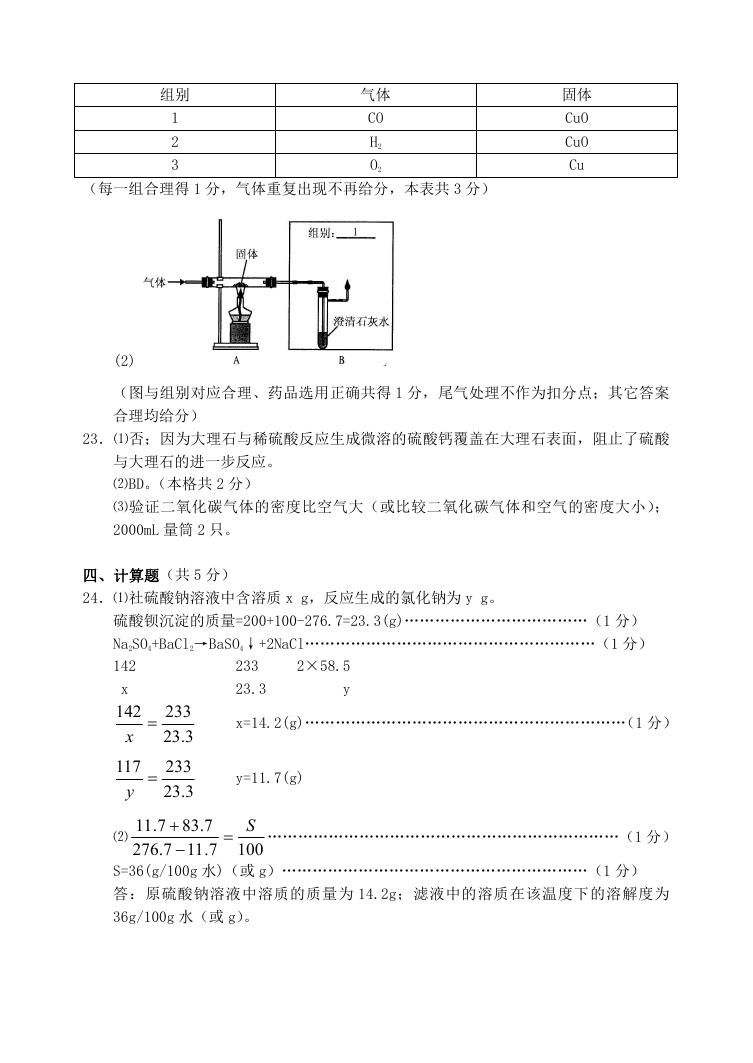
22.(1)
�
组别
1
2
3
气体
CO
H2
O2
固体
CuO
CuO
Cu
(每一组合理得 1 分,气体重复出现不再给分,本表共 3 分)
(2)
(图与组别对应合理、药品选用正确共得 1 分,尾气处理不作为扣分点;其它答案
合理均给分)
23.⑴否;因为大理石与稀硫酸反应生成微溶的硫酸钙覆盖在大理石表面,阻止了硫酸
与大理石的进一步反应。
⑵BD。(本格共 2 分)
⑶验证二氧化碳气体的密度比空气大(或比较二氧化碳气体和空气的密度大小);
2000mL 量筒 2 只。
四、计算题(共 5 分)
24.⑴社硫酸钠溶液中含溶质 x g,反应生成的氯化钠为 y g。
硫酸钡沉淀的质量=200+100-276.7=23.3(g)………………………………(1 分)
Na2SO4+BaCl2→BaSO4↓+2NaCl…………………………………………………(1 分)
142
233
23.3
2×58.5
y
x
142
x
117
y
233
3.23
233
3.23
7.83
7.11
7.
7.11
276
⑵
x=14.2(g)………………………………………………………(1 分)
y=11.7(g)
S
100
……………………………………………………………(1 分)
S=36(g/100g 水)(或 g)……………………………………………………(1 分)
答:原硫酸钠溶液中溶质的质量为 14.2g;滤液中的溶质在该温度下的溶解度为
36g/100g 水(或 g)。
�












 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc