2011 年河北高考理科综合真题及答案
本试卷分第 1 卷(选择题)和第 2 卷(非选择题)两部分,第 1 卷 1 至 4 页,第 II 卷 5 至
12
页,考试结束后,将本试题卷和答题卡一并交回。
第 I 卷
注意事项:
(1)答题前,考生在答题卡上务必用直径 0.5 毫米黑色墨水签字笔将自己的姓名、准考证号
填写清楚。并贴好条形码。请认真核准条形码上的准考证号、姓名和科目。
(2)每小题选出答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑,如需改动。用橡皮
擦干净后,在选涂其他答案编号,在试题卷上作答无效
.........。
(3)第 I 卷共 21 小题,每题 6 分,共 126 分。
以下数据可供解题时参考:
相对原子质量(原子量):Hl
S 32
C1 35.5
Cr52 Fe 56
Cl2
N14 016
Na23
Mg 24 A1 27
Cu 64
一、选择题:本大题共 l3 小题。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.下列能说明某细胞已经发生分化的是
A.进行 ATP 的合成
C.存在血红蛋白
B.进行 mRNA 的合成
D.存在纤维蛋白原基因
2.将紫色洋葱在完全营养液中浸泡一段时间,撕取外表皮,先用浓度为 0.3g/mL 的蔗糖溶液处
理,细胞发生质壁分离后,立即将外表皮放入蒸馏水中,直到细胞中的水分不再增加。若在
该实验过程中,蔗糖溶液处理前外表皮细胞液的浓度为甲,细胞中的水分不再增加时外表皮
细胞液的浓度为乙,则甲、乙的关系,以及实验过程中水分进出细胞的方式为
A.甲<乙,被动运输
C. 甲>乙,主动运输
B.甲>乙,被动运输
D.甲=乙,主动运输
3.将生长状态一致的同一品种玉米植株分为甲、乙两组,甲组培养在适宜的光照条件下,其叶维
管束鞘细胞中有淀粉积累;乙组培养在光照较弱的条件下,其叶维管束鞘细胞中没有检测到
淀粉。乙组来检测到淀粉的原因是
A.叶片不进行光合作用,只进行呼吸作用
B.叶片光合作用强度低,没有淀粉的积累
C.维管束鞘细胞没有与淀粉合成相关的酶
D.维管柬鞘细胞不含叶绿体,不能进行光合作用
4.某校园有一片草坪和一片树林,下列关于这两个群落中动物分层现象的叙述,正确
A.草坪和树林中的动物都具有分层现象
B.草坪和树林中的动物都没有分层现象
C.只有草坪和树林混杂在一起时动物才具有分层现象
D.草坪中的动物没有分层现象,而树林中的动物具有分层现象
5.研究发现两种现象:①动物体内的 B 细胞受到抗原刺激后,在物质甲的作用下,可增殖、分化
为效应 B 细胞;②给动物注射从某种细菌获得的物质乙后。此动物对这种细菌具有了免疫能
力。则这两种物质中
A.甲是抗体,乙是抗原
B.甲是抗体,乙是淋巴因子’
�
C.甲是进巴因子,乙是抗原
D.甲是淋巴因子,乙是抗体
6.等浓度的下列稀溶液:①乙酸、②苯酚、③碳酸、④乙醇,它们的 pH 由小到大排列正确的是
A.④②③①
B.③①②④
C.①②③④
D.①③②④
7.下列叙述错误的是
A.用金属钠可区分乙醇和乙醚
B.用高锰酸钾酸性溶液可区分己烷和 3-己烯
C.用水可区分苯和溴苯
D.用新制的银氨溶液可区分甲酸甲酯和乙醛
8.在容积可变的密闭容器中,2mol
2N 和 8mol
2H 在一定条件下反应,达到平衡时, 2H 的转化
率为 25%,则平衡时氨气的体积分数接近于
A.5%
B.10%
C.15%
D.20%
9.室温时,将浓度和体积分别为 1c 、 1V 的 NaOH 溶液和 2c 、 2V 的 3CH COOH 溶液相混合,下列
关于该混合溶液的叙述错误的是
A.若
ph ,则一定是 1 1
c v
7
c v
2 2
B.在任何情况下都是
(
c Na
)
(
c H
)
(
c CH COO
3
)
(
c OH
)
v
C.当 pH=7 时,若 1
v ,则一定是 2
c
2
c
1
v
D.若 1
v , 2
c
2
c ,则
1
(
c CH COO
3
)
(
c CH COOH
3
)
(
c Na
)
10.用石墨作电极电解
CuSO 溶液。通电一段时间后,欲使电解液恢复到起始状态,应向溶液中
4
加入适量的
.
A.
CuSO
4
B. 2H O
C.CuO
D.CuS04·5
2H O
11.将足量 2CO 通入下列各溶液中,所含离子还能大量共存的是
A.
K
B.
H
、SiO 、 、
Cl
2
3
NO
3
、NH 、 、
Al
3
4
2
SO
4
C.
Na
D.
Na
、S 、 、
OH
2
2
SO
4
、 H O 、CH
C
6
5
COO HCO
3
、
3
12. AN 为阿伏加德罗常数,下列叙述错误的是
A.18g
2H O 中含有的质子数为 10
AN
B.12g 金刚石中含有的共价键数为 4
AN
�
C.46g
2NO 和 2
4N O 混合气体中含有原子总数为 3
AN
D.1molNa 与足量 2O 反应,生成 2N O 和 2
2N O 的混合物,钠失去 AN 个电子
13.某含铬(r2O2-
7)废水用硫酸亚铁铵[FeSO4·(NH4)2SO4·6H2O]处理,反应中铁元素和铬元素完
全转化为沉淀。该沉淀干燥后得到 n molFeO·FeyCrx·O3。不考虑处理过程中的实际损耗,下
列叙述错误的是
B.处理废水中 Cr2O2-
7 的物质的量为
n
A.消耗硫酸亚铁铵的物质的量为 (2
)
x mol
nx mol
2
C.反应中发生转移的电子数为3nxmol
D.在 FeO·FeyCrx·O3 中,3x=y
二、选择题:本大题共 8 小题。在每小题给出的四个选项中,有的只有一个选项符合题目要求,
有的有多个选项符合题目要求。全部选对的得 6 分,选对但不全的得 3 分,有选错的得 0 分。
14.关于一定量的气体,下列叙述正确的是
A.气体吸收的热量可以完全转化为功
B.气体体积增大时,其内能一定减少
C.气体从外界吸收热量,其内能一定增加
D.外界对气体做功,气体内能可能减少
15.如图,两根相互平行的长直导线分别通有方向相反的电流 1I 和 2I ,且 1
I
I ;a、b、c、d
2
为导线某一横截面所在平面内的四点,且 a、b、c 与两导线共面;b 点在两导线之间,b、d
的连线与导线所在平面垂直。磁感应强度可能为零的点是
A.a 点
B.b 点
C.c 点
D.d 点
16.雨后太阳光入射到水滴中发生色散而形成彩虹。设水滴是球形的,图中
的圆代表水滴过球心的截面,入射光线在过此截面的平面内,a、b、c、
d 代表四条不同颜色的出射光线,则它们可能依次是
A.紫光、黄光、蓝光和红光
B.紫光、蓝光、黄光和红光
C.红光、蓝光、黄光和紫光
D.红光、黄光、蓝光和紫光
17.通常一次闪电过程历时约 0.2~O.3s,它由若干个相继发生的闪击构
成。每个闪击持续时间仅 40~80μs,电荷转移主要发生在第一个闪击过程中。在某一次闪
电前云地之间的电势差约为 1.0× 910 v,云地间距离约为 l km;第一个闪击过程中云地间
转移的电荷量约为 6 C,闪击持续时间约为 60μs。假定闪电前云地间的电场是均匀的。根据
以上数据,下列判断正确的是
A.闪电电流的瞬时值可达到 1× 510 A
�
B.整个闪电过程的平均功率约为 l× 1410 W
C.闪电前云地间的电场强度约为 l×106V/m
D.整个闪电过程向外释放的能量约为 6× 610 j
18.已知氢原子的基态能量为 E1,激发态能量
nE
2
1 /
E n
,其中 n=2,3…。用 h 表示普朗克常量,
c 表示真空中的光速。能使氢原子从第一激发态电离的光子的最大波长为
A.
4
hc
3
E
B.
2hc
E
1
C.
4hc
E
1
D.
9hc
E
1
19.我国“嫦娥一号”探月卫星发射后,先在“24 小时轨道”上绕地球运行(即绕地球一圈需要
24 小时);然后,经过两次变轨依次到达“48 小时轨道”和“72 小时轨道”;最后奔向月球。
如果按圆形轨道计算,并忽略卫星质量的变化,则在每次变轨完成后与变轨前相比,
A.卫星动能增大,引力势能减小
C.卫星动能减小,引力势能减小
B.卫星动能增大,引力势能增大
D.卫星动能减小,引力势能增大
20.质量为 M、内壁间距为 L 的箱子静止于光滑的水平面上,箱子中间有一质量为 m 的小物块,
小物块与箱子底板间的动摩擦因数为μ。初始时小物块停在箱子正中间,如图所示。现给小
物块一水平向右的初速度 v,小物块与箱壁碰撞 N 次后恰又回到箱子正中间,井与箱子保持
相对静止。设碰撞都是弹性的,则整个过程中,系统损失的动能为
A.
1
2
C. 1
2
2
mv
N mgL
2
B.
1
2
mM v
m M
D. N mgL
21.一列简谐横波沿 x 轴传播,波长为 1.2m,振幅为 A。当坐标为 x=0 处质元的位移为
3
2
A
且向 y 轴负方向运动时.坐标为 x=0.4m 处质元的位移为
3
2
A 。当坐标为 x=0.2m 处的质
元位于平衡位置且向 y 轴正方向运动时,x=0.4m 处质元的位移和运动方向分别为
A. 1
2
A
、延 y 轴正方向
C.
3
2
A
、延 y 轴正方向
A
B. 1
2
3
2
D.
,延 y 轴负方向
A
、延 y 轴负方向
第Ⅱ卷
注意事项:
1.答题前,考生先在答题卡上用直径 0.5 毫米黑色墨水签字笔将自己的姓名、准考证号填
写清楚,然后贴好条形码。请认真核准条形码上的准考证号、姓名和科目。
2.第Ⅱ卷共 8 页,请用直径 0.5 毫米黑色墨水签字笔在答题卡上各题的答题区域内作答,
�
在试题卷上作答无效。
..........
3.第Ⅱ卷共 13 题,共 174 分。
22.(6 分)(注意:在试题卷上作答无效)
在“油膜法估测油酸分子的大小”实验中,有下列实验步骤:
①往边长约为 40 cm 的浅盘里倒入约 2 cm 深的水.待水面稳定后将适量的痱子粉均匀地撒在
水面上。
②用注射器将事先配好的油酸酒精溶液滴一滴在水面上,待薄膜形状稳定。
③将画有油膜形状的玻璃板平放在坐标纸上,计算出油膜的面积,根据油酸的体积和面积计
算出油酸分子直径的大小。
④用注射器将事先配好的油酸酒精溶液一滴一滴地滴入量筒中,记下量筒内每增加一定体积
时的滴数,由此计算出一滴油酸酒精溶液的体积。
⑤将玻璃板放在浅盘上,然后将油膜的形状用彩笔描绘在玻璃板上。
完成下列填空:
(1)上述步骤中,正确的顺序是__________。(填写步骤前面的数字)
(2)将 1 cm3 的油酸溶于酒精,制成 300 cm3 的油酸酒精溶液;测得 l cm3 的油酸酒精溶液有
50 滴。现取一滴该油酸酒精溶液滴在水面上,测得所形成的油膜的面积是 0.13 m2。由
此估算出油酸分子的直径为_________m。(结果保留 l 位有效数字)
23.(12 分)(.注意:在试题卷上作答无效
............).
使用多用电表测量电阻时,多用电表内部的电路可以等效为一个直流电源(一般为电池)、一
个电阻和一表头相串联,两个表笔分别位于此串联电路的两端。现需要测量多用电表内电池
的电动势,给定的器材有:待测多用电表,量程为 60 mA 的电流表,电阻箱,导线若干。实
验时,将多用电表调至×1 Ω挡,调好零点;电阻箱置于适当数值。完成下列填空:
(1)仪器连线如图 l 所示(a 和 b 是多用电表的两个表笔)。若两电表均正常工作,则表笔 a
为_________ (填“红”或“黑”)色;
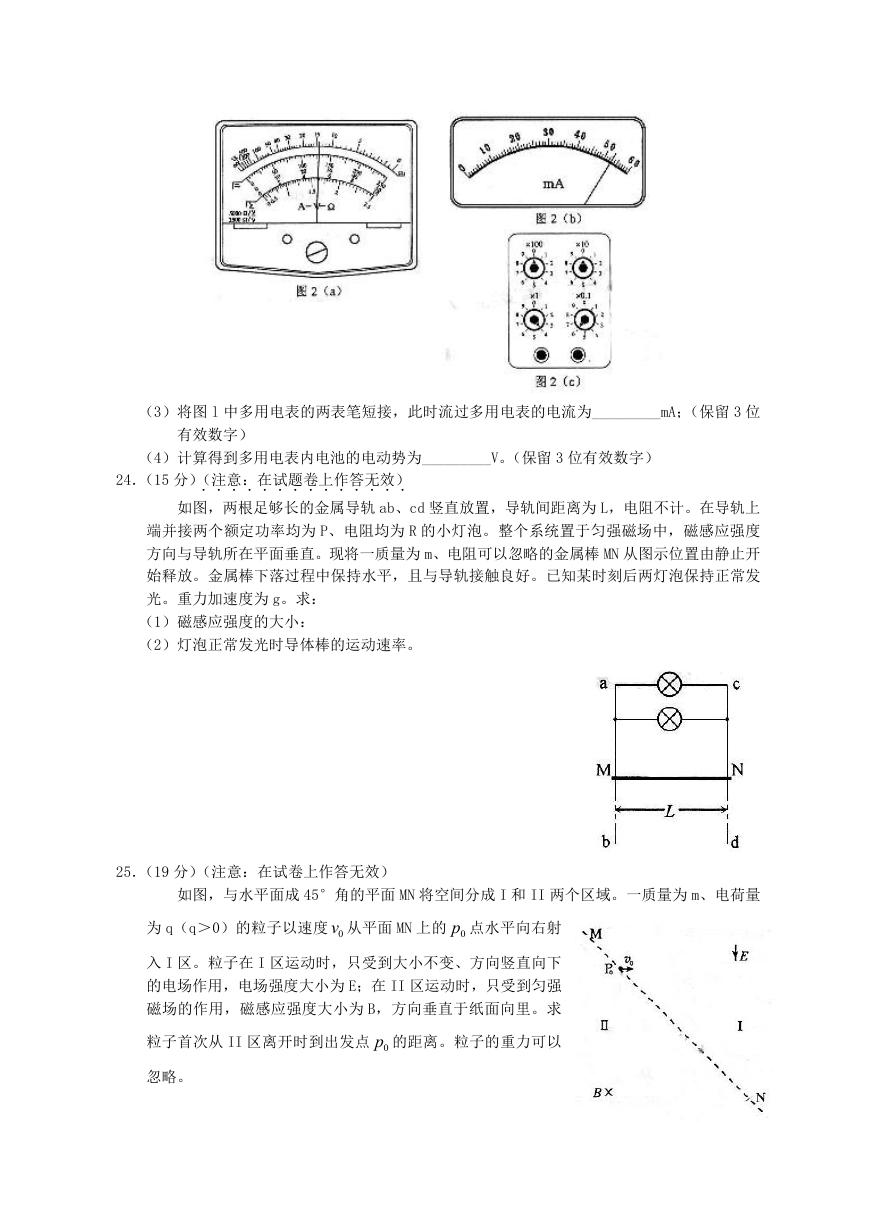
(2)若适当调节电阻箱后,图 1 中多用电表、电流表与电阻箱的示数分别如图 2(a),(b),
(c)所示,则多用电表的读数为_________Ω.电流表的读数为_________mA,电阻箱的
读数为_________Ω:
�
(3)将图 l 中多用电表的两表笔短接,此时流过多用电表的电流为_________mA;(保留 3 位
有效数字)
(4)计算得到多用电表内电池的电动势为_________V。(保留 3 位有效数字)
24.(15 分)(.注意:在试题卷上作答无效
............).
如图,两根足够长的金属导轨 ab、cd 竖直放置,导轨间距离为 L,电阻不计。在导轨上
端并接两个额定功率均为 P、电阻均为 R 的小灯泡。整个系统置于匀强磁场中,磁感应强度
方向与导轨所在平面垂直。现将一质量为 m、电阻可以忽略的金属棒 MN 从图示位置由静止开
始释放。金属棒下落过程中保持水平,且与导轨接触良好。已知某时刻后两灯泡保持正常发
光。重力加速度为 g。求:
(1)磁感应强度的大小:
(2)灯泡正常发光时导体棒的运动速率。
25.(19 分)(注意:在试卷上作答无效)
如图,与水平面成 45°角的平面 MN 将空间分成 I 和 II 两个区域。一质量为 m、电荷量
为 q(q>0)的粒子以速度 0v 从平面 MN 上的 0p 点水平向右射
入 I 区。粒子在 I 区运动时,只受到大小不变、方向竖直向下
的电场作用,电场强度大小为 E;在 II 区运动时,只受到匀强
磁场的作用,磁感应强度大小为 B,方向垂直于纸面向里。求
粒子首次从 II 区离开时到出发点 0p 的距离。粒子的重力可以
忽略。
�
26.(20 分)(注意:在试题卷上作答无效)
装甲车和战舰采用多层钢板比采用同样质量的单层钢板更能抵御穿甲弹的射击。通过对
以下简化模型的计算可以粗略说明其原因。
质量为 2m、厚度为 2d 的钢板静止在水平光滑桌面上。质量为 m 的子弹以某一速度垂直
射向该钢板,刚好能将钢板射穿。现把钢板分成厚度均为 d、质量均为 m 的相同两块,间隔
一段距离水平放置,如图所示。若子弹以相同的速度垂直射向第一块钢板,穿出后再射向第
二块钢板,求子弹射入第二块钢板的深度。设子弹在钢板中受到的阻力为恒力,且两块钢板
不会发生碰撞不计重力影响。
27.(15 分)(注意:在试卷上作答无效)
下图中,A、B、C、D、E 是单质,G、H、I、F 是 B、C、D、E 分别和 A 形成的二元化合物。已
知:
①反应 C+G
B+H 能放出大量的热,改反应曾应用于铁轨的焊接;
②I 是一种常见的温室气体,它和 E 可以发生反应:2E+I
2F+D,F 中 E 元素的质量分
数
�
为 60%。
回答问题:
(1)①中反应的化学方程式为
(2)化合物 I 的电子式为
(3)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,计算至少需铜粉的质量(写出粒子方
,它的空间结构是
;
;
程式和计算过程);
(4)C 与过量 NaOH 溶液反应的离子方程式为
(5)E 在 I 中燃烧观察到的现象是
28.(15 分)(注意:在试题卷上作答无效
.........)
;
。
反应 aA(g)+bB(g)
cC(g)( H<0)在等容条件下进行。改变其他反应条件,
在 I、II、III 阶段体系中各物质浓度随时间变化的曲线如下图所示:
回答问题:
(1)反应的化学方程式中,a:b:c 为
;
(2)A 的平均反应速率 Iv (A)、 IIv (A)、 IIIv (A)从大到小排列次序为
;
(3)B 的平衡转化率 (
a B
I
)
、
(
a B
II
)
、
a (
III
B
)
中最小的是
,其值是
;
(4)由第一次平衡到第二次平衡,平衡移动的方向是
,采取的措施是
;
(5)比较第 II 阶段反应温度( 2T )和第 III 阶段反应速度( 3T )的高低: 2T
3T 填“>、
=、<”判断的理由是
;
�















 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc