2016 年辽宁普通高中会考化学真题及答案
第Ⅰ卷(选择题 共 60 分)
一、选择题(本题包括 15 小题,每小题 4 分,共 60 分;每小题只有一个选项符合题意)
1.化学与生活息息相关。下列叙述中正确的是
A.单晶硅常用于制造光导纤维
B.馒头越嚼越甜
C.油脂经水解可变成葡萄糖
D.淀粉经水解可变成酒
2.“84”消毒液在日常生活中使用广泛,该消毒液无色,有漂白作用。它的有效成分是
A.NaClO
B.NaOH
C.Na2CO3
D.Na2O2
3.“化学,让生活更美好”。下列叙述不能直接体现这一主旨的是
A.合成可降解塑料,让环境更美好
B.风力发电,让能源更清洁
C.合成药物,让人类更健康
D.合成环保涂料,让居室更安全
4.下列物质分类合理的是
A
B
C
D
类别
金属氧化物 非金属单质 金属单质
含氧酸
物质
CaO
CO2
H2
N2
C
Zn
H2SO4 H2O
5.下列现象与氧化还原反应无关的是
A.铁制护栏生锈 B.食物的腐败 C.用天然气作燃料 D.蒸发海水制盐
6.NA 为阿伏加德罗常数的值。下列说法中正确的是
A.标准状况下,22.4 L 水中含有的分子数是 NA
B.28 g 氮气含有的原子数是 2NA
C.1 mol 铁与足量盐酸完全反应,失去的电子数为 3NA
D.常温常压下,11.2 L CO2 中含有的分子数是 0.5NA
7.关于金属钠的性质,下列叙述中正确的是
�
A.钠在空气中燃烧生成氧化钠
B.少量金属钠可以保存在冷水中
C.钠的焰色反应呈黄色
D.钠和硫酸铜溶液反应能置换出铜
8.进行化学实验时应强化安全意识。下列做法正确的是
A.金属钠着火时使用泡沫灭火器灭火
B.给盛有碳酸氢钠固体的试管加热时,使试管口竖直向上
C.浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗
D.氢气还原氧化铜时应先检验氢气的纯度
9.下列离子检验中,所选试剂及实验现象均正确的是
离子
试剂
实验现象
A
B
C
D
Cl-
2-
SO4
Fe3+
+
NH4
AgNO3 溶液
生成黄色沉淀
CaCl2 溶液
生成白色沉淀
KSCN 溶液
溶液呈红色
NaOH 溶液
生成无色无味气体
10.化学与能源开发、环境保护、资源利用等密切相关。下列说法正确的是
A.大力发展汽车工业,鼓励市民购买家用汽车
B.为提高农作物的产量和质量,应大量使用化肥和农药
C.赤潮是与人类活动无关的自然现象
D.绿色化学的核心就是利用化学原理从源头上减少和消除工业生产对环境的污染
11.下列反应的离子方程式书写错误的是
A.盐酸与氢氧化钠溶液反应:H+ + OH- = H2O
B.溴化钾溶液中通入氯气:Cl2 + 2Br- = 2Cl- + Br2
C.碳酸钙与稀盐酸反应:CaCO3 + 2H+ = Ca2+ + H2O + CO2↑
D.铝与氢氧化钠溶液反应:Al + 2H2O + OH- = AlO2
- + 2H2↑
12.下列物质可以用来制造耐火坩埚、耐火管和耐高温的实验仪器的是
A.Al2O3
B.Na2O
C.Fe2O3
D.CaO
�
13.下列装置中能够形成原电池的是
A
B
C
D
14.“吸烟有害健康”。吸烟时产生的烟气中有多种有害物质,其中尼古丁(C10H14N2)对人体危害最大。
下列说法正确的是
A.尼古丁分子是由 26 个原子构成的
B.尼古丁中 C、H、N 三种元素原子的质量比为 10∶14∶2
C.由题中信息不能算出尼古丁的相对分子质量
D.尼古丁不会造成室内空气污染
15.已知反应:2Al + Fe2O3
Al2O3 + 2Fe 为放热反应。下列说法正确的是
A.升高温度,该反应速率减慢
B.由该反应可知铁比铝活泼
C.反应物的总能量一定大于生成物的总能量
D.因该反应为放热反应,故不必加热就可发生
第Ⅱ卷(非选择题 共 40 分)
二、必考题(本题包括 3 个小题,共 25 分)
16.(8 分)右图是关于药物华素片(西地碘片)使用说明书的部分
内容。请回答下列问题:
⑴华素片中含有的活性成分是_____(写分子式),据此推测华素片
_____(填“是”或“不是”)白色的。
⑵学生甲为验证华素片中确实含有上述成分,设计实验如下,:取一
份】本品每片含分子碘
【药品名称】
通用名称:西地碘片
商品名称:华素片
【成
1.5 mg。辅料为薄荷脑等。
【贮
凉处保存。
【有效期】二年
藏】遮光、密闭、在阴
�
粒药片放入研钵中研碎,再将药粉装入试管并加入约 2 mL 蒸馏水;向该试管中再加入约 2 mL______(填
选项字母),并用力振荡,静置后观察到的实验现象是_______________。
a.酒精
b.醋酸
c.四氯化碳
⑶学生乙向盛有 2 mL 淀粉溶液的试管中,加入少量的华素片药粉,观察到_______的实验现象,也得出与
学生甲相同的结论。
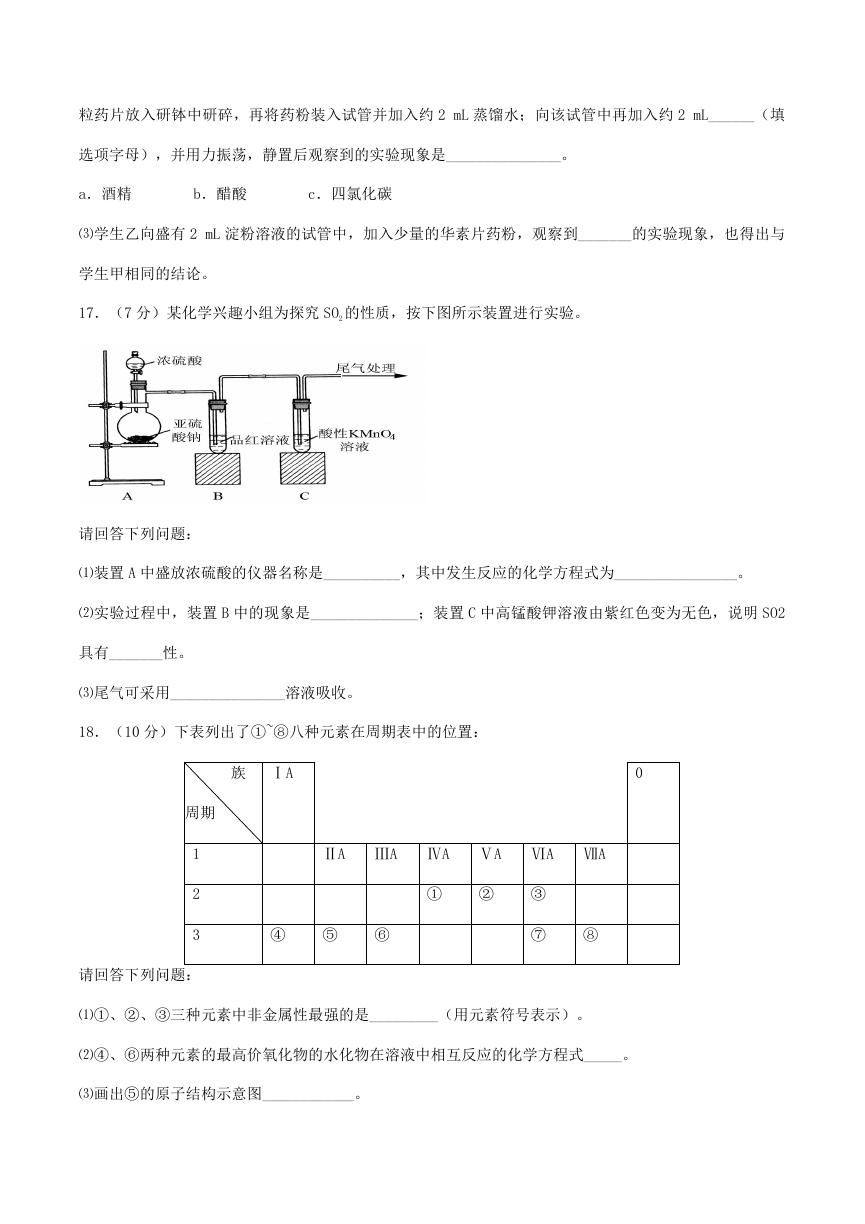
17.(7 分)某化学兴趣小组为探究 SO2 的性质,按下图所示装置进行实验。
请回答下列问题:
⑴装置 A 中盛放浓硫酸的仪器名称是__________,其中发生反应的化学方程式为________________。
⑵实验过程中,装置 B 中的现象是______________;装置 C 中高锰酸钾溶液由紫红色变为无色,说明 SO2
具有_______性。
⑶尾气可采用_______________溶液吸收。
18.(10 分)下表列出了①~⑧八种元素在周期表中的位置:
族
ⅠA
0
周期
1
2
3
请回答下列问题:
ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
④
⑤
⑥
①
②
③
⑦
⑧
⑴①、②、③三种元素中非金属性最强的是_________(用元素符号表示)。
⑵④、⑥两种元素的最高价氧化物的水化物在溶液中相互反应的化学方程式_____。
⑶画出⑤的原子结构示意图____________。
�
⑷⑦、⑧两种元素原子半径大小比较__________(用元素符号表示)。
⑸画出⑧的氢化物的电子式____________。
三、选考题(本题包括《化学与生活》和《化学反应原理》两个模块,每个模块 15 分;请任意选择其中一
个模块做答,用 2B 铅笔在答题卡上把所选题目对应题号右方的方框涂黑。)
19.《化学与生活》模块(15 分)
(1)低血糖症发作时,喝葡萄糖水可快速见效。葡萄糖作为营养剂供给人体能量,在体内发生的主要反应
是_____(填字母)。
A.加成反应
B.取代反应
C.氧化反应
D.聚合反应
(2)下列食品添加剂与类别对应错误的是_____(填字母)。
A.着色剂——氯化钠
B.营养强化剂——赖氨酸
C.调味剂——食醋
D.防腐剂——苯甲酸钠
(3)生活中常用药品很多,如碘酒、麻黄碱、青霉素、阿司匹林,其中属于抗生素的是_______________,
属于国际奥委会严格禁用的兴奋剂的是_______________。
(4)保持洁净安全的生存环境已成为全人类的共识。在二氧化碳、二氧化硫、氟氯烃中,引起温室效应的
主要是_________。
20.《化学反应原理》模块(15 分)
(1)下列现象与电化学腐蚀无关的是________________(填字母)。
A.黄铜(铜锌合金)制作的铜锣不易产生铜绿
B.生铁比软铁芯(几乎是纯铁)容易生锈
C.铁质器件附有铜质配件,在接触处易生锈
D.银质奖牌久置后表面变暗
(2)高炉炼铁过程中发生的主要反应是:
Fe2O3(s) + 3CO(g)
2Fe(s) + 3CO2(g)
ΔH<0
欲提高此反应中 CO 的平衡转化率,可采取的措施是____________(填字母)。
A.减少 Fe 的量
B.增加 Fe2O3 的量
�
C.移出部分 CO2
D.提高反应温度
(3)硝酸铵是农业上常用的化肥之一,其水溶液显___(填“酸性”、“中性”或“碱性”),溶液中 c(NO3
-)___c(NH4
+)
(填“>”、“=”或“<”)。
(4)烧碱、氯气是重要的化工原料,工业上常用电解饱和食盐水的方法生产,写出用惰性电极电解饱和食
盐水的化学方程式________________________________。
参考答案及评分标准
1B 2A 3B 4B 5D 6B 7C 8D 9C 10D 11D 12A 13C 14A 15C
16.(8 分)
⑴I2(1 分)
不是(1 分)
⑵c(2 分)
液体分层,下层液体呈紫红色(2 分)
⑶溶液变蓝(2 分)
17.(7 分)
⑴分液漏斗(2 分) Na2SO3 + H2SO4(浓) = Na2SO4 + SO2↑+ H2O(2 分)
⑵溶液红色褪去(1 分) 还原(1 分)
⑶NaOH(1 分)
18.(10 分)
⑴O
⑵Al(OH)3 + NaOH =NaAlO2 + 2H2O
⑶
⑷S>Cl
⑸
(各 2 分)
19.(15 分)
⑴C(4 分)
⑵A(4 分)
⑶青霉素(2 分)
麻黄碱(2 分)
�
⑷二氧化碳(或答“CO2”也给分)
(3 分)
20.(15 分)
⑴D(4 分)
⑵C(4 分)
⑶酸性(2 分)
>(2 分)
⑷2NaCl + 2H2O
2NaOH + H2↑+ Cl2↑(3 分)
�













 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc