2022 年四川省巴中市中考化学真题及答案
一、单项选择题(本大题共 30 个小题,每小题 2 分,共 60 分)
1. 以下巴中特产制作过程中涉及到化学变化的是
A. 制作腊肉时将成品切块包装
B. 酿造白酒的发酵过程
C. 制作中草药时晾干水分
D. 制作豆腐时用纱布滤浆
【答案】B
【解析】
【详解】A、制作腊肉时将成品切块包装的过程中,只是改变了物质的形状,没有新物质生
成,属于物理变化,不属于化学变化,故不符合题意;
B、酿造白酒的发酵过程,有新物质生成,属于化学变化,故符合题意;
C、制作中草药时晾干水分的过程中,只是改变了草药中水的形态,没有新物质生成,属于
物理变化,不是化学变化,故不符合题意;
D、制作豆腐时用纱布滤浆的过程中,只是将豆腐与滤浆分离,没有新物质生成,属于物理
变化,不属于化学变化,故不符合题意。
故选 B。
2. 下列食物中蛋白质含量最高的是
B. 西红柿
C. 大豆
D. 菜籽油
A. 大米
【答案】C
【解析】
【详解】A、大米中主要含有的是糖,故 A 不符合题意;
B、西红柿中主要含有维生素,故 B 不符合题意;
C、大豆中主要含有蛋白质,故 C 符合题意;
D、菜籽油中主要含有油脂,故 D 不符合题意;
故选 C。
3. 为了推进垃圾分类工作,把生活垃圾按图示进行科学分类处理,实行“定时、定点”投
放。手机废旧电池属于
学科 网(北 京)股 份有限 公司
�
A.
可回收物
B.
其他垃圾
C.
有害垃圾
D.
厨余垃圾
【答案】C
【解析】
【详解】A、可回收物一般包括纸张,金属、玻璃等,不包括废旧电池,不符合题意;
B、其他垃圾包括餐巾纸、卫生间用纸、尿不湿、拖把、抹布、一次性筷子等,不包括废旧
电池,不符合题意;
C、有害垃圾指对人体健康或者自然环境造成直接或潜在危害的生活废弃物。常见的有害垃
圾包括废灯管、废油漆、杀虫剂、废弃化妆品、过期药品、废电池等,包括废旧电池,符合
题意;
D、厨余垃圾包括菜叶、瓜果皮、骨鱼刺、过期食品等,不包括废旧电池,不符合题意;
故选:C。
4. 为了防止天然气漏造成危险,可在家中安装报警器,如图安装位置最合理的是
学科 网(北 京)股 份有限 公司
�
A. a 处
C. c 处
【答案】A
【解析】
B. b 处
D. 以上各处都可以
【详解】A. 天然气的主要成分是甲烷,甲烷的密度比空气的密度小,故报警器安装最合理
位置是最上面 a 处,故 A 正确;
B. b 处高度低于一般成年人身高,不容易察觉天然气泄漏,故 B 错误;
C. c 处高度更低,更不容易察觉天然气泄漏,故 C 错误;
D. 根据以上分析,a 处最合理,故 D 错误。
故选:A。
5. 下列说法错误的是
A. 家中使用的保鲜膜属于有机合成材料
B. 自制简易净水器中活性炭的主要作用是杀菌、消毒
C. “大漠孤烟直”中的“烟,是固体小颗粒悬浮在空气中形成的现象
D. 车用乙醇汽油中乙醇属于可再生能源
【答案】B
【解析】
【详解】A、家中使用的保鲜膜的成分是聚乙烯,是一种塑料,属于有机合成材料,选项正
确;
B、活性炭具有吸附性,能够吸附色素和异味,即自制简易净水器中活性炭的主要作用是吸
附色素和异味,选项错误;
C、烟是固体小颗粒悬浮在空气中形成的现象,选项正确;
D、乙醇能够通过粮食发酵生成,所以车用乙醇汽油中乙醇属于可再生能源,选项正确,故
选 B。
6. 下列判断正确的是
A. 含氧元素的化合物一定是氧化物
B. 生成盐和水的反应都是中和反应
C. 只含一种元素的物质一定是单质
D. 含碳元素的化合物不一定是有机物
【答案】D
学科 网(北 京)股 份有限 公司
�
【解析】
【详解】A.含氧元素的化合物不一定是氧化物,如
KMnO 、
4
KClO 都不是氧化物;氧化
3
物是由两种元素组成,其中一种元素是氧元素的化合物,如 2CO 、 3
Fe O 是氧化物,此选
4
项错误;
B.生成盐和水的反应不一定是中和反应,如酸和金属氧化物的反应生成盐和水,碱和非金属
氧化物反应生成盐和水都不是中和反应,此选项错误;
C.只含一种元素的物质不一定是单质,如 2
3
O O、 的混合物只含一种元素;而只含一种元素
的纯净物是单质,此选项错误;
D.含碳元素的化合物不一定是有机物,如 2CO 、CO 、碳酸盐等都含碳元素但是是无机物,
此选项正确;
故选 D
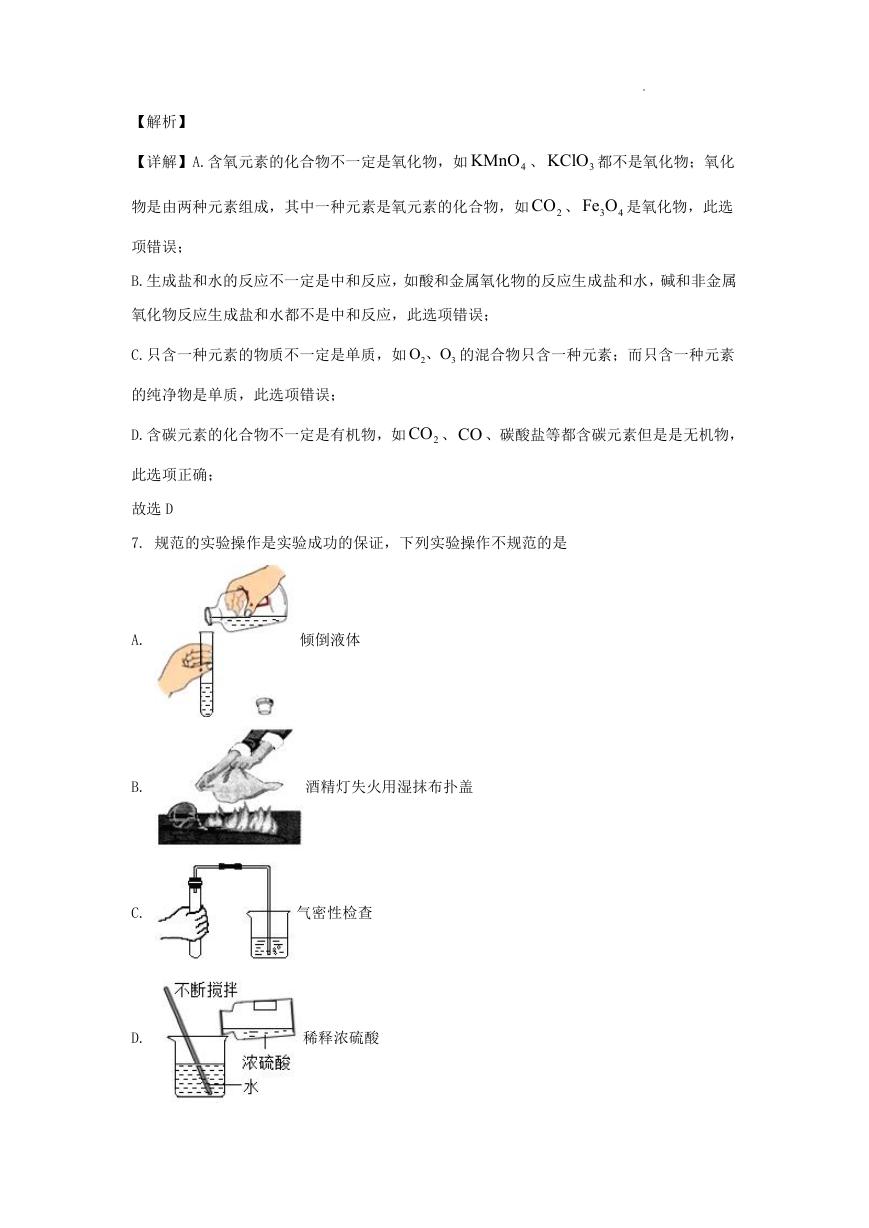
7. 规范的实验操作是实验成功的保证,下列实验操作不规范的是
倾倒液体
酒精灯失火用湿抹布扑盖
气密性检查
稀释浓硫酸
A.
B.
C.
D.
学科 网(北 京)股 份有限 公司
�
【答案】A
【解析】
【详解】A、倾倒液体时,要瓶塞倒放在桌上,标签对着手心(防止标签被腐蚀),瓶口要紧
挨着试管口,试管倾斜,使液体缓缓地倒入试管,符合题意;
B、酒精灯不慎打翻起火,用湿抹布扑盖,采用隔离氧气的方法进行灭火,不符合题意;
C、将导管的下端浸入水中,用手紧握试管,若导管口有气泡冒出,松开手后,水进入到导
管中形成一段水柱,证明装置气密性良好,不符合题意;
D、稀释浓硫酸步骤为:打开浓硫酸的瓶盖,缓慢把浓硫酸倒入装有水的烧杯中,在缓慢倒
入浓硫酸的同时,用玻璃杯不断进行搅拌, 使稀释时放出的热量进行扩散,不符合题意。
故选 A。
8. “丹砂烧之成水银”中的“丹砂”指的是硫化汞。该反应的微观示意图如图,有关说法
正确的是
A. “
”代表非金属单质汞
B. 反应前后的原子种类发生了改变
C. 此反应属于置换反应
D. 反应前后各元素的化合价都不变
【答案】C
【解析】
【详解】A. 汞是金属单质,错误;
B. 化学反应前后原子得种类、数目、质量一定不变,错误;
C. 该反应是单质和化合物反应生成单质和化合物的反应,是置换反应,正确;
D. 单质中元素的化合价为 0,化合物中元素的化合价不为 0,反应中有单质参与反应,有单
质生成,所以反应前后一定有元素的化合价发生改变,错误。
故选:C。
9. 如图为 KNO3、NaCl 两种物质的溶解度曲线,下列说法正确的是
学科 网(北 京)股 份有限 公司
�
A. a1℃时,向 100g 水中加入 20gKNO3,充分溶解后所得溶液是饱和溶液
B. KNO3 和 NaCl 的溶解度相等
C. 当 KNO3 中含有少量 NaCl 时,可以用蒸发结晶的方法提纯 KNO3
D. 将 a2℃时等质量的 NaCl 与 KNO3 的饱和溶液降温到 a1℃,所得溶液中溶质质量 NaCl 大于
KNO3
【答案】D
【解析】
【详解】A. a1℃时,硝酸钾溶解度大于 20g,所以,向 100g 水中加入 20gKNO3,充分溶解后
所得溶液是不饱和溶液,错误。
B. 未指明温度,不能比较两种物质的溶解度。错误。
C. 硝酸钾和氯化钠的溶解度均随温度的升高而增大,硝酸钾的溶解度随温度的变化较大,
氯化钠的溶解度随温度的变化较小,所以当 KNO3 中含有少量 NaCl 时,可以用降温结晶的方
法提纯 KNO3,错误。
D. 硝酸钾溶解度随温度的降低减少较大,将 a2℃时等质量的 NaCl 与 KNO3 的饱和溶液降温
到 a1℃,硝酸钾析出晶体较大,硝酸钾溶液质量减少较大,所以所得溶液中溶质质量 NaCl
大于 KNO3,正确。
故选:D。
10. 常温下取稀盐酸与氢氧化钠反应后的溶液进行实验,下列能说明稀盐酸和氢氧化钠恰好
完全反应的是
A. 加入碳酸钙粉末,有气泡产生
B. 加入 AgNO3 溶液,有白色沉淀产生
C. 加入酚酞溶液,溶液显红色
D. 测定溶液的 pH,pH=7
【答案】D
学科 网(北 京)股 份有限 公司
�
【解析】
【详解】A、向稀盐酸与氢氧化钠反应后的溶液中加入碳酸钙粉末,有气泡产生,说明稀盐
酸有剩余,故 A 不符合题意;
B、稀盐酸与氢氧化钠反应生成氯化钠和水,稀盐酸中的氯化氢、反应后生成的氯化钠与 AgNO3
反应,都会生成氯化银白色沉淀,故 B 不符合题意;
C、稀盐酸与氢氧化钠恰好完全反应后的溶液是氯化钠溶液,氯化钠溶液呈中性,加入酚酞
溶液,溶液为无色,故 C 不符合题意;
D、稀盐酸与氢氧化钠恰好完全反应后的溶液是氯化钠溶液,氯化钠溶液呈中性,溶液的
pH=7,故 D 符合题意。
故选 D。
11. 下列实验方案不合理的是
A. 除去 CO2 中少量的 HCl 气体,通过足量的 NaOH 溶液
B. 除去 CaO 中少量的 CaCO3,高温煅烧至质量不变
C. 鉴别 NaCl 固体和 NH4NO3 固体,加水溶解,感知温度变化
D. 鉴别羊毛线和棉线,灼烧、闻气味
【答案】A
【解析】
【详解】A 、CO2 和 HCl 气体均能与 NaOH 溶液反应,不但能把氯化氢除去,也会把二氧化碳
除去,不符合除杂原则,A 实验方案不合理。
B、CaO 不分解,CaCO3 高温煅烧生成氧化钙和二氧化碳,除去碳酸钙的同时得到氧化钙,符
合除杂原则,B 实验方案合理。
C、氯化钠加水溶解温度基本不变,硝酸铵加水溶解温度明显降低,C 实验方案合理。
D、羊毛线灼烧后产生羽毛烧焦气味,棉线灼烧后不会产生羽毛烧焦气味,D 实验方案合理。
综上所述:选择 A。
12. 取少量实验室制取 CO2 后的废液,向其中加入紫色石蕊溶液变成红色。现另取一定质量
的废液于烧杯中,向其中逐渐加入碳酸钠粉末,如图:横坐标表示加入的碳酸钠粉末的质量,
根据图像判断,纵坐标可能表示
学科 网(北 京)股 份有限 公司
�
A. 溶液中溶剂的质量
C. 溶液的 pH
【答案】B
【解析】
B. 烧杯中固体的质量
D. 溶液中溶质的质量
【分析】实验室用碳酸钙和稀盐酸反应制取二氧化碳,取少量实验室制取二氧化碳后的废液,
向其中加入紫色石蕊溶液变成红色。说明溶液显酸性,则说明盐酸有剩余,溶液中此时含有
剩余的盐酸和生成的氯化钙,据此解题。
【详解】A、根据分析,向废液中逐渐加入碳酸钠粉末,碳酸钠与盐酸反应生成氯化钠、水
和二氧化碳,则溶液中的溶剂逐渐增多,由反应前溶液中有溶剂即曲线的起点不为 0,在纵
坐标上,如图所示,选项错误;
B、根据分析,向废液中逐渐加入碳酸钠粉末,碳酸钠与盐酸反应生成氯化钠、水和二氧化
碳,此时烧杯内没有固体,因此曲线起点不为 0,随着盐酸完全反应后碳酸钠会与废液中的
氯化钙反应生成碳酸钙沉淀和氯化钠,此时烧杯内固体增多,氯化钙完全反应后,再加入碳
酸钠固体不再增多,随之碳酸钠不断溶解达到饱和后再加入碳酸钠则无法再继续溶解,此时
烧杯内固体质量再次增多,如图所示,纵坐标表示烧杯中固体的质量与曲线符合,选项正确;
C、根据分析,加入碳酸钠之前溶液显酸性 pH<7,向废液中逐渐加入碳酸钠粉末,碳酸钠与
盐酸反应生成氯化钠、水和二氧化碳,酸性减弱恰好完全反应时 pH=7,再加入碳酸钠和氯
化钙反应至其完全反应 pH=7,再加入碳酸钠,溶于水由于碳酸钠溶液显碱性,此时 pH>7,
如图所示,纵坐标与曲线不符合,选项错误;
D、根据分析,反应前废液中含有溶质,溶质不为 0,如图所示,曲线起点在横坐标上,纵
坐标与曲线不符合,选项错误;
故选:B。
二、填空题(除标注分数外,其余每空 1 分,共 14 分)
13. 我国著名的化工专家侯德榜,为纯碱和氮肥工业的发展作出了杰出的贡献。侯氏制碱法
学科 网(北 京)股 份有限 公司
�















 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc