2014 年重庆理工大学化学综合考研真题 A 卷
一. 填空题(每题 3 分,共 15 分)
(一)有机化学部分
1.路易斯酸碱理论的实质是
_____________________________________________________ 。
2. 构象异构是指
______________________________________________________________ 。
3. 由于____________________________,使醇表现酸性。
4.油脂的主要成份是__________________________________________________________。
5.天然存在的核酸有___________________和___________________两大类。
二、选择题(共 30 分)
1、单选题(每题 3 分,共 15 分)
(1)糖原和支链淀粉的不同点仅在于( )
A 组成单糖的单位
B 分支的多少
C 与碘反应的颜色
D 苷键的形成
(2)人体中不能合成的脂肪酸是(
)
A 亚油酸 B 月桂酸 C 软脂酸
D 硬脂酸
(3)维持蛋白质α-螺旋结构的主要化学键是(
)
A 肽键
B 二硫键
C 酯键
D 氢键
(4)下列化合物在低温下与亚硝酸反应生成重氮盐的是哪一个(
)
A
B
�
C
D
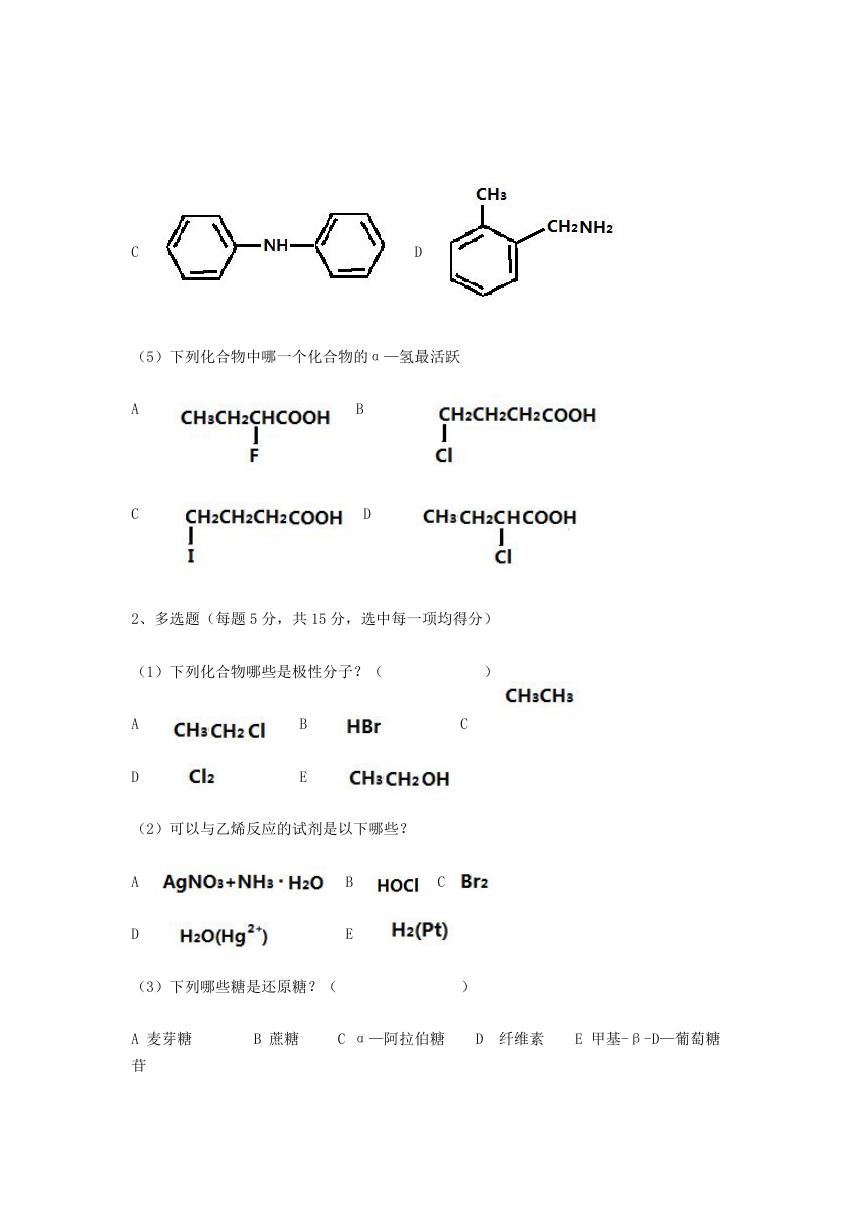
(5)下列化合物中哪一个化合物的α—氢最活跃
A
C
B
D
2、多选题(每题 5 分,共 15 分,选中每一项均得分)
(1)下列化合物哪些是极性分子?(
)
A
D
B
E
(2)可以与乙烯反应的试剂是以下哪些?
A
D
B
E
C
C
(3)下列哪些糖是还原糖?(
)
A 麦芽糖
B 蔗糖
C α—阿拉伯糖
D 纤维素
E 甲基-β-D—葡萄糖
苷
�
三、机理题((每题 5 分,共 15 分)
1、为什么酚中的 C-O 键比醇中的 C-O 键键长要短?
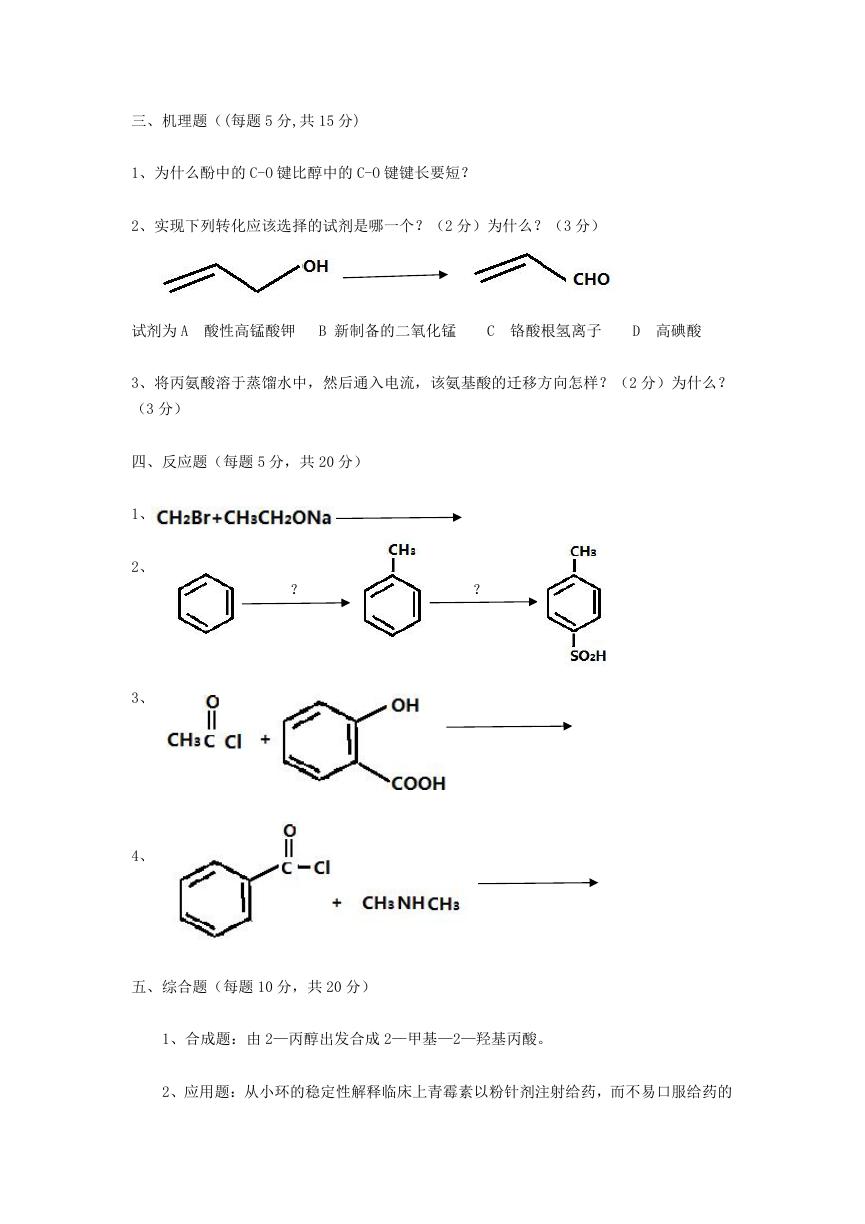
2、实现下列转化应该选择的试剂是哪一个?(2 分)为什么?(3 分)
试剂为 A 酸性高锰酸钾 B 新制备的二氧化锰
C 铬酸根氢离子
D 高碘酸
3、将丙氨酸溶于蒸馏水中,然后通入电流,该氨基酸的迁移方向怎样?(2 分)为什么?
(3 分)
四、反应题(每题 5 分,共 20 分)
?
?
1、
2、
3、
4、
五、综合题(每题 10 分,共 20 分)
1、合成题:由 2—丙醇出发合成 2—甲基—2—羟基丙酸。
2、应用题:从小环的稳定性解释临床上青霉素以粉针剂注射给药,而不易口服给药的
�
原因。
(二)无机化学部分
一、填空题(共 5 题,每题 2 分,共 10 分)
1、热力学第一定律的数学表达式是ΔU=Q+W,其实质是____________________。
2、所谓的原子轨道是指____________________。
3、向含有的 AgCl 沉淀的溶液中加水,AgCl 的溶解度_______,容度积常数_______。
4、已知①A+B→C+D,ΔrHθ
m,1=-40kJ·mol-1;②2C+2D→E,ΔrHθ
m,2=60kJ·mol-1,③ E→2A+2B
的ΔrHθ
m,3 等于____________________。
5、25℃条件下,10-8mol/L 的 NaOH 溶液的 pH 值为_____________。
二、选择题(共 5 题,每题 3 分,共 15 分)
1、在相同的温度下,将等质量的 O2 和 N2 分别充入体积相等的两个容器中,下列有关两种
气体的说法中,正确的是________。
(A)N2 分子碰撞器壁的频率小于 O2 分子
(B)N2 的压力大于 O2 的压力
(C)O2 分子的平均动能大于 N2 分子的平均动能
(D)O2 和 N2 分子的平均速度分布图是相同的
2、化学平衡是有条件的,相对的,_______能缩短反应达到平衡的时间,但不能使化学平
衡移动。
(A)浓度 (B)压力 (C)温度 (D)催化剂
3、按照软硬酸碱分类,下列离子中最软的酸是________。
(A)Cu2+
(B)K+
(C)Cu+
(D)Co2+
4、对于燃料电池:Pt·C4H10(g)┃ZrO2(s) ┃O2·Pt,其放电时,负电极反应为________。
(A)O2+H2O+4e→4OH-
(B)C4H10+13O2-—26e→4CO2+5H2O
(C)C4H10+8H2O—26e→4CO2+26H+
(D)13/2O2+26e→13 O2-
5、下列各组物质可能共存的是________。
(A)Cu2+,Fe2+,Sn4+,Ag
(B)Cu2+,Ag +,Fe2+,Fe
(C)Fe 3+,Fe,Cu2+,Ag
(D)Fe 3+,I-,Sn4+,Fe2+
�
三、问答题(共 5 题,每题 5 分,共 25 分)
1、氧气钢瓶的容积为 40.0L,压力为 10.1MPa,温度为 27℃。计算钢瓶中氧气的质量。
2、通常温度的改变则会影响化学反应速率的快慢。温度影响反应速率的机理是什么?
3、杂化轨道理论的基本要点有那些?
4、试用离子极化理论讨论 Cu2+和 Na+虽然半径相近,但是 CuCl 的水中溶解度比 NaCl 小的多
的原因。
5、阿司匹林的有效成分是乙酰水杨酸 HC9H7O4,其 Ka
杨酸,最后稀释至 65mL。计算该溶液的 pH。
θ=3.0×10-4,在水中溶解 0.65g 乙酰水
�








 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc