2022 年山东高考化学试题及答案
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需
改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。
写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1
C 12
O 16
S 32
Cl 35.5
Ti 48
Co 59
一、选择题:本题共 10 小题,每小题 2 分,共 20 分。每小题只有一个选项符合题目要求。
1.古医典富载化学知识,下述之物见其氧化性者为(
)
A.金( Au ):“虽被火亦未熟”
B.石灰( CaO ):“以水沃之,即热蒸而解”
C.石硫黄(S):“能化……银、铜、铁,奇物”
D.石钟乳(
CaCO ):“色黄,以苦酒(醋)洗刷则白”
3
2.下列试剂实验室保存方法错误的是(
)
A.浓硝酸保存在棕色细口瓶中
B.氢氧化钠固体保存在广口塑料瓶中
C.四氯化碳保存在广口塑料瓶中
D.高锰酸钾固体保存在棕色广口瓶中
3 . 13
16
8
8 O 、 15
3
; 16
8
2
8 O 的 半 衰 期 很 短 , 自 然 界 中 不 能 稳 定 存 在 。 人 工 合 成 反 应 如 下 :
13
8
。下列说法正确的是(
O He
O He
O X
a
b
15
8
O
m
n
Y
3
2
)
A.X 的中子数为 2
B.X、Y 互为同位素
C. 13
8 O 、 15
8 O 可用作示踪原子研究化学反应历程
D.自然界不存在 13
8
2O 、 15
8
2O 分子是因其化学键不稳定
�
4.下列高分子材料制备方法正确的是(
)
A.聚乳酸( [
O
||
O CH C ]
|
3CH
)由乳酸经加聚反应制备
n
B.聚四氟乙烯( [
CF CF ]
2
2
n )由四氟乙烯经加聚反应制备
C.尼龙 66 ( [
NH CH
6
2
O
||
NH C CH
O
||
C ]
4
2
n )由己胺和己酸经缩聚反应制备
D.聚乙烯醇(
[
CH
2
]CH
|
OH
n
)由聚乙酸乙烯酯(
[
CH
2
]CH
n
|
OCOCH
)经消去反应制备
3
5.AlN 、GaN 属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在 N Al
键、 N Ga 键。下列说法错误的是(
)
A. GaN 的熔点高于 AlN
B.晶体中所有化学键均为极性键
C.晶体中所有原子均采取 3sp 杂化
D.晶体中所有原子的配位数均相同
6.实验室用基准 2
3
Na CO 配制标准溶液并标定盐酸浓度,应选甲基橙为指示剂,并以盐酸
滴定 2
Na CO 标准溶液。下列说法错误的是(
3
)
A.可用量筒量取
25.00mL Na CO 标准溶液置于锥形瓶中
2
3
B.应选用配带塑料塞的容量瓶配制 2
Na CO 标准溶液
3
C.应选用烧杯而非称量纸称量 2
Na CO 固体
3
D.达到滴定终点时溶液显橙色
7. 崖柏素具天然活性,有酚的通性,结构如图。关于 崖柏素的说法错误的是(
)
�
A.可与溴水发生取代反应
B.可与
NaHCO 溶液反应
3
C.分子中的碳原子不可能全部共平面
D.与足量 2H 加成后,产物分子中含手性碳原
子
8.实验室制备
KMnO 过程为:①高温下在熔融强碱性介质中用
4
KClO 氧化
3
K MnO ;②水溶后冷却,调溶液 pH 至弱碱性, 2
2
4
K MnO 歧化生成
KMnO 和
2MnO 制备
2MnO ;
4
4
③减压过滤,将滤液蒸发浓缩、冷却结晶,再减压过滤得
KMnO 。下列说法正确的是(
4
)
A.①中用瓷坩埚作反应器
B.①中用 NaOH 作强碱性介质
C.②中 2
K MnO 只体现氧化性
4
D.
2MnO 转化为
KMnO 的理论转化率约为 66.7%
4
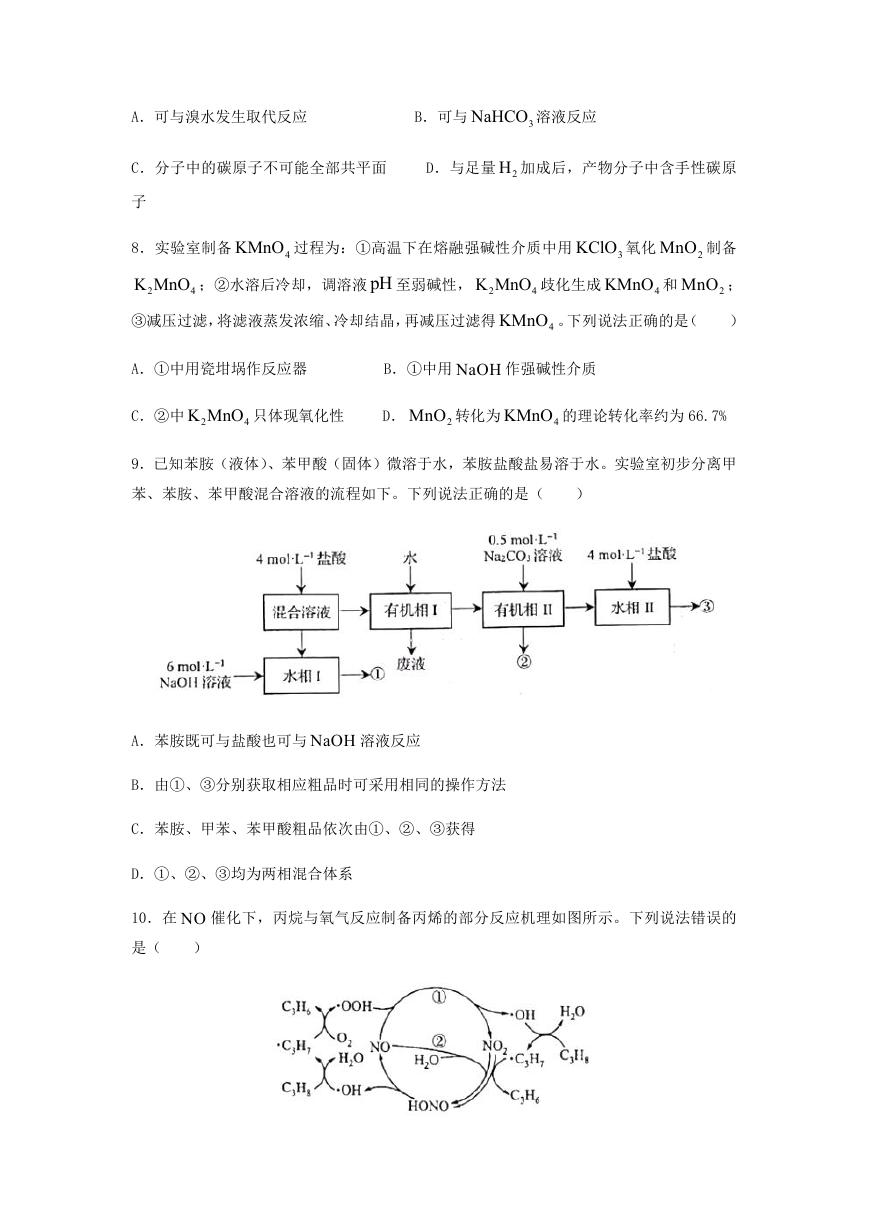
9.已知苯胺(液体)、苯甲酸(固体)微溶于水,苯胺盐酸盐易溶于水。实验室初步分离甲
苯、苯胺、苯甲酸混合溶液的流程如下。下列说法正确的是(
)
A.苯胺既可与盐酸也可与 NaOH 溶液反应
B.由①、③分别获取相应粗品时可采用相同的操作方法
C.苯胺、甲苯、苯甲酸粗品依次由①、②、③获得
D.①、②、③均为两相混合体系
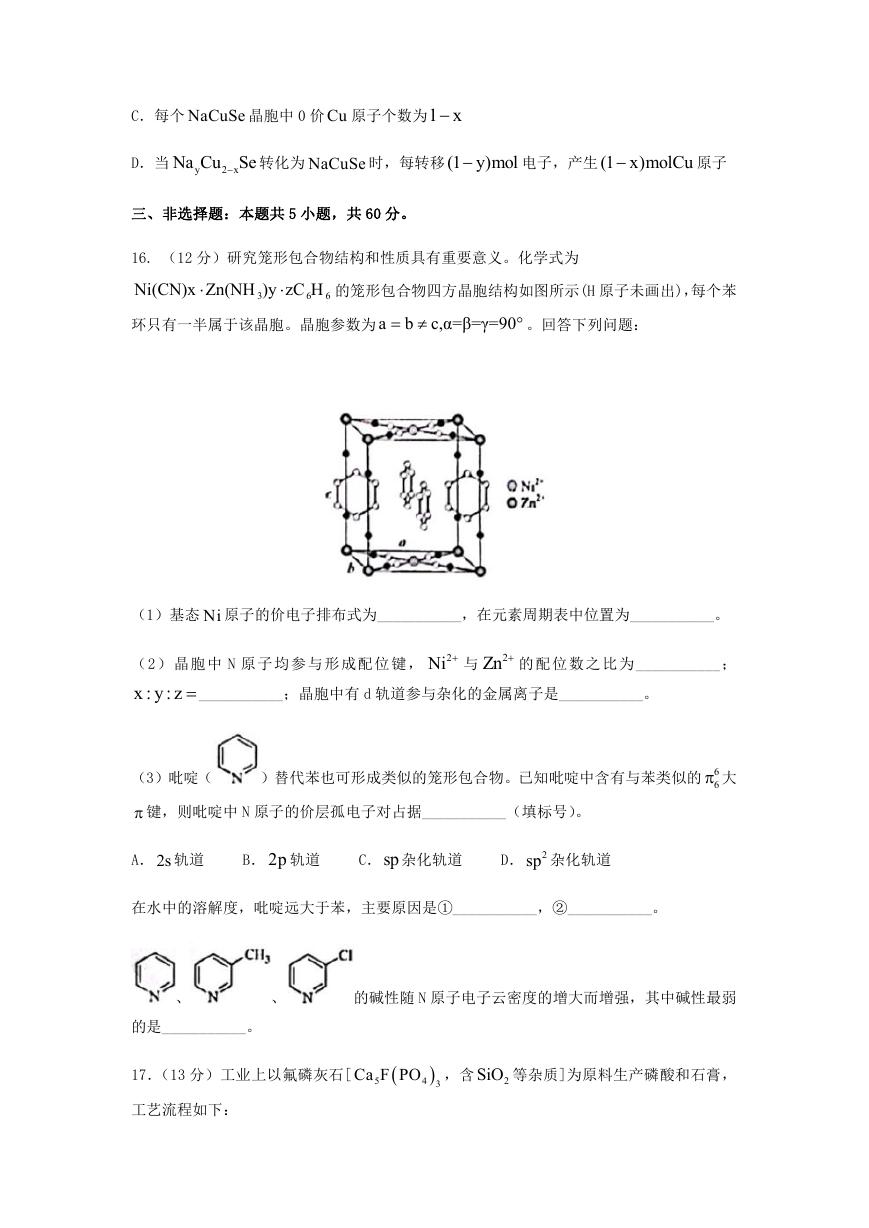
10.在 NO 催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法错误的
是(
)
�
A.含 N 分子参与的反应一定有电子转移
B.由 NO 生成 HONO 的反应历程有 2 种
C.增大 NO 的量, 3
8C H 的平衡转化率不变
D.当主要发生包含②的历程时,最终生
成的水减少
二、选择题:本题共 5 小题,每小题 4 分,共 20 分。每小题有一个或两个选项符合题目要
求,全部选对得 4 分,选对但不全的得 2 分,有选错的得 0 分。
11.某同学按图示装置进行实验,欲使瓶中少量固体粉末最终消失并得到澄清溶液。下列物
质组合不符合要求的是(
)
气体
2CO
2Cl
HCl
3NH
A
B
C
D
液体
固体粉末
饱和 2
Na CO 溶液
3
FeCl 溶液
2
Cu NO 溶液
3 2
2H O
CaCO
3
Fe
Cu
AgCl
12.高压氢还原法可直接从溶液中提取金属粉。以硫化铜精矿(含 Zn 、 Fe 元素的杂质)
为主要原料制备 Cu 粉的工艺流程如下,可能用到的数据见下表。
�
Fe(OH)
3
Cu(OH)
2
Zn(OH)
2
开始沉淀 pH
沉淀完全 pH
1.9
3.2
4.2
6.7
6.2
8.2
下列说法错误的是(
)
A.固体 X 主要成分是
Fe(OH) 和 S;金属 M 为 Zn
3
B.浸取时,增大 2O 压强可促进金属离子浸出
C.中和调 pH 的范围为 3.2~4.2
D.还原时,增大溶液酸度有利于 Cu 的生成
13.设计如图装置回收金属钴。保持细菌所在环境 pH 稳定,借助其降解乙酸盐生成 2CO ,
LiCoO (s) 转化为 2Co ,工作时保持厌氧环境,并定时将乙
将废旧锂离子电池的正极材料
2
室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法正确的是
(
)
A.装置工作时,甲室溶液 pH 逐渐增大
B.装置工作一段时间后,乙室应补充盐酸
C.乙室电极反应式为
LiCoO 2H O e
2
2
Li
Co
2
4OH
D.若甲室 2Co 减少 200mg ,乙室 2Co 增加 300mg ,则此时已进行过溶液转移
14.工业上以
SrSO (s) 为原料生产
4
SrCO (s) ,对其工艺条件进行研究。现有含
3
SrCO (s)
3
�
的
1
0.1mol L
、
1.0mol L Na CO
1
2
溶 液 , 含
3
SrSO (s) 的
4
1
0.1mol L
、
1.0mol L Na SO
1
2
溶液。在一定 pH 范围内,四种溶液中
4
lg c Sr
2
1
/ mol L
随 pH 的
变化关系如图所示。下列说法错误的是(
)
A.反应
SrSO (s) CO
4
2
3
SrCO (s) SO
3
2
4
的平衡常数
K
sp
K SrSO
4
K SrCO
sp
3
B. a
6.5
C.曲线④代表含
SrCO (s) 的
3
1.0mol L Na CO
1
2
溶液的变化曲线
3
D.对含
SrSO (s) 且 2
Na SO 和 2
Na CO 初始浓度均为
4
4
3
1
1.0mol L
的混合溶液,pH 7.7
时才发生沉淀转化
15. 2 xCu Se 是一种钠离子电池正极材料,充放电过程中正极材料立方晶胞(示意图)的组
成变化如图所示,晶胞内未标出因放电产生的 0 价 Cu 原子。下列说法正确的是(
)
A.每个 2 xCu Se 晶胞中 2Cu 个数为 x
B.每个 2Na Se 晶胞完全转化为 2 xCu Se 晶胞,转移电子数为 8
�
C.每个 NaCuSe 晶胞中 0 价Cu 原子个数为1 x
D.当
yNa Cu Se 转化为 NaCuSe 时,每转移 (1 y)mol
2 x
电子,产生 (1 x)molCu
原子
三、非选择题:本题共 5 小题,共 60 分。
16. (12 分)研究笼形包合物结构和性质具有重要意义。化学式为
Ni(CN)x Zn(NH )y zC H
环只有一半属于该晶胞。晶胞参数为 a
3
6
6
的笼形包合物四方晶胞结构如图所示(H 原子未画出),每个苯
b
c,α=β=γ=90
。回答下列问题:
(1)基态 Ni 原子的价电子排布式为___________,在元素周期表中位置为___________。
(2) 晶胞 中 N 原 子均 参 与形 成配 位 键, 2Ni 与 2Zn 的 配位 数 之比 为 ___________;
x : y: z ___________;晶胞中有 d 轨道参与杂化的金属离子是___________。
(3)吡啶(
)替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的 6
6 大
键,则吡啶中 N 原子的价层孤电子对占据___________(填标号)。
A. 2s 轨道
B. 2p 轨道
C.sp 杂化轨道
D. 2sp 杂化轨道
在水中的溶解度,吡啶远大于苯,主要原因是①___________,②___________。
、
、
的碱性随 N 原子电子云密度的增大而增强,其中碱性最弱
的是___________。
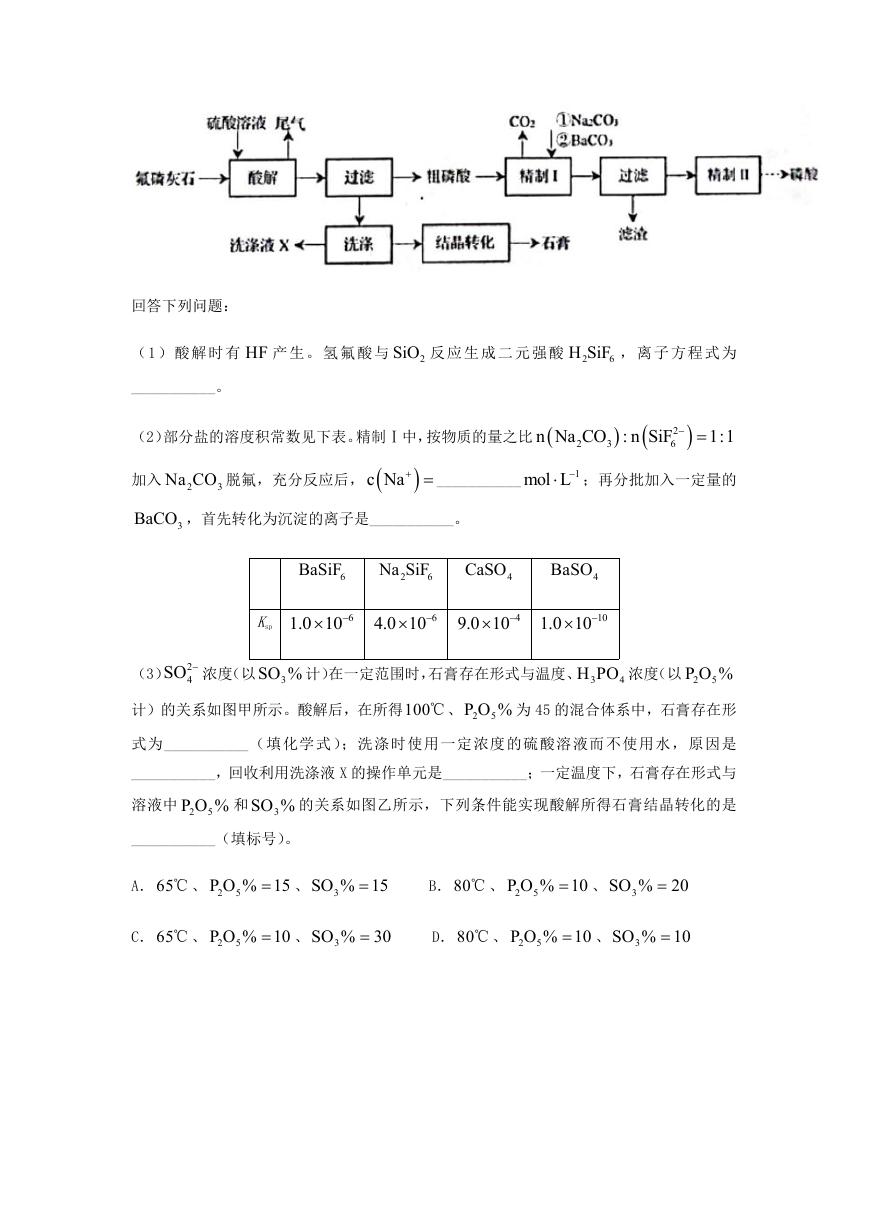
17.(13 分)工业上以氟磷灰石[
工艺流程如下:
Ca F PO ,含 2SiO 等杂质]为原料生产磷酸和石膏,
5
4 3
�
回答下列问题:
( 1 ) 酸 解 时 有 HF 产 生 。 氢 氟 酸 与
___________。
2SiO 反 应 生 成 二 元 强 酸 2
H SiF , 离 子 方 程 式 为
6
(2)部分盐的溶度积常数见下表。精制Ⅰ中,按物质的量之比
n Na CO : n SiF
6
2
3
2
1:1
Na CO 脱氟,充分反应后,
加入 2
3
c Na ___________
1
mol L
;再分批加入一定量的
BaCO ,首先转化为沉淀的离子是___________。
3
BaSiF
6
Na SiF
6
2
CaSO
4
BaSO
4
Ksp
6
1.0 10
6
4.0 10
4
9.0 10
10
1.0 10
(3) 2
4SO 浓度(以 3SO % 计)在一定范围时,石膏存在形式与温度、 3
计)的关系如图甲所示。酸解后,在所得100℃、 2
5P O %
5P O % 为 45 的混合体系中,石膏存在形
H PO 浓度(以 2
4
式为___________(填化学式);洗涤时使用一定浓度的硫酸溶液而不使用水,原因是
___________,回收利用洗涤液 X 的操作单元是___________;一定温度下,石膏存在形式与
5P O % 和 3SO % 的关系如图乙所示,下列条件能实现酸解所得石膏结晶转化的是
溶液中 2
___________(填标号)。
A. 65℃ 、 2
5P O % 15 、 3SO % 15
B.80℃ 、 2
5P O % 10 、 3SO % 20
C. 65℃ 、 2
5P O % 10 、 3SO % 30
D.80℃ 、 2
5P O % 10 、 3SO % 10
�













 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc