2004 年黑龙江省中考化学真题及答案(非课改区)
(满分 100 分,时间 90 分钟)
一、选择题(本题共 20 小题,每小题 2 分,共 40 分。1~15 小题每小题只有一个正确选
项,16~20 小题每小题有一个或两个正确选项,请将正确选项的序号填入括号内)
1.日常生活中经常遇到下列变化,其中属于化学变化的是
C.水受热沸腾
)
B.家庭自制冰块
(
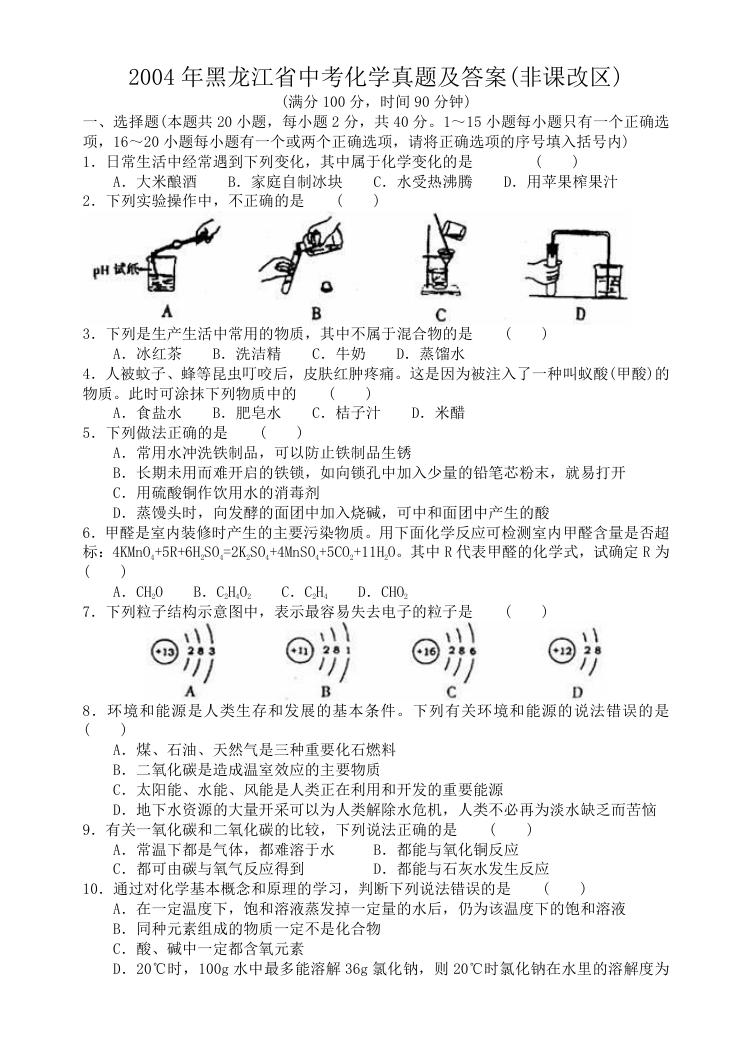
2.下列实验操作中,不正确的是
D.用苹果榨果汁
A.大米酿酒
(
)
3.下列是生产生活中常用的物质,其中不属于混合物的是
(
)
A.冰红茶
B.洗洁精
C.牛奶
D.蒸馏水
4.人被蚊子、蜂等昆虫叮咬后,皮肤红肿疼痛。这是因为被注入了一种叫蚁酸(甲酸)的
物质。此时可涂抹下列物质中的
(
)
A.食盐水
B.肥皂水
C.桔子汁
D.米醋
5.下列做法正确的是
(
)
A.常用水冲洗铁制品,可以防止铁制品生锈
B.长期未用而难开启的铁锁,如向锁孔中加入少量的铅笔芯粉末,就易打开
C.用硫酸铜作饮用水的消毒剂
D.蒸馒头时,向发酵的面团中加入烧碱,可中和面团中产生的酸
6.甲醛是室内装修时产生的主要污染物质。用下面化学反应可检测室内甲醛含量是否超
标:4KMnO4+5R+6H2SO4=2K2SO4+4MnSO4+5CO2+11H2O。其中 R 代表甲醛的化学式,试确定 R 为
(
)
A.CH2O
B.C2H4O2
C.C2H4
D.CHO2
7.下列粒子结构示意图中,表示最容易失去电子的粒子是
(
)
8.环境和能源是人类生存和发展的基本条件。下列有关环境和能源的说法错误的是
(
)
A.煤、石油、天然气是三种重要化石燃料
B.二氧化碳是造成温室效应的主要物质
C.太阳能、水能、风能是人类正在利用和开发的重要能源
D.地下水资源的大量开采可以为人类解除水危机,人类不必再为淡水缺乏而苦恼
9.有关一氧化碳和二氧化碳的比较,下列说法正确的是
(
)
A.常温下都是气体,都难溶于水
C.都可由碳与氧气反应得到
B.都能与氧化铜反应
D.都能与石灰水发生反应
(
10.通过对化学基本概念和原理的学习,判断下列说法错误的是
)
A.在一定温度下,饱和溶液蒸发掉一定量的水后,仍为该温度下的饱和溶液
B.同种元素组成的物质一定不是化合物
C.酸、碱中一定都含氧元素
D.20℃时,100g 水中最多能溶解 36g 氯化钠,则 20℃时氯化钠在水里的溶解度为
�
36g
11.下列物质的用途中,只利用其物理性质的是
(
)
12.下列对实验现象的描述,不正确的是
(
)
A 硫粉在氧气中燃烧发出蓝紫色火焰 B 将氢氧化钙溶液与碳酸钠浓溶液混合产生白色
沉淀
C 磷在空气中燃烧产生大量的白烟 D 一氧化碳在空气中燃烧产生苍白色火焰
13.同学们喜欢的油炸食品中,含有一种叫丙烯醛(化学式 C2H4O)的有毒物质。下列有关
丙烯醛的说法正确的是
(
)
A.它是由碳、氢、氧原子构成的
C.它的相对分子质量为 56
B.它的一个分子中含有两个氢分子
D.丙烯醛中碳、氢、氧元素的质量比为 3:4:1
14.下列由实验现象得到的结论,正确的是
(
)
A.向某溶液中加入 BaCl2 溶液,生成不溶于稀 HNO3 的白色沉淀,说明该溶液中—定含
2-
SO4
B.向某固体中加入稀盐酸,有气泡产生,说明此固体一定是金属
C.氯化钠晶体不导电,说明氯化钠晶体中不含离子
D.向某溶液中滴加无色酚酞试液,酚酞试液变红色,说明该溶液显碱性
15.硫酸亚铁可用于治疗缺铁性贫血。某贫血患者每天需补充 1.12g 铁元素,则他服用
的药物中含硫酸亚铁的质量至少为
(
A.3.80g
B.6.95g
C.10g
16.下列说法正确的是
(
)
)
D.3.04g
A.空气中氧气与氮气的质量比为 l:4
B.元素的化学性质主要由原子的核电荷数决定
C.复分解反应发生的条件为:生成物中有沉淀析出或有气体放出或有水生成
D.硝酸钾是一种复合肥料
17.利用家庭生活用品可以对化学知识进行学习和探究。食盐、食醋、纯碱均为家庭厨
房中常用的物质。利用这些物质你不能完成的实验为
)
B.除去热水瓶中的水垢
(
A.检验自来水中是否含有氯离子
C.鉴别食盐和纯碱
D.制出二氧化碳气体
18.在一定温度下,向一定量的 NaCl 不饱和溶液中不断加入 NaCl 固体,并搅拌。在此
过程中,加入 NaCl 质量(n)与溶液中溶质的质量分数(m)的变化关系如下图所示,其中正
确的是
19.某同学设计了四种物质制备的实验方案。其中理论上正确,操作上可行的是
(
)
A.
Fe
点燃
OFe
2
3
稀
SOH
2
4
Fe
2
(
SO
)
34
�
溶液
Fe
Cu
MgO
NaOH
溶液
B.
C.
2
4
SOH
CuO
OH
CaCO
稀
通电
O
2
HCl
稀
2
CuSO
4
Mg
CO
CO
2
3
2
Na
D.
20.在托盘天平两边各放一只烧杯,调节
至平衡。在两只烧杯里注入相同质量、相
同质量分数的足量稀盐酸,然后分别向左
右两端烧杯中加入质量相等的 Fe 和金属
A。有气体产生时,天平指针慢慢向左偏
转(如图 1);指针偏转到一定角度后,又
慢慢向右偏转;反应结束,天平指针指向
右端(如图 2)。则天平右端加入的金属 A 可能是
溶液
3
(
)
A.Zn
B.Mg
C.Cu
D.Al
二、填空题(本题共 10 小题;每空 1 分,共 24 分)
21.化学用语是高度浓缩的符号体系,可准确、简洁地记录、表达、交流化学信息。请
用化学用语表示:
⑴2 个水分子
⑶最简单的有机化合物
;⑵3 个硫原子
;
。
。
;可以用来配制波尔多液的是
22.从①石灰石 ②活性炭 ③硫酸铜中选出适当的物质,将序号填空。可以用来吸附
有毒气体的是
;可以用来作建筑材料的
是
23.在久未开启的菜窖、枯井和深洞底部的空气中
方前,为避免危险发生,必须先做
质设计的。
24.右图是某个化学反应前、后的微观模拟图。
请根据图示回答:
的含量比较高。在进入这些地
的性
试验,这个试验是根据该气体
①该化学反应中,参加反应的 和
与
反应后生成的
各粒子间的个数比为
;
②该反应的基本反应类型为
③该反应中的生成物
25.亚硝酸钠(NaNO2)是一种食品添加剂。它虽可保持肉类鲜美.但食用过量会使人
(填“可能”或“不可能”)属于氧化物。
;
中毒。NaNO2 中氮元素的化合价为
价。
26.用两种化学方法鉴别氢气和氧气。
方法⑴
方法⑵
。
。
27.已知 5gA 与 2gB 恰好完全反应生成 3gC 和若干克 D。若制取 8gD,则需
28.欲除去下列物质中的杂质(括号内为杂质),请写出所用试剂的名称。
。
; NaNO3(NaCl)
O2(水蒸气)
gA。
29.从氯酸钾与二氧化锰混合加热完全分解后的剩余固
体中分离出氯化钾,可采取的操作步骤是:①溶解、②
过滤、③
。在以上三步操作中均需使用的一种
玻璃仪器是
30.某化学试剂厂 A、B、C、D 四个车间排放的废水中,
分别含有氢氧化钠、氯化铁、碳酸钠、盐酸中的一种。
。
�
在不加其他试剂的情况下,若控制流量,将它们排入反应池中,使其恰好完全反应,最
后可形成不污染环境的废液排入河流。已知 B 车间排放的污水显碱性,C 车间排放的污水
有颜色,反应池 1 中有气泡产生,则 A 车间排放的废水中含有
D 车间排放的废水中含有
入河流的废液中,含有的离子是
三、简答题(本题共 4 小题,31、33 小题各 3 分,32,34 小题备 4 分,共重 4 分)
31.下图是某大理石雕像分别摄于 1908 年、1969 年的两幅图片。雕像的严重腐蚀反映出
最主要的环境污染问题是什么?请就如何解决这一环境污染问题提出你的建议。(至少提
出两点)
。反应池 2 中可观察到
。
,
最后排
32.如图,这是泡沫灭火器工作时的模拟实验。请你根据所学物理、化学知识;简述其
中的工作原理和灭火原理。写出有关反应的化学方程式。
33.下图为同学经常使用的某品牌修正液包装标签上的部分文字和图片。请仔细阅读、
观察,根据此图及日常生活经验分析、推测修正液的性质。(至少答出三点)
34.某同学在家做如图所示实验:在一个玻璃容器中加入 100ml 水,向水中放入一块糖,
在容器外壁沿液面画一条水平线,过一会儿发现糖块溶解,液面比原来水平线降低了。
通过这一现象请你推测分子具有哪些性质?选择其中一点性质,重新设计一个实验进行探
究。请写出实验步骤、现象和结论。
�
四、实验题(本题共 3 小题,35 小题 2 分,36 小题 3 分,37 小题 7 分,共 12 分)
35.民族英雄林则徐领导的禁烟运动捍卫了民族的尊严。其销烟的原理是利用生石灰与
水 反 应 会
, 将 鸦 片 焚 毁 。 生 石 灰 倒 入 水 池 中 还 会 产 生
的现象。
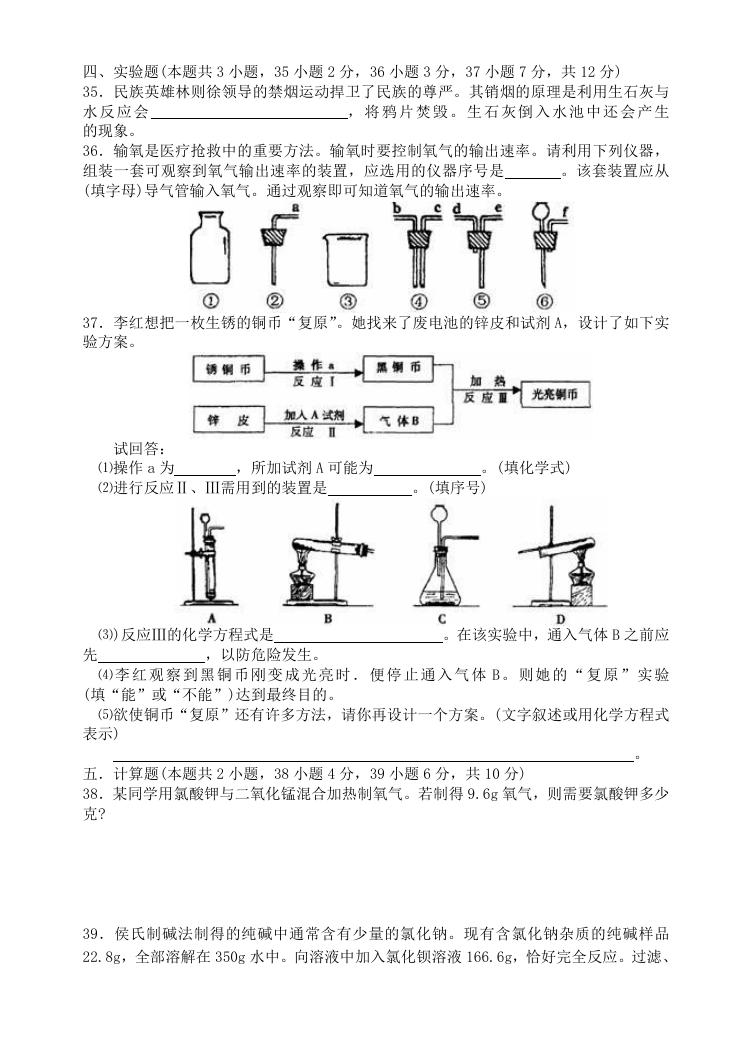
36.输氧是医疗抢救中的重要方法。输氧时要控制氧气的输出速率。请利用下列仪器,
组装一套可观察到氧气输出速率的装置,应选用的仪器序号是
。该套装置应从
(填字母)导气管输入氧气。通过观察即可知道氧气的输出速率。
37.李红想把一枚生锈的铜币“复原”。她找来了废电池的锌皮和试剂 A,设计了如下实
验方案。
试回答:
⑴操作 a 为
⑵进行反应Ⅱ、Ⅲ需用到的装置是
,所加试剂 A 可能为
。(填化学式)
。(填序号)
⑶)反应Ⅲ的化学方程式是
先
,以防危险发生。
。在该实验中,通入气体 B 之前应
⑷ 李 红 观 察 到 黑 铜 币 刚 变 成 光 亮 时 . 便 停 止 通 入 气 体 B 。 则 她 的 “ 复 原 ” 实 验
(填“能”或“不能”)达到最终目的。
⑸欲使铜币“复原”还有许多方法,请你再设计一个方案。(文字叙述或用化学方程式
表示)
五.计算题(本题共 2 小题,38 小题 4 分,39 小题 6 分,共 10 分)
38.某同学用氯酸钾与二氧化锰混合加热制氧气。若制得 9.6g 氧气,则需要氯酸钾多少
克?
。
39.侯氏制碱法制得的纯碱中通常含有少量的氯化钠。现有含氯化钠杂质的纯碱样品
22.8g,全部溶解在 350g 水中。向溶液中加入氯化钡溶液 166.6g,恰好完全反应。过滤、
�
干燥后称得沉淀质量为 39.4g。求:⑴原样品中的碳酸钠的质量;⑵最后所得滤液中溶质
的质量分数。
04 黑龙江中考化学试题参考答案
1.A
15.D
2.A
16.CD
3.D
4.B
5.B
17.A
18.A
6.A
19.BD
7.B
20.A
8.D
9.C
10.C
11.B
12.D
13.C
14.D
烧
28.浓硫酸(或固体氢氧化钠、或固体氧化钙等);硝酸根
29.蒸发(或结晶、或蒸发结晶);玻璃棒
30.HCl(或盐酸);NaOH(或氢氧化钠);产生红褐色沉淀;Na+、Cl-(或钠离子、氯离
子)
�
39.解:设原样品中碳酸钠的质量为 X,生成氯化钠的质量为 Y,
Na2CO3+BaCl2 = BaCO3↓+2NaCl
106
117
197
39.4g
Y
X
106
197
197
117
=
=
X
39.4g
39.4g
Y
X = 21.2g
Y = 23.4g
23.4g+22.8g-21.2g
22.8g+350g+166.6g-39.4g ×100% = 5%
答:略
�












 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc