2013 年贵州普通高中会考化学真题及答案
相对原子质量:H-1
C-12
N-14
O-16
Na-23
Al-27
Cl-35.5
Fe-56
Cu-64
一、选择题(本卷包括 26 小题,每小题 3 分,共 78 分。在每小题给出的四个选项中,
只有一项是符合题意的)
1.按常用危险化学品的分类,下列危险化学品与分类图形标志不一致的是(
)
A.浓硫酸—1
B.甲烷—2
C.酒精—3
D.钠—4
2.地壳中含量最多的元素是(
)
A.铁
B. 氧
C. 硅
D. 铝
3.下列物质中,既能跟盐酸反应,又能跟 NaOH 反应的是(
)
A.H2
B.SO2
C.Cu
D.Al2O3
4.下列气态氢化物中,最稳定的是(
)
A.HF
B. HCl
C. HBr
D. HI
5.下列物质在光照条件下能与 CH4 发生取代反应的是(
)
A.N2
B.酸性 KMnO4
C.Cl2
D.H2
6.与稀盐酸反应能放出 H2 的金属是(
)
A.Zn
B.Hg
C. Cu
D.Ag
7.下列属于高效、环境友好的化学电源是(
)
A.铅蓄电池
B.锌锰电池
C.镍镉电池
D.氢氧燃料电池
8.目前人类已发现几千万种物质,对物质进行分类,有利于我们的学习。对于 H2SO4 分类
不合理的是(
)
A.酸
B. 含氧酸
C. 无氧酸
D. 强酸
9.我国食盐产量居世界首位。实验室中的下列操作类似“海水晒盐”原理的是(
)
A.萃取
B.蒸发
C.过滤
D.分液
10.下列过程中,属于放热反应的是(
)
A.水的蒸发 B.Ba(OH)2·8H2O与NH4Cl的反应 C.黑火药爆炸 D.酒精挥发
11.20mL 1mol / L NaOH 溶液中,Na+ 的物质的量浓度为(
)
�
A.40g/mol
B.1.0mol/L
C.0.2mol
D.0.8g
12.某气体通入品红溶液中,溶液褪色,加热后能恢复原来颜色。该气体是(
)
A.CO2
B.O2
C.SO2
D.Cl2
13.下列溶液中,离子间能大量共存的是(
)
A.K+、Ca2+、CO3
2 一 B.Na+、H+、OH 一 C. Ag+、NO3
一、Cl 一 D.
Na+、H+、SO4
2 一
14.用于粗盐提纯时除去泥沙的实验装置是 (
)
”
A.
B.
C.
D.
15.下列属于同分异构体的是(
)
A.金刚石和石墨
B.甲烷和乙烷 C.12C 和 14C
D.正丁烷和异丁烷
16.下列反应中,反应速度最快的是(
)
A.25oC 时,镁条与 0.1mol/L 盐酸反应
B.25oC 时,镁条与 0.2mol/L 盐酸反应
C.35oC 时,镁条与 0.2mol/L 盐酸反应
D.35oC 时,镁条与 0.3mol/L 盐酸反应
17.按照金属冶炼方法的发展分析。下列金属中最晚得到广泛利用的是(
)
A.Na
B.Fe
C.Cu
D.Ag
18.人类利用能源分为三个时期:柴草时期、化石能源时期和多能源结构时期。下列能源
不属于化石能源的是(
)
A.石油
B.太阳能
C.煤
D.天然气
19.下列食物中主要成分属于酯类的是(
)
A.植物油
B.鸡蛋
C.牛奶
D.面粉
20.下列仪器在使用中不能加热的是(
)
A.试管
B.烧杯
C.容量瓶
D.圆底烧瓶
21.下列对酯化反应及其产物的理解不正确的是(
)
A.炒菜时加入少量料酒和食醋能生成少量酯增加菜品的香味 B.酯化反应属于取代反应
C.酯化反应是有限度的
D.油脂是一类易溶于水的酯
22.用 NaOH 固体配置一定物质的量浓度的 NaOH 溶液。下列操作中正确的是(
)
A.将固体氢氧化钠直接放在托盘天平左盘上称量
B.加烧杯中溶解固体氢氧化钠所得溶液,冷却到室温后转移至容量瓶中
C.定容时,如果加水超过刻度线,用胶头滴管直接吸出多余的部分
�
D.定容、摇匀后,发现液体体积低于刻度线,再补加少量蒸馏水至刻度线
23. 将盛有 15mLNO2 的试管倒置于水中,充分反应(3NO2+H2O = 2HNO3 + NO)后,试管内剩
下气体的体积为(同温同压下测定)(
)
A.0mL
B.2.5mL
C.5mL
D.7.5mL
24. 下列有机物中含有碳碳双键的是(
)
A.甲烷
B.乙烯
C.乙醇
D.乙酸
25. 下列物质不能与氢氧化钠溶液反应的是(
)
A.Cu
B.HCl
C.MgCl2
D.Al2(SO4)3
26. 某稀硫酸和稀硝酸混合溶液 200mL,平均分成甲、乙两份。向甲中逐渐加入铜粉,最多
能溶解 9.6 克,向乙中逐渐加入铁粉,产生气体的量随铜粉质量的变化如下图所示(已知:
Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O)。下列分析结果不正确的是(
)
A.原混合溶液中 NO3
一的物质的量浓度为 4mol/L
B.AB 段的反应为:Fe+2Fe3+=3Fe2+
C.C 点时,乙中溶质为 FeSO4
D.标准状况下,OA、BC 段产生的气体总体积约为 4.48L
二、选择题(本卷包括 9 个小题,每题 4 分,共计 36 分。在每小题给出的四个选项中,
只有一个或两个选项符合题意,全部选对的得 4 分,选对但不全得 2 分,有选错的得 0 分)
27.下列物质中,含有共价键的化合物是(
)
A.Na2O
B.H2O
C.NaCl
D.Ar
28. 下列有关实验操作不正确的是(
)
A.用药匙取用粉末状固体
B.向盛有浓硫酸的烧杯中加入蒸馏水进行稀释
C.用胶头滴管滴加少量液体
D.直接用手拿着镁条进行镁条在空气中的燃烧实验
29. 下列试剂能鉴别甲烷和乙烯的是(
)
A.蒸馏水
B.溴的四氯化碳溶液
C.酸性高锰酸钾溶液
D.苯
30. 向含 FeCl3、FeCl2、AlCl3、和 NaCl 的混合溶液中,加入足量 Na2O 固体,在空气中充分
搅拌,反应后再加入稍过量的盐酸,溶液中下列离子物质的量增大的是(
)
A.Na+
B.Al3+
C.Fe3+
D.Fe2+
31. H2 在 O2 中燃烧的反应为 2H2+O2=2H2O,反应前后没有发生变化的是(
)
A.元素的种类
B.分子的数目 C.物质的总能量 D.物质的总质量
32. 下列化学方程式改写成离子方程式正确的是(
)
�
A.CuSO4+Ba(OH)2=Cu(OH)2↓+BaSO4↓
Cu2++2OH 一= Cu(OH)2↓
B.CaCO3+2HCl=CaCl2+CO2↑+H2O
CO3
2 一+2H+= CO2↑+H2O
C.Ca(NO3)2+Na2CO3=CaCO3↓+2NaNO3
Ca2++ CO3
2 一= CaCO3↓
D. Ba(OH)2+H2SO4= BaSO4↓+2H2O
H++OH 一=H2O
33. 要除去 CO 气体中混有的少量 CO2,通过下列装置能达到目的的是(不考虑水蒸气)
→
→
→
→
A. 碱石灰
B.饱和食盐水
C.氢氧化钠溶液
D.浓硫酸
34. 下列有关叙述中正确的是(
)
A. 利用乙醇能使重铬酸钾变色的原理检验酒驾时,乙醇发生取代反应
B.将等体积 CH4 和 Cl2 混合,光照反应后,只生成 CH3Cl 和 HCl 且体积相等
C.淀粉、纤维素、蛋白质在一定条件下能发生水解反应
D. 乙烯和 SO2 均能使酸性高锰酸钾溶液褪色,乙烯发生加成反应,SO2 表现了漂白性
35. 某短周期元素 X 最高正价含氧酸化学式为 H2XO3,关于该元素的判断不正确的是(
)
A. 该元素可能位于第三周期 IVA 族
B.常温下 XO2 一定是气态氧化物
C.若 XO2 能与 HF 反应,那么 XO2 也能和 NaOH 反应
D.X 元素的氢化物化学式可能是 XH4
选修模块卷
请在两个模块中选择一个模块作答,务必在答题卡中填涂所选答模块的标记,两个标
记都不涂或都涂的,按选答第一模块计分。本卷共 12 小题,每小题 3 分,共计 36 分。在
每小题给出的四个选项中,只有一项是符合题意的。
《化学与生活》选修模块
36. 关于食品安全的报道中不断有①“工业甲醛”②“苏丹红”③“碘元素”④“三聚氰
胺”等化学名词出现。业内人士告诉记者,化学性污染正成为危及食品安全的一大“杀手”。
与上述化学名词相关的物质或元素,在食品添加剂中允许含有的是(
)
A.①②③
B. ②③
C. ③
D.①②④
37. 下列关于药物的说法正确的是(
)
A. 使用青霉素时,不需要进行皮试,可以直接注射
B.虽然药物能治病,但大部分药物有毒副作用
C. 长期大量使用阿司匹林可预防疾病,没有副作用
�
D.R 和 OTC 类药物不需要持有医生处方都可以从药店购买
38. 下列关于合金的叙述中不正确的是 (
)
A.合金与其成分金属相比具有更优良的化学或机械性能
B.形状记忆合金是一种新型合金,可应用于生物工程领域
C. 不锈钢是一种抗腐蚀能力很强的合金,在海水也不会被腐蚀
D.硬铝是一种常见的的铝合金,它密度小,强度高,是制造飞机的理想材料
39. 下列有关叙述中不正确的是(
)
A. 传统陶瓷经高温烧结而成,其强度很高,抗摔能力很强
B.钢化玻璃比普通玻璃有更高的强度,常用于制造汽车或火车的车窗
C. 目前中、美、日等国家掌握的陶瓷发动机技术,使热效率大幅度提高
D.石英玻璃制成的光导纤维是一种新型无机非金属材料
40. 下列物质不属于天然高分子的是(
)
A.纤维素
B.油脂
C.淀粉
D.蛋白质
41. 大气污染的危害是多方面的,下列有关叙述中不正确的是(
)
A. 含氟制冷剂的大量生产和使用,会使臭氧层遭到破坏
B. 化石燃料的大量使用会加剧空气污染
C. 二氧化碳的大量排放,是形成酸雨的主要原因
D. 含铅汽油的广泛使用,带来了严重的铅污染
42. 景德镇盛产瓷器,瓷器的材质属于(
)
A.合金材料
B.合成高分子材料
C.天然高分子材料
D.无机非金
属材料
43. 利用蛋白质的变性可以为我们日常生活和医疗卫生服务。下列实例与蛋白质变性无关
的是(
)
A. 利用高温、紫外线对医疗器械进行消毒 B. 将鸡蛋蒸煮后食用
C. 给重金属中毒的病人服用蛋白质
D. 胃蛋白酶帮助人体消化食物
44.对食品的酸碱性判断是基本的生活常识。下列相关判断正确的是(
)
A. 西红柿、柠檬属于酸性食物
B. 黄瓜、胡萝卜属于碱性食物
C. 鸡蛋属于碱性食物
D. 猪肉、牛肉属于碱性食物
45. 下列污水处理方法中不属于化学方法的是(
)
A. 混凝法
B. 中和法
C. 自然沉降法
D. 氧化还原法
�
46. 下列四种常见食物与其所含主要营养物质对应关系正确的是(
)
A. 豆腐——油脂
B.鱼类——纤维素
C.葡萄——蛋白质 D.面包——
淀粉
47. 下列有关金属腐蚀与防护的说法不正确的是(
)
A. 钢铁发生电化学腐蚀时,若表面水膜呈中性,则正极发生的反应为:
2H2O+O2+4e 一= 4OH 一
B. 在潮湿的空气中,黄铜(铜锌合金)制品比纯铜制品更易产生铜绿
C. 金属制品在海水中比淡水中更容易发生腐蚀
D. 从本质上看,金属腐蚀是金属原子失去电子变成阳离子被氧化的过程
《化学反应原理》选修模块
36. 恒温恒容时,发生反应 2A(g)
B(g)+C(g),若反应物的浓度由 0.8mol/L 降至
0.6mol/L 需 20s,那么由 0.6mol/L 降到 0.4mol/L,所需反应时间(
)
A. 等于 20s
B. 大于 20s
C. 小于 20s
D. 以上都不正确
37. .下列过程表示吸热反应的是(
)
38. 镍镉(Ni 一 Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液
为 KOH 溶液,其充、放电反应按下式进行:
该电池充电时的阳极是(
)
A. Cd
B. Cd(OH)2
C. Ni(OH)2
D. NiO(OH)
39. 25℃时,测得某溶液由水电离产生的 H+浓度为 1.0×10 一 13mol/L,则关于该溶液的判断
正确的是(
)
A.一定是碱的溶液,且 pH=13
B.一定是酸的溶液,且 pH=1
C.有可能是盐的溶液,由于发生了水解反应,使得 pH=1 或 pH=13
D.酸、碱、盐的溶液均有可能
40. 下列能表示物质燃烧热的热化学方程式是(
)
A.C(s)+
1
2
O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
B.CO(g)+
1
2
O2(g)===CO2(g) ΔH=
-283.0kJ·mol-1
�
1
C.H2(g)+
2
O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1
D.2C8H18(l)+25O2(g)===16CO2+18H2O(l) ΔH=-11036 kJ·mol-1
41. 下列措施能使溶液中醋酸的电离平衡(CH3COOH
CH3COO 一+H+)逆向移动的是
A.加热
B.滴加 NaOH 溶液 C.加入少量醋酸钠固体 D.加入适量蒸馏水
42. 实验室制备 CuSO4 溶液时,为了抑制 CuSO4 水解,正确的操作方法是(
)
A. 加入硫酸
B. 加水稀释
C. 加入 NaOH
D. 加热
43. 关于 CO(g)+H2O(g)
CO2(g)+H2(g)的平衡常数(K)的表达式是(
)
A. K=c(CO)·c(H2O) / c(CO2) ·c(H2)
B. K= c(CO2) ·c(H2) / c(CO)·c(H2O)
C. K= c(CO2) ·c(H2) / c(CO)
D. K= c(CO2)
/ c(CO)·c(H2)
44. 已知常温下 Ksp(AgCl)=1.8×10 一 10、Ksp(AgI)=1.0×10 一 16。下列说法中不正确的是(
)
A.AgCl 和 AgI 都难溶于水
B.AgCl 和 AgI 的 Ksp 相差大,AgCl 可以转化为 AgI
C.常温下,向 AgI 饱和溶液中加入少量 AgNO3 固体, Ksp(AgI)增大
D.常温下,AgCl 和水形成的悬浊液中,Cl 一物质的量浓度为√1.8×10 一 5mol/L
45. 已知:①C(石墨,s)+O2=CO2(g) ΔH1=一 393.5 kJ·mol-1
② C(金刚石,s)+O2=CO2(g) ΔH1=一 395.0 kJ·mol-1
下列有关叙述中,不正确的是(
)
A.相同条件下,金刚石比石墨更稳定
B.反应 C(石墨,s)= C(金刚石,s)是吸热反应
C.相同条件下,等质量的金刚石和石墨完全燃烧,金刚石放出的热量更多
D.相同条件下,等质量的石墨比金刚石的能量更低
46. 下列有关说法正确的是(
)
A 若某反应的ΔH > 0,反应体系能量升高,有利于该反应自发进行
B 若某反应的ΔS < 0,反应体系混乱度减小,有利于该反应自发进行
C 若某反应的ΔH <0,ΔS < 0,该反应一定不能自发进行
D 若某反应的ΔH <0,ΔS > 0,该反应一定能自发进行
47. 银器的保护主要是维持它的原貌,对于轻微腐蚀蒙有硫化银的银器,可将其与铝片一
起接触浸泡在稀 NaOH 溶液中,经一定时间污迹消失,取出后用水洗净,再用软布或棉
团擦干。有关叙述正确的是(
)
�
A.溶液中 OH 一向正极移动 B.在银器表面发生的反应为 Ag2S+2e 一=2Ag+S2 一
C.在铝表面的反应为 Al 一 3e 一=Al3+
D.在铝表面的反应为 Al+4OH 一+3e 一=AlO2
一+2H2O
班级
姓名
成绩
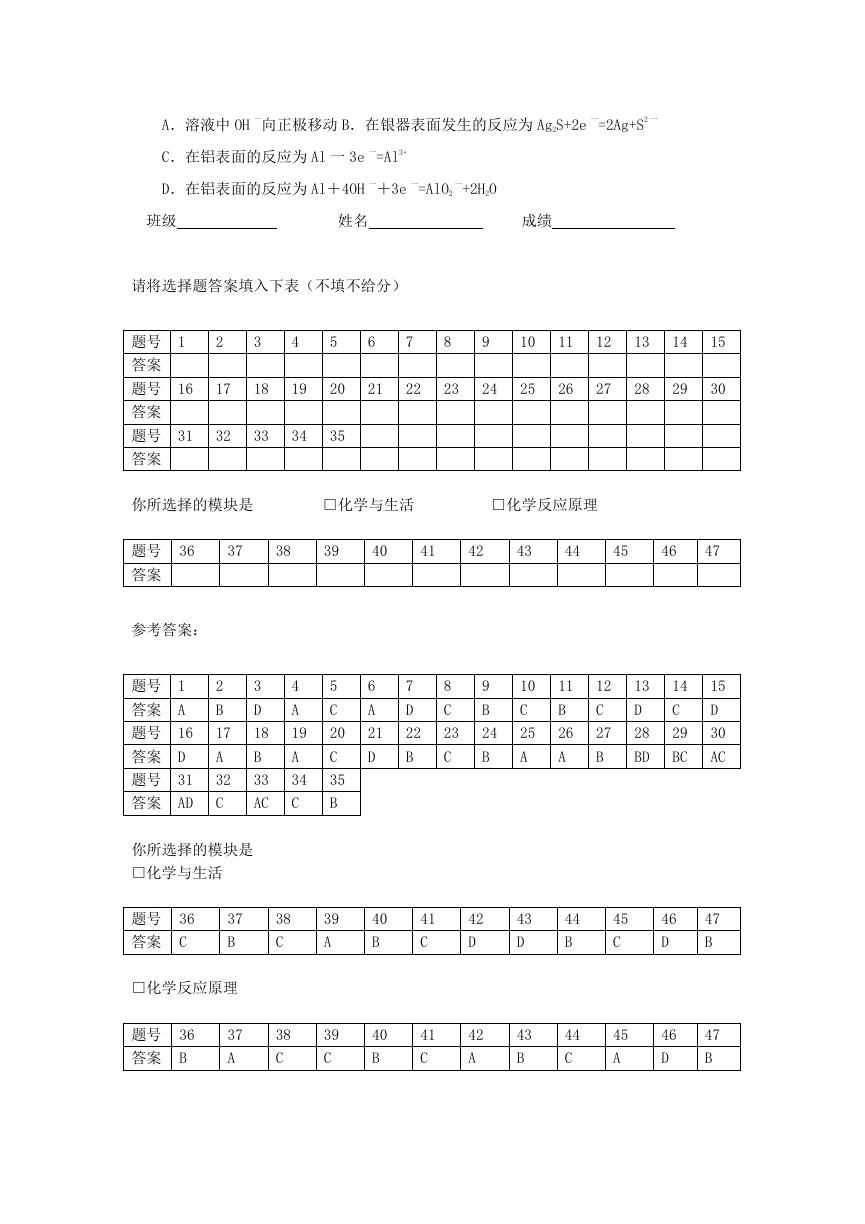
请将选择题答案填入下表(不填不给分)
题号 1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
答案
题号 16
17
18
19
20
21
22
23
24
25
26
27
28
29
30
答案
题号 31
32
33
34
35
答案
你所选择的模块是
□化学与生活
□化学反应原理
题号 36
37
38
39
40
41
42
43
44
45
46
47
答案
参考答案:
题号 1
答案 A
题号 16
答案 D
题号 31
答案 AD
2
B
17
A
32
C
3
D
18
B
33
AC
4
A
19
A
34
C
5
C
20
C
35
B
你所选择的模块是
□化学与生活
6
A
21
D
7
D
22
B
8
C
23
C
9
B
24
B
10
C
25
A
11
B
26
A
12
C
27
B
13
D
28
BD
14
C
29
BC
15
D
30
AC
题号 36
答案 C
37
B
□化学反应原理
题号 36
答案 B
37
A
38
C
38
C
39
A
39
C
40
B
40
B
41
C
41
C
42
D
42
A
43
D
43
B
44
B
44
C
45
C
45
A
46
D
47
B
46
D
47
B
�















 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc