2015 年西藏林芝中考化学真题及答案
可能用到的相对原子质量:H-1
C-12
O-16
S-32
Fe-56
一、选择题
1、下列生活事例中,属于化学变化的是(
)
A、西瓜榨汁
B、铁锅生锈
C、冰雪消融
D、白醋挥发
2、下列属于化石能源的是(
)
A、太阳能
B、风能
C、地热能
D、煤炭
3、下图把示的实验操作中,完全正确的是(
)
A.测定溶液 pH
B.取用液体药品
C.稀释浓硫酸
D.加入大理石
4、下列物质属于氧化物的中(
)
A、K2CO3
B、O3
C、Al2O3
D、FeCl2
5、有关溶液的说法正确的是(
)
A、溶液中的溶质一定是固体
B、溶液一定是混合物
C、溶液中上层浓度小,下层深度大
D、溶液一定是无色透明的[来源:学,科,网]
6、“无土栽培”使用的营养液含有以下主要成分,其中属于复合肥料的是(
)
A、KNO3
B、CO(NH2)2
C、Ca(H2PO4)2
D、(NH4)SO4
7、以下实验现象描述不正确的是(
)
A、铁丝在氧气中燃烧,火星四射
B、红磷在空气中燃烧产生大量白烟
C、镁条在空气中燃烧发出耀眼的白光
D、硫粉在氧气中燃烧产生淡蓝色火焰
8、下列选项中物质的俗名和化学名称表示同一物质的是(
)
A、纯碱
氢氧化钠
B、干冰
水
C、生石灰 碳酸钙
D 、小苏打 碳酸氢钠
9.健康人的体液必须维持在一定的酸碱度范围内,以下体液一定呈碱性的是(
)
A
血浆
B
唾液
C
胃液
D
尿液
体液
�
pH
7.35~7.45
6.6~7.1
0.9~1.5
4.7~8.4
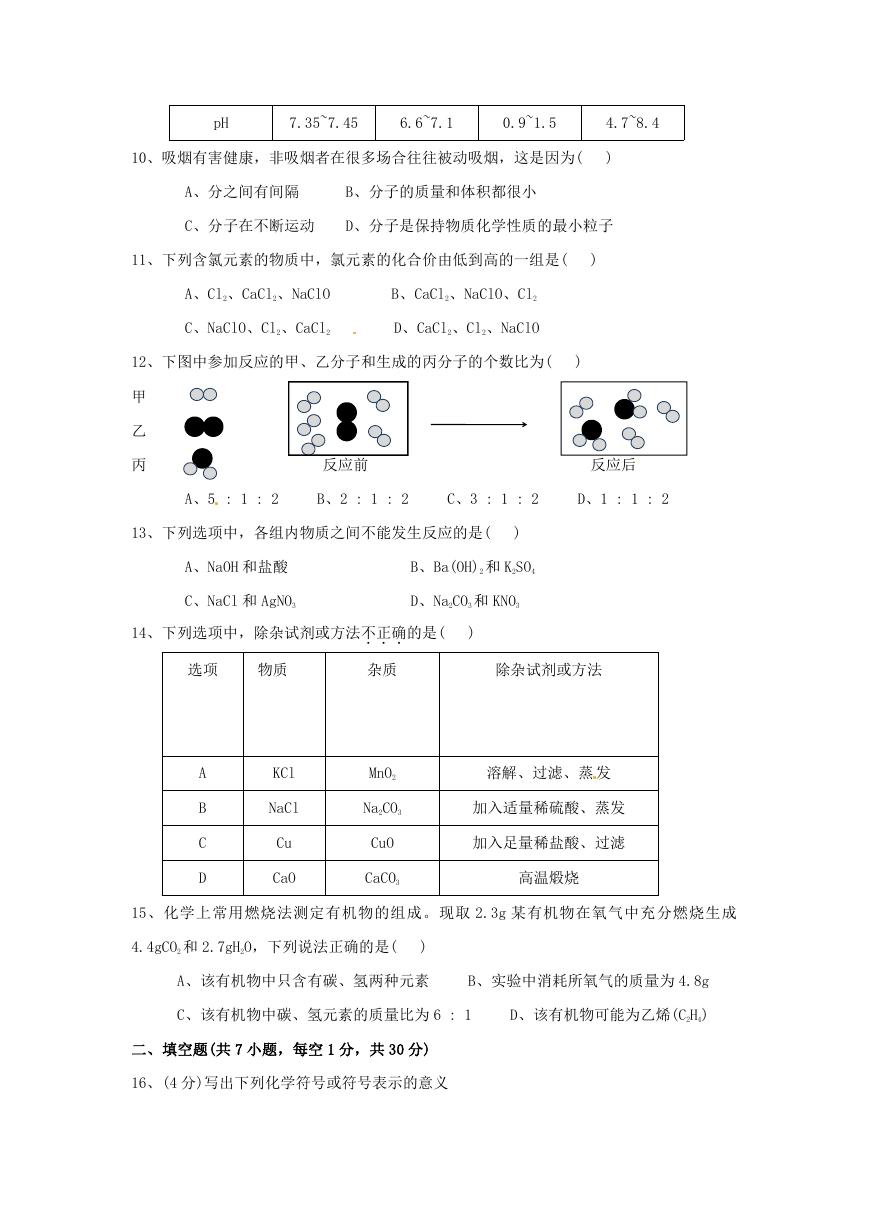
10、吸烟有害健康,非吸烟者在很多场合往往被动吸烟,这是因为(
)
A、分之间有间隔
B、分子的质量和体积都很小
C、分子在不断运动
D、分子是保持物质化学性质的最小粒子
11、下列含氯元素的物质中,氯元素的化合价由低到高的一组是(
)
A、Cl2、CaCl2、NaClO
B、CaCl2、NaClO、Cl2
C、NaClO、Cl2、CaCl2
D、CaCl2、Cl2、NaClO
12、下图中参加反应的甲、乙分子和生成的丙分子的个数比为(
)
甲[来源:Zxxk.Com]
乙
丙
反应前
反应后
A、5 : 1 : 2
B、2 : 1 : 2
C、3 : 1 : 2
D、1 : 1 : 2
13、下列选项中,各组内物质之间不能发生反应的是(
)
A、NaOH 和盐酸
B、Ba(OH)2 和 K2SO4
C、NaCl 和 AgNO3
D、Na2CO3 和 KNO3
14、下列选项中,除杂试剂或方法不正确...的是(
)
选项
物质[来
杂质
除杂试剂或方法
源:Zxxk.
Com]
KCl
NaCl
Cu
CaO
A
B
C
D
MnO2
Na2CO3
CuO
CaCO3
溶解、过滤、蒸 发
加入适量稀硫酸、蒸发
加入足量稀盐酸、过滤
高温煅烧
15、化学上常用燃烧法测定有机物的组成。现取 2.3g 某有机物在氧气中充分燃烧生成
4.4gCO2 和 2.7gH2O,下列说法正确的是(
)
A、该有机物中只含有碳、氢两种元素
B、实验中消耗所氧气的质量为 4.8g
C、该有机物中碳、氢元素的质量比为 6 : 1
D、该有机物可能为乙烯(C2H4)
二、填空题(共 7 小题,每空 1 分,共 30 分)[来源:Zxxk.Com]
16、(4 分)写出下列化学符号或符号表示的意义
�
(1)2 个磷原子
(2)Mg2+中“2”的意义
(3)7 个二氧化氮分子
(4)二氧化硅中硅元素的化合价显+4 价
17、(4 分)现有 C、H、O、N 四种元素,选择项中一种或几种元素组成符合下列要求的物质,
并用化学式...表示:
(1)空气中体积分数最大的气体
。 (2)自然界中天然存在的最硬的物质
。
(3)天然气的主要成分
。
(4)溶解于水使溶液温度降低的是
。
18、(4 分)图中 A、B、C、D 是四种粒子的结构示意图,E 是碘元素在元素周期表中的信息。
回答下列问题:
(1)A、B、C、D 四种粒子共表示
元素,其中阴离子 的符号为
。
(2)D 中的 X=
。
(3)E 中碘元素原子的核外电子数为
。
19、(5 分)化学与生活密切相关。
(1)右图是某校食堂的食谱,从所含营养素分析,除水和无机盐外,
主 食 中 主 要 含 有 营 养 素 是
, 食 谱 中 缺 少 的 营 养 素
是
。
今日菜谱
主食:米饭、馒头
副食:红烧鱼、排骨
鸡蛋、牛肉
饮料:牛奶、纯净水、
可乐
(2)小强去医院体检,医生说他有点贫血,你认为他应该适当补充
元素。
(3)炒菜时油锅着火,可用锅盖盖灭。其灭火原理是
。
(4)生活中常用
的方法降低水的硬度,同时又可以杀菌消毒。
20、(3 分)向氯化铜和氯化镁混合溶液中加入一定质量的锌粉,有关反应的化学方程式为
,待充分反应后过滤,向滤渣中滴加稀盐酸,有气体产生,则滤渣中一定含
有
,滤液中一定含有的溶质为
。
21、(5 分)图甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题。
(1)t1℃时,甲、乙、丙的溶解度由大到小的顺序是
。
(2)P 点的含义
。
(3) t3℃时,在 150g 水中加入 100g 甲,所得溶液
(选填“是”
或“不是”)饱和溶液,形成溶液的质量为
g。
�
(4) t2℃时,甲、乙、丙三种物质的饱和溶液升温至 t3℃后,三种溶液的溶质质量分数由大
到小的顺序是
。
22、(5 分)已知 A~G 为初中化学常见的物质。
如图所示“→”表示转化关系,“—”表示相互能发生反
应。已知 A 是人体胃液中含有的酸,E 是最轻的气体,B
和 D 所含元素相同。
请回答:
(1)写出下列物质的化学式:A
,D
。
(2)G 物质的一种用途
。
(3)写出 F→E 的化学反应方程式
,该反应的基本类型为____
反应。
三、实验探究题(共 5 小题,每空 1 分,共 29 分)
23、(4 分)(1)用完酒精灯后,必须用
盖灭,不可用嘴去吹。
(2)加热时,试管内液体不应超过试管容积的
。
(3)溶解、过滤 和蒸发操作中都要用到玻璃棒。溶解时玻璃棒的作用是
。过滤时玻
璃棒的作用是
。
24、(7 分)实验室中,利用下列装置可以制取某些气体。
回答下列问题:
(1)写出带标号仪器的名称①
;②
。
(2)向组装好的气体发生装置中加入药品前,应该进行的操作是
。
(3)实验室若用高锰酸钾制取氧气,选择的发生装置是
(填字母);用过气化氢溶液制
取氧气的化学方程式为
。
(4)乙炔又称电石所,是一种无色无味、密度比补气略小、不易溶于水的气体,工业上常用
它燃烧产生的高法国来切割和焊接金属。实验室用电石(固体)与水反应制取乙炔,你认为应
选择的发生装置是_____(填字母),为了收集到纯度较高的乙炔,应选择的收集装置是
______(填字母)。
�
25、(4 分)欲配制 100g10%的 NaCl 溶液,操作如下图所示。
请回答下列问题:
(1)图中操作有错误的是
(填序号)
(2)配制该溶液时,需要 NaCl 固体
g。
(3)量取溶剂时,采用仰视的方法读数,会导致溶液的溶质质量分数
(“偏大”、“偏
小”或“无影响”)。
(4)将配好的溶液稀释成溶质质量分数为 5%的 NaCl 溶液,需加入
g 水。
26、(6 分)某研究小组发现,维 C 泡腾片(主要成分如图所示)溶于水,有许多气泡产生,小
组同学对该气体的成分进行了如下探究:
【猜想与假设】
卓玛说:该气体可能是 O2、H2、SO2、CO、CO2。
扎西说:不可能有 SO2,因为
。
德吉说:不可能有 H2 和 CO,从药品安全角度考
虑,H2 易燃易爆,CO
。
讨论后,小组同学认为该气体可能有 O2、CO2 中的一种或两种。
【进行实验】
实验编号
实验操作
实验现象
①
②
【得出结论】
将气体通入澄清石灰水中
澄清石灰水 变浑浊
将带火星的木条伸入该气体中
带火星的木条没有复燃
(1)由实验①可知,该气体中肯定含有
,写出该反应的化学方程式:
。
(2)由实验②不能确定该气体中不含氧气,理由是
。
【拓展延伸】向维 C 泡沸片溶液中滚圆石蕊试液,溶液变红,说明溶液显
性。
27、(8 分)氢化钙固体是登山运动员常用的能源提供剂。某探究小组的同学通过查阅资料得
知,氢化钙(CaH2)遇水反应生成氢氧化钙和氢气,请写出该反应的化学方程式
。
探究小组的同学把一定量的 CaH2 加入 Na2CO3 溶液中,充分反应后过滤,得到滤渣和滤液。
�
经检验滤渣的成份是碳酸钙。
【提出问题】滤液中溶质的成份是什么?
【猜想与假设】
猜想一:NaOH
猜想二:NaOH 和 Ca(OH)2
猜想三:NaOH 和
猜想四:NaOH、Na2CO3 和 Ca(OH)2
经过讨论,大家认为猜想四不合理,用化学方程式说明原因
。
【实验证明】
实验
现象
结论
实验一:取滤液,向其中滴入少量碳酸钠溶液 Ⅰ:
猜想二不成立
实验二:另取滤液,向其中加入足量
Ⅱ:产生气泡
猜想
成立
【反思与拓展】
(1)向 CaH2 和足量水反应后的溶液加入 NH4Cl 溶液,产生的气体是
(2)登山运动员常用 CaH2 作为能源提供剂,与氢气相比,其优点是
。
。
四、计算题 (共 11 分)
28、(4 分)丁二酮(C4H6Ox)可用作糖果增香剂。请计算:
(1)丁二酮是由
元素组成的。
(2)碳元素和氢元素的质量比为
。
(3)丁二酮的相对分子质量为 86,则 x 的数值为
。
(4) 17.2g 的丁二酮含碳元素的质量为
g。
29、(7 分)硅钢合金是变压器、充电器中的核心材料,其主要成份是铁和硅。向 8.4g 硅钢
中加入 100g 稀硫酸,恰好完全反应(硅及其杂质不溶于水,且都不与稀硫酸反应),放出气
体的质量与反应时的关系如图所示。
试回答:(计算结果精确到 0.1% )
(1)硅钢合金属于
材料(选填“金属”或“有机物”)
(2)硅钢合金中铁的质量分数。
(3)反应结束后所得溶液溶质质量分数。
[来源:Zxxk.Com]
�
2015 年西藏自治区高中中职学校招生统一考试试卷
化学参考答案
一、选择题
1、B
2、D
3、B
4、C
5、B
6、A
7、D
8、D
9. A
10、C
11、D
12、B
13、D
14、B
15、B
二、填空题(共 7 小题,每空 1 分,共 30 分)
16、(4 分)(1)2P;(2)一个镁离子带 2 个单位的正电荷;(3)7NO2;(4) 。
17、(4 分)(1)N2;(2)C;(3)CH4;(4)NH4HCO3。
18、(4 分)(1)3;Cl-。(2)8。(3)53。
19、(5 分)(1)糖类;维生素。(2)Fe。(3)隔绝空气(或氧气)。(4)煮沸。
20、(3 分) Zn+CuCl2==Cu+ZnCl2;Zn;ZnCl2、MgCl2。
21、(5 分)(1)乙>丙>甲; (2)t2℃时,甲、丙两物质的溶解度相等;
(3)不是;250。 (4)乙>甲>丙。
22、(5 分)(1)HCl; CO。(2)改良酸性土壤。(3)2H2O 通电 2H2↑+O2↑;分解。
三 、实验探究题(共 5 小题,每空 1 分,共 29 分)
23、(4 分)(1)灯帽 (2)1/3 (3)搅拌,加速溶解;引流。
24、(7 分) (1)铁架台;锥形瓶
(2)检查装置的气密性。
(3)A;2H2O2MnO22H2O+O2↑
(4)B;C 或 E
25、(4 分)(1)② (2)10g (3)偏小
26、(6 分)
【猜想与假设】根据元素的质量守恒,主要成分中没有 S 元素;有毒。
【得出结论】(1)CO2;CO2+Ca(OH)2==CaCO3↓+H2O (2)是因为氧气含量很低时带火星的
木条也不能复燃。
【拓展延伸】酸。
27、(8 分) CaH2+2H2O == Ca(OH)2+2H2↑。
【猜想与假设】猜想三:Na2CO3;Na2CO3+Ca(OH)2== CaCO3↓+2NaOH。
【实验证明】实验一:没有产生沉淀;实验二:稀盐酸;猜想三。
四、计算题 (共 11 分)
28、(4 分)
�
(1)碳、氢、氧(或三种)。
(2)8︰1
(3)2
(4)9.6g
29、(7 分)
(1)金属
解:设 8.4g 硅钢中铁的质量为 x,生成硫酸亚铁的质量为 y
Fe+H2SO4==FeSO4+ H2↑
56
X
0.25g
56/x==152/y==2/0.25g
X==7g
152
y
2
y==19g
(2)硅钢合金中铁的质量分数==(7g÷8.4g)×%≈83.3%
(3)反应结束后所得溶液溶质质量分数==19g÷(7g+100g-0.25g)×%≈17.8%
答:略。
�















 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc