2005 年福建普通高中会考化学真题
一、选择题(每小题只有一个正确选项,每小题 2 分,共 44 分)
1.许多城市禁止燃放烟花爆竹,除噪声污染外,爆竹燃放时会产生一种无色有刺激性气味、
有毒的气体,这种气体是
A.N2
B.Cl2
C.CO2
D.SO2
2.下列物质中只含有离子键的是
‥
‥
A.H︰O︰H
‥
B.Mg2+[︰O︰H]2—
‥
3.下列物质所含分子数最少的是
‥
C.Na+[︰O︰H]
—
‥
H
H
C=C
H
H
D.
A.标准状况下 11.2 L HCl
B.32g O2(O2 的摩尔质量为 32g/ mol)
C.6.02 ×1023 个 N2
D.1.5 mol H2O
4.日常生活中常用下面一种物质的热溶液(该物质水解后溶液呈碱性)作为清除油污的洗
涤剂,该物质是
A.食盐
B.白糖
C.食醋
D.纯碱
5.下列做法对人体健康无害的是
A.工业酒精(含甲醇)兑水配制白酒饮用
B.在食用盐中加入碘酸钾(KIO3)以消除碘缺乏病
C.制作腊肉常加入亚硝酸盐作增色剂和防腐剂,宜长期食用
D.用工业石蜡给瓜子美容
6.在水溶液中能大量共存的离子组是
A.Na+ 、Mg2+ 、NO3
—
B.Fe3+、Cl—、OH—
C.K+ 、H+ 、HCO3
—
D.Cu2+、Ag+ 、Cl—
7.溴水滴入下列溶液中,不发生反应的是
A.KI
B.KOH
C.AgNO3
D.NaCl
8.右图是有机物分子的球棍模型,其中白球表示氢原子,黑球表示碳原子,短棍表示共价
键,该有机物的名称为 (
)
A.乙烯 B.乙烷
C.乙炔
D.乙醛
9.下列各组物质互为同素异形体的是
�
A. O16
8 与 O18
8
B.金刚石与石墨
C.CH3OH 与 CH3CH2OH
D.
CH3—CH—CH3 与 CH3—CH2—CH2—CH3
|
CH3
10.下列家庭化学小实验不能达到预期目的的是
A.利用灼烧法区别羊毛织物和棉织物
B.热水瓶胆内的水垢[主要成份 CaCO3,Mg(OH)2]用食醋清洗
C.将动物油(如:牛油)与食盐共热以制造肥皂
D.用水果(如葡萄等)自制甜酒酿
11.下列反应中 H2O 只作氧化剂的是
A.2 Na + 2 H2O == 2 Na OH + H2↑ B.CaO + H2O == Ca(OH)2
C.2 F2 + 2 H2O == 4HF + O2
D.Cl2 + H2O == HCl + HClO
12.选用一种试剂就能把浓度均为 1 mol/L 的 Na2CO3、Na2SO4、Na2SO3、BaCl2 溶液加以区别,
这种试剂是
A.CaCl2
B.AgNO3
C.NaOH
D.H2SO4
13.下列离子方程式书写正确的是
A.铁粉与稀盐酸反应:Fe + 6 H+ == Fe3+ + 3 H2↑
B.氯气通入碘化钾溶液中 Cl2 + I— == Cl— + I2
C.氨水与氯化铝溶液反应 Al3+ + 3 NH3·H2O == Al(OH)3 + 3 NH4
+
D.稀硫酸与氢氧化钡溶液反应 Ba2+ + SO4
2— == BaSO4↓
14.某研究性学习小组为了评价当地地雨水的酸度(酸性强弱),选用下列检测试剂,正确
的是
A.pH 试纸
B.酚酞试液
C.淀粉碘化钾试纸
D.红色石蕊试纸
15.实验室用铁片与稀 H2SO4(1mol/L)反应制 H2 时,采取下列措施,不能使生成 H2 的速率
加快的是(
)
A.给试管内混合物加热
B.将稀 H2SO4 改为浓 H2SO4
�
C.将铁片改为铁粉
D.滴加少量 CuSO4 溶液
16.一氧化碳中毒,是由于一氧化碳跟血液里的血红蛋白结合,使血红蛋白不能很好地跟
氧气结合,人因缺少氧气而窒息,甚至死亡。这个反应可表示如下:
(血红蛋白—O2)+ CO
(血红蛋白—CO)+ O2,抢救中毒患者采取的措施中不正确的是
A.立即打开门窗通风
B.将中毒者转移到空旷的地带
C.给中毒者喷淋水
D.给危重病人及时输氧
17.节约用水,保护水资源是每个公民应尽的义务,下列说法正确的是
A.沿海地区可以不考虑节约用水的问题
B.既要预防和消除对水的污染,又经节约用水
C.减少饮用水
D.将工业废水直接排放到江河湖泊中
18.下列物质能用无色带玻璃塞的试剂瓶保存的是
A.氢氧化钾溶液
B.氯水
C.稀盐酸
D.用作感光材料的 AgBr
19.下列各组物质相混合能产生可燃性气体的是(
)
A. 电石(CaC2)与水
B.双氧水(H2O2)与二氧化锰
C.石灰石与稀盐酸
D.二氧化锰与浓盐酸共热
20.化学实验室里,金属钠着火时,可选择的灭火材料是
A.泡沫灭火器
B.水
C.干冰(CO2 固体)灭火器
D.沙子
21.下列关于硝酸的叙述,正确的是(
)
A.常温下稀 HNO3 能使铁钝化
B.浓 HNO3 是强酸,稀 HNO3 是弱酸
C.浓 HNO3 和稀 HNO3 都是强氧化剂
D.铜分别与浓 HNO3 、稀 HNO3 反应都生成 NO2
22.在实际生活中,以下说法不正确的是
A.钙、铁、锌有益人体健康,应大量食用
B.家庭中不宜用铝合金容器长期存放菜、汤食品
C.苯酚可用于环境消毒,医用酒精可用于皮肤消毒,其原因均在于可使病毒和细菌体
内的蛋白质变性
D.鱼胆弄破后会使鱼肉粘上难溶于水的胆汁酸(一种酸)而变苦,要减少这种苦味,
�
可用 Na2CO3 洗涤
二、填空题(本大题共 36 分)
23.某学生将青香蕉与熟苹果装入塑料袋后,紧系袋口,过几天青香蕉变黄成熟了,这是
因为成熟水果自身放出
气体可以催熟生水果(填“甲烷”或“乙烯”)。蛋白
质、淀粉、油脂是三类重要的营养物质,其中
不是天然高分子化合物。浓硝
酸常呈黄色,是由于硝酸分解产生的
溶于硝酸的缘故(填“NO2”或“O2”)。(6
分)
24.针对下表中 8 种元素,填写以下空格。(8 分)
族
周
期
2
3
Ⅰ
Ⅱ
Ⅲ
Mg
Al
Ⅳ
C
Ⅴ
Ⅵ
O
S
Ⅶ
F
Cl
0
Ar
(1)非金属性最强的元素是__________________。
(2)Ar 原子结构示意图为__________________。
(3)C 与 O 中,原子半径较大的是_________________。
(4)HCl 的电子式为_________________。
(5)H2O 与 H2S 中,较不稳定的是_________________。
(6)Mg(OH)2 与 Al(OH)3 中,碱性较强的是_________________。
(7)Al2O3 与盐酸反应的离子方程式为________________________________________。
25.写出下列反应的化学方程式。(4 分)
(1)碳酸氢钠受热分解:
(2)在催化剂存在下,苯与溴反应:
26.
O
丙烯醛的结构简式为:CH2=CH—C—H。请填写下列空格。
(1)丙烯醛分子中除碳碳双键外,还含有的官能团是
(填名称)。
(2)丙烯醛能发生的反应是
(填选项的标号)。
A.消去反应
B.酯化反应
C.氧化反应
D.水解反应
(3)丙烯醛与新制 Cu(OH)2 悬浊液共热生成的有机物的结构简式为
(4)1mol 丙烯醛最多能与
mol H2 发生加成反应。
27.现有 NH4Cl、Al2O3 及 Na2O2 组成的混合物,加足量水,加热后,固体全部溶解。变化关
�
系如下图所示。填写以下空格。(5 分)
NH4Cl
Al2O3
Na2O2
足量水、加热
刺激性气体 A
溶液 B
(1)气体 A 是
和
的混合气。
(2)溶液 B 中一定含有的阴离子是
和
,可能含有的阴离子是
(注:不考虑水的电离)。
28.含 BaCl2 的物质的量相同的氯化钡溶液分别与体积相同的 KAl(SO4)2 溶液和 Al2(SO4)3 溶
液 恰 好 完 全 反 应 , 则 KAl(SO4)2 溶 液 和 Al2(SO4)3 溶 液 中 Al3+ 的 物 质 的 量 浓 度 之 比
是
。
29.简要回答下列问题。(6 分)
(1)2004 年 4 月 16 日重庆某化工厂氯气池泄漏,引起氯气罐爆炸,消防人员用 6 个高压
水枪同时喷水和稀烧碱溶液,以防止氯气扩散,其原理是____________________________。
_____________________________________________________________________________
(2)据报道,北京曾发生一起游客用 H2SO4 伤熊事件,致辞使动物园内五只熊被严重烧伤。
用你所学的化学知识分析报道中“烧”的含义____________________________________
_____________________________________________________________________________
(3)目前“白色污染”问题日趋严重,请你就怎样解决“白色污染”提出一些切实可行的
措施:_____________________________________________________________________。
三、实验题(本题共 12 分)
30.为了达到下列表格中的实验要求,请从供选择的化学试剂及实验方法中选出合适的,
将其标号填入对应的空格中。(5 分)
�
实验要求
选项的标号
供选择的化学试剂及实验方法
证明马铃薯中含有淀粉
检验酒精中含有水
A. 无水硫酸铜
B. 焰色反应
检验 Na2CO3 溶液中含有 K2CO3
C. 通入溴的四氯化碳溶液
鉴别铝制品与银制品
除去 CH4 中的 CH2 =CH2
D. 加盐酸
E.加碘水
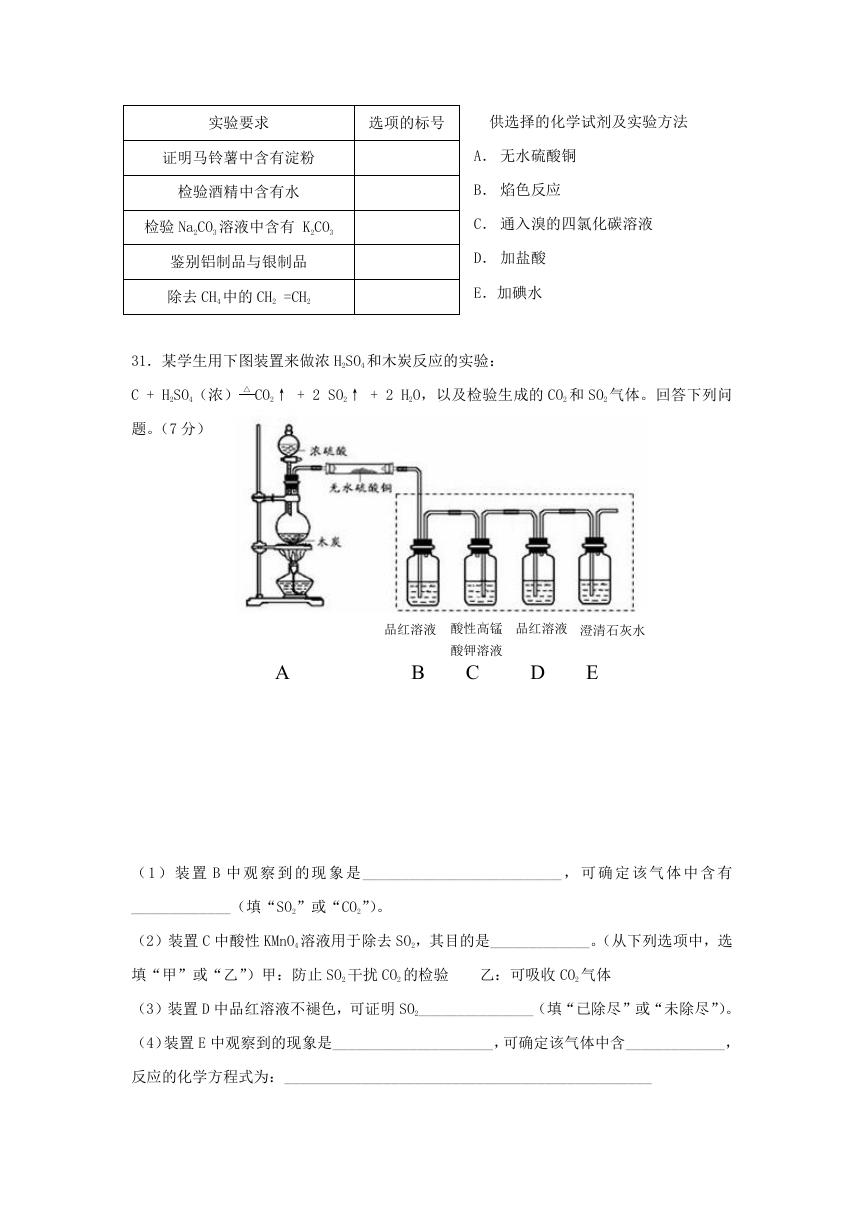
31.某学生用下图装置来做浓 H2SO4 和木炭反应的实验:
C + H2SO4(浓) △ CO2↑ + 2 SO2↑ + 2 H2O,以及检验生成的 CO2 和 SO2 气体。回答下列问
题。(7 分)
品红溶液 酸性高锰
品红溶液
澄清石灰水
酸钾溶液
C
B
D
E
A
( 1 ) 装 置 B 中 观 察 到 的 现 象 是 __________________________ , 可 确 定 该 气 体 中 含 有
_____________(填“SO2”或“CO2”)。
(2)装置 C 中酸性 KMnO4 溶液用于除去 SO2,其目的是_____________。(从下列选项中,选
填“甲”或“乙”)甲:防止 SO2 干扰 CO2 的检验
乙:可吸收 CO2 气体
(3)装置 D 中品红溶液不褪色,可证明 SO2_______________(填“已除尽”或“未除尽”)。
(4)装置 E 中观察到的现象是_____________________,可确定该气体中含_____________,
反应的化学方程式为:________________________________________________
�
三、计算题(本题共 8 分)
32.将 4g NaOH 固体溶于水配成 250mL 溶液,计算溶液中 NaOH 的物质的量浓度。
(NaOH 的摩尔质量为 40g/mol)(2 分)
33.在一定条件下,铁粉与稀硝酸反应:8 Fe +30 HNO3(稀)==8 Fe(NO3)3 + 15 H2O + 3
N2O↑。如果反应结束时,共收集到 6.72 L N2O(标准状况)。求:
(1)被氧化的铁粉的质量。(Fe 的摩尔质量为 56g/mol)
(2)作为氧化剂的 HNO3 的物质的量。
�













 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc