2014 浙江省绍兴市中考化学真题及答案
1. (绍兴-1)下图所示的实验操作不正确的是(
)
A. 取用液体
B.称量 NaCl 质量
C.闻气体的气味
D.读取液体体积
2.(绍兴-7) “模拟实验”是一种常用的科学研究方法,以下不属于该研究方法的是(
)
A.研究气压与流速实验
B.米勒实验
C.研究宇宙膨胀实验 D.研究地球形状实验
3.(绍兴-8)某化肥包装袋上的部分说明如图所示,则下列说法不正确的是
(
)
A.硝酸铵属于氮肥
B.“含氮量”中的“氮”是指氮元素
C.硝酸铵受热可能会分解
D.硝酸铵中氮、氢、氧元素的质量比是 2∶4∶3
硝酸铵
化学式 NH4NO3
净 重 50Kg
含氮量 ≥28%
4.(绍兴-12)除去下列物质中的少量杂质,所用试剂和方法正确的是(
)
选项
A
B
C
D
物质
NaNO3
KCl
CO
H2
杂质
Na2CO3
K2SO4
CO2
HCl
试剂和方法
滴入足量稀盐酸至不再产生气泡
滴入适量Ba(NO3)2溶液、过滤
通过灼热的氧化铜粉末
先通过NaOH溶液,再通过浓硫酸
5. (绍兴-15)如图,表示镁、铜与其氧化物的质量关系。图线不重合的原因是 (
)
A.镁和铜的密度不同
B.与等质量的镁和铜化合的氧元素质量不同
C.加热不充分,没有完全氧化
D.实验的误差造成
6.(绍兴-19)下列图像不能正确反映对应变化关系的是(
)
A.在一定量 AgNO3 和 Zn(NO3)2 的混合溶液中加入铁粉
�
B.向等质量的锌粉和铁粉中,分别加入相同质量分数的稀盐酸
C. 常温下,向硝酸钾的不饱和溶液中加入硝酸钾晶体
D.向一定量的稀盐酸中加入过量的 NaOH 溶液
7.(绍兴-23)人类对原子结构的认识,经历了汤姆生、卢
瑟福和波尔等提出的模型的过程。
(1)卢瑟福核式结构模型是利用α粒子轰击金箔实验
的基础上提出的。下列能正确反映他的实验结果的
示意图是
(选填序号)。
(2 ) 从 原 子 结 构 模 型 建 立 的 过 程 中 , 我 们 发 现
(选填序号)。
A.科学模型的建立是一个不断完善、不断修正的过程
B.模型在科学研究中起着很重要的作用
C.波尔的原子模型建立,使人们对原子结构的认识达到了完美的境界
D.人类借助模型的建立,对原子的认识逐渐接近本质
8.(绍兴-26)以化合价为纵坐标,以物质的类别为横坐标所绘制的图像叫价类
图。如图为铁的价类图,例如 E 点可表示+2 价的亚铁盐。请回答:
⑴A 点表示的物质所属的物质类别是
⑵请写出 B 点表示的物质化学式
⑶已知 C 点表示的化合物在常温下能与氧气、水发生化合反应
生成 D,写出相应的化学方程式
。
。
。
9.(绍兴-28)氯化钡是一种可溶性重金属盐,广泛应用于化工领域。用毒重石(主要成分
为 BaCO3)制备氯化钡晶体的部分工艺流程如下图:
(1)本流程中“浓缩”、“结晶”属于
(2)滤液 2 中可利用的物质除水外,还有
(3)下列措施中,能提高原料的利用率和氯化钡晶体产量的有
变化。
(填化学式)。
(选填序号)。
①将毒重石进行粉碎 ②加入足量的稀盐酸 ③将滤液 2 通入到滤液 1 中
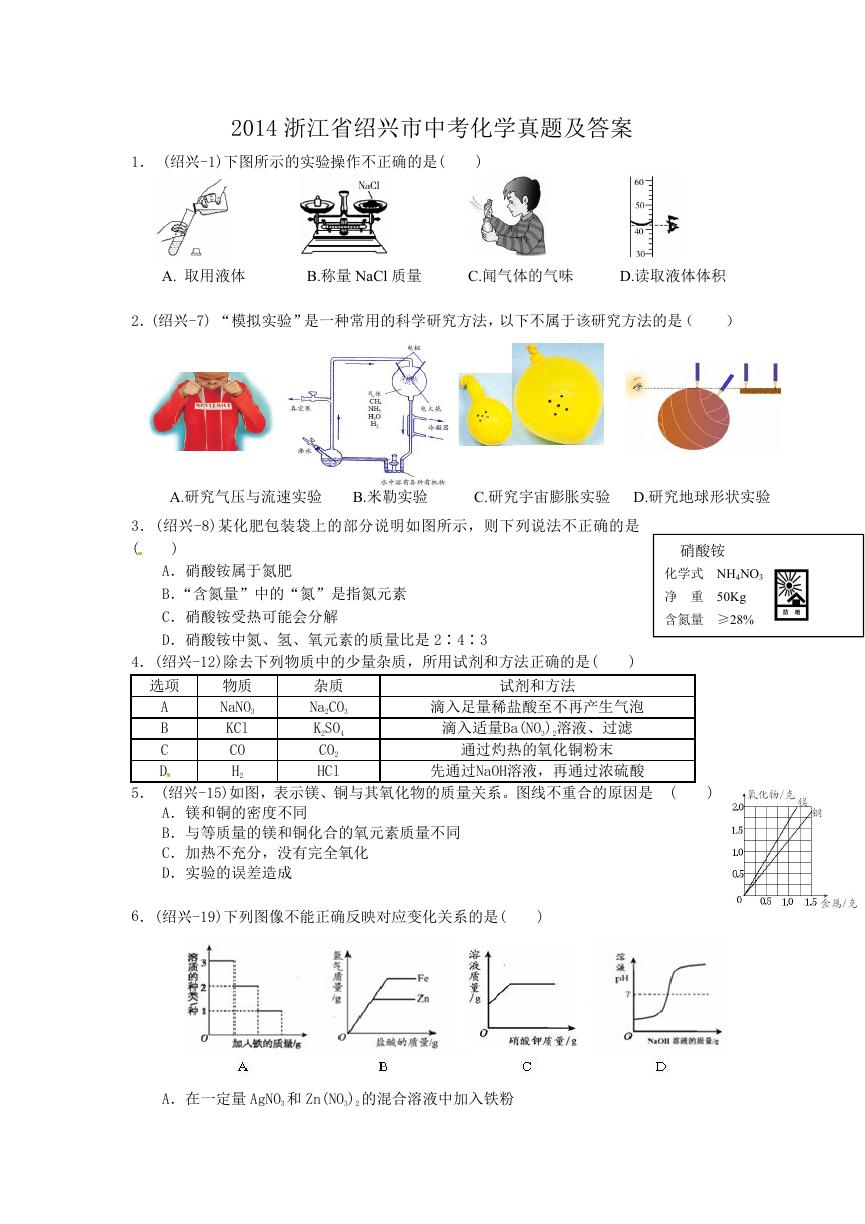
10.(绍兴-31)实验小组同学向盛有 2ml 稀硫酸的试管中加入 2ml 氢氧化钠溶液,未观察
到明显现象。
【提出问题】两者是否发生了化学反应?
【实验探究】将盛有上述实验混合液的试管标为①,如图甲。
小华:测得实验所用稀硫酸的 pH<7,试管①中溶液 pH>7。于是得出结论:
小敏:取两支试管,编号为②和③,分别加入稀硫酸和试管①中溶液各 2ml,逐滴滴
加 Na2CO3 溶液至过量..,实验过程与现象如图乙,由此他得出了与小华一样的
实验结论。
。
�
甲
乙
【反思评价】小军认为小敏在实验设计中存在不够严密的地方,请帮他指出:
【交流讨论】试管③中的溶液中有哪些溶质?同学们分析了两位同学的实验过程,一致
。
认为没有 H2SO4,其理由是
推理 1:含有 Na2SO4、Na2CO3 和 NaOH
推理 2:含有 Na2SO4、Na2CO3
正确的是推理
(选填“1”或“2”)。
。在此基础上,同学们提出了二种推理:
11.(绍兴-34)三位同学分别用相同质量分数的稀盐酸,测定某石灰石样品中碳酸钙的质量
分数(石灰石中的杂质既不与酸反应,也不溶于水)。
(1)小敏的方法可用如下流程表示,测得的碳酸钙的质量分数为_ ;在过滤操作中,
需要用到的玻璃仪器有_
(选填序号)。
A.酒精灯、漏斗、玻璃棒
B. 漏斗、玻璃棒、烧杯 C. 酒精灯、试
管、玻璃棒
样品 10 克
加入稀盐酸 50 克
充分反应后过滤,洗涤、干燥
滤渣 5 克
加入稀盐酸 50 克
充分反应后过滤,洗涤、干燥
滤渣 2.1 克
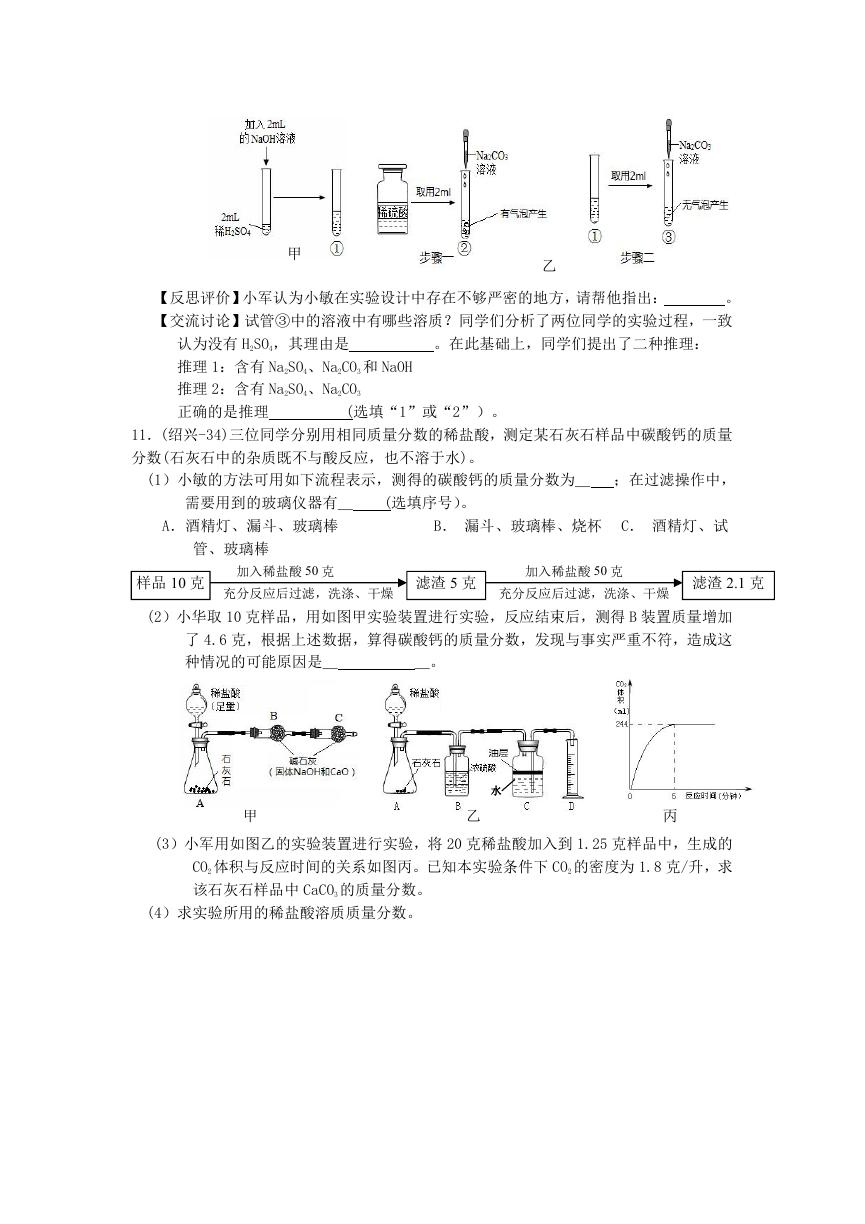
(2)小华取 10 克样品,用如图甲实验装置进行实验,反应结束后,测得 B 装置质量增加
了 4.6 克,根据上述数据,算得碳酸钙的质量分数,发现与事实严重不符,造成这
种情况的可能原因是_
_。
甲
水
乙
丙
(3)小军用如图乙的实验装置进行实验,将 20 克稀盐酸加入到 1.25 克样品中,生成的
CO2 体积与反应时间的关系如图丙。已知本实验条件下 CO2 的密度为 1.8 克/升,求
该石灰石样品中 CaCO3 的质量分数。
(4)求实验所用的稀盐酸溶质质量分数。
�
2.A
13.C
1.B
12.D
21.(1)A (2)换用低倍镜
3.D
14.A
4.A
15.B
5.B
6.B
7.A
8.D
9.B
10.D
11.D
16.C
17.C
18.D
19.A
20.C
(2)受精卵
远
(2)A、B、D
22.视网膜
23.(1)乙
24.(1)传染性
25.(1)<
(2) 变小
26.(1)单质 (2) FeO
27.96 右
28.(1)物理
29.(1)小球到达斜面的高度 (2)1 与 2
30.(1)设置对照组
(2)能
(2)BaCl2
(3)①②③
(3)长度、材料
(3)有无脊椎骨(其他合理答案均可)
变大[来源:学*科*网]
(3)4Fe(OH)2+O2+ 2H2O=4Fe(OH)3
(3)微生物可能来自软木塞(加热时间不够长)(其它合理答案均可)
(4)会
31.(1)两者发生了反应
(2)应取用试管①中的全部溶液与 2ml 稀硫酸做比对实验
(3)试管①溶液 pH 大于 7(H2SO4 已经反应完或试管③中滴入 Na2CO3 无气泡)
(4)
l
32.(1)6.50
⑵如图
(3)①导体的电阻大小与导体的材料有关
②导体的电阻大小与导体的长度有关
33.(1)杀死容器内原有的微生物 (2)B (3)25℃—42℃ 8
34.(1)79%(1 分)
B(2 分)
(2)B 中吸收了二氧化碳带出的水蒸气或 HCl 气体
(3)生成 CO2 的 m=ρV=1.8 克/升×0.244 升≈0.44 克
设参加反应的碳酸钙质量为 X,则
(1 分)
(1 分)
CaCO3+2HCl=CaCl2+CO2↑+H2O
44
100
X
100:44=X:0.44 克
X=1 克
0.44 克
CaCO3%=1 克/1.25 克=80%(1 分)
(4)设参加反应的稀盐酸的质量分数为 Y,则
CaCO3+2HCl=CaCl2+CO2↑+H2O
73
100
5 克 50 克 Y
100:73==5 克:50 克 Y
Y =7.3%(2 分)
(l)R 总=_U/I=8V/0.1A=80Ω
R0=80Ω—20Ω=60Ω
(2)受到的压力越大,弹簧的长度越短(2 分)
(3)模拟电路最大载重时弹簧长度为 24 厘米,20Ω/40 厘米=R1/24 厘米 R1=12Ω
I=UR=8V/(60Ω+12Ω)=0.11A(1 分)
�
故选 R3 电阻(1 分)
最大载重电流 I=U/R=8V/(5Ω+12Ω)=0.47A(1 分)
(1)非特异性(2 分)
(2)A、C(2 分)
(3)c(1 分)
(4)①P=UI=200Ah×380v/3.8h=20000W(2 分)
②v=54 千米/时=1 5 米/秒(1 分)
匀速行驶时 f=F=P /V=36000 瓦/l5 米/秒=2400 牛(1 分)
�








 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc