2023 年新课标卷高考化学真题及答案
1. 化学在文物的研究和修复中有重要作用。下列说法错误的是
A. 竹简的成分之一纤维素属于天然高分子
B. 龟甲的成分之一羟基磷灰石属于
无机物
C. 古陶瓷修复所用的熟石膏,其成分为 Ca(OH)2
D. 古壁画颜料中所用的铁红,其成分
为 Fe2O3
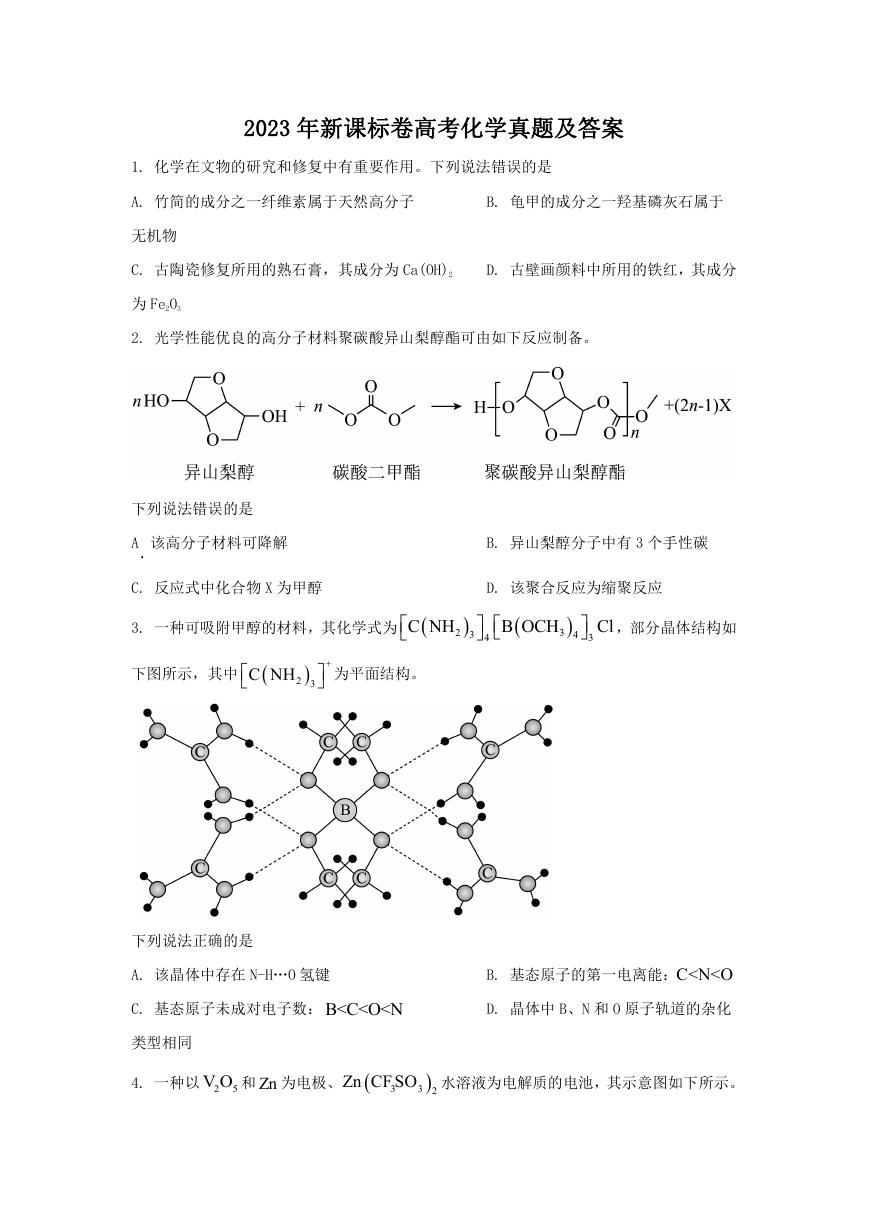
2. 光学性能优良的高分子材料聚碳酸异山梨醇酯可由如下反应制备。
下列说法错误的是
A. 该高分子材料可降解
C. 反应式中化合物 X 为甲醇
3. 一种可吸附甲醇的材料,其化学式为
C NH
B. 异山梨醇分子中有 3 个手性碳
D. 该聚合反应为缩聚反应
3
4
2
B OCH
3
4 3
Cl
,部分晶体结构如
下图所示,其中
C NH
2 3
+
为平面结构。
下列说法正确的是
A. 该晶体中存在 N-H…O 氢键
C. 基态原子未成对电子数: B
放电时, 2+Zn 可插入 2
5V O 层间形成 x
Zn V O nH O
2
5
2
。下列说法错误的是
A. 放电时 2
5V O 为正极
B. 放电时 2+Zn 由负极向正极迁移
C. 充电总反应:
2
5
2
xZn+V O +nH O=Zn V O nH O
x
2
5
2
D. 充电阳极反应:
Zn V O nH O-2xe =xZn +V O +nH O
2+
-
x
2
5
2
5
2
2
5. 根据实验操作及现象,下列结论中正确的是
实验操作及现象
结论
常温下将铁片分别插入稀硝酸和浓硝酸中,前者产生无色气体,
稀硝酸的氧化性
后者无明显现象
比浓硝酸强
取一定量 2
Na SO 样品,溶解后加入
3
BaCl 溶液,产生白色沉淀。
2
此样品中含有
选
项
A
B
C
加入浓
3HNO ,仍有沉淀
将银和
AgNO 溶液与铜和 2
3
Na SO 溶液组成原电池。连通后银表
4
面有银白色金属沉积,铜电极附近溶液逐渐变蓝
D
向溴水中加入苯,振荡后静置,水层颜色变浅
2-
4SO
Cu 的金属性比
Ag 强
溴与苯发生了加
成反应
A. A
B. B
C. C
D. D
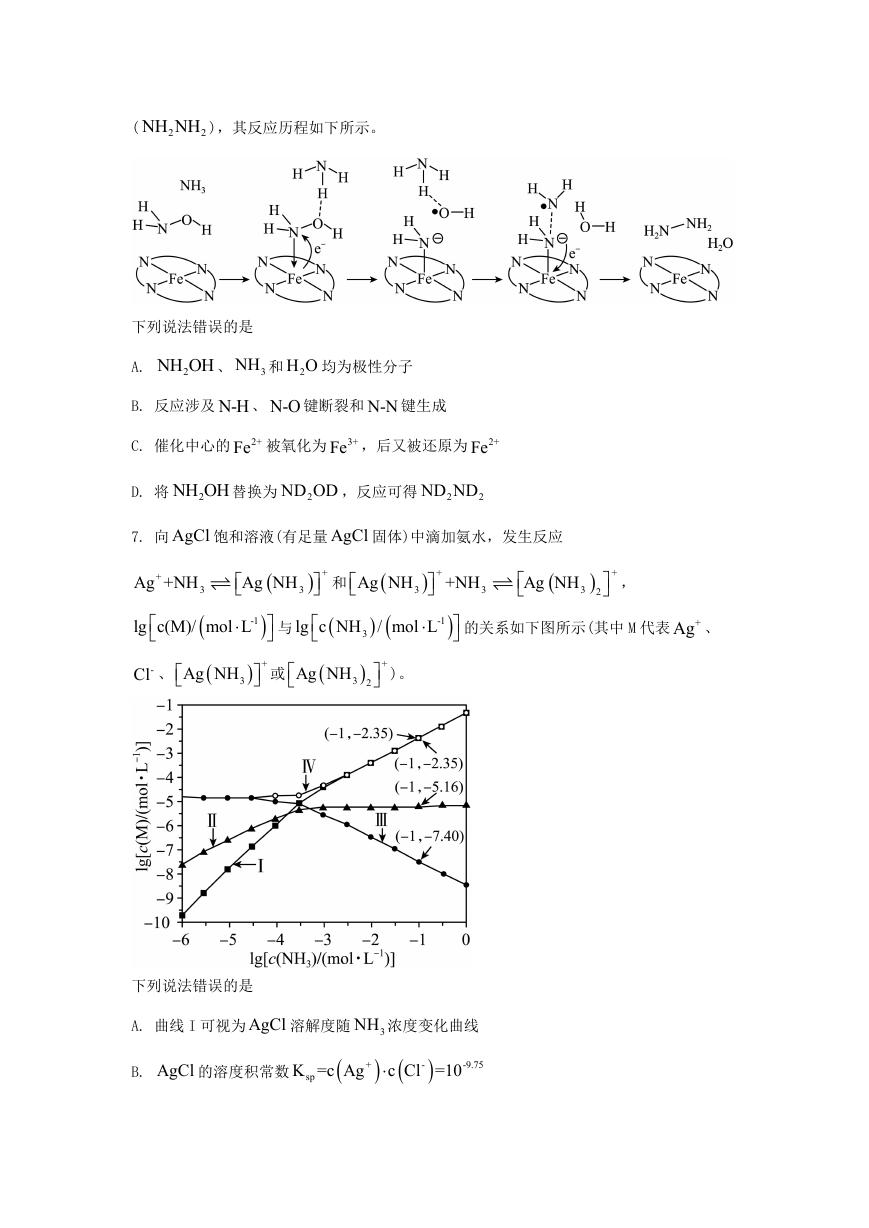
6. “肼合成酶”以其中的 2+Fe 配合物为催化中心,可将 2NH OH 与 3NH 转化为肼
�
NH NH ),其反应历程如下所示。
(
2
2
下列说法错误的是
A.
2NH OH 、 3NH 和 2H O 均为极性分子
B. 反应涉及 N-H 、 N-O 键断裂和 N-N 键生成
C. 催化中心的 2+Fe 被氧化为 3+Fe ,后又被还原为 2+Fe
D. 将 2NH OH 替换为 2ND OD ,反应可得 2
ND ND
2
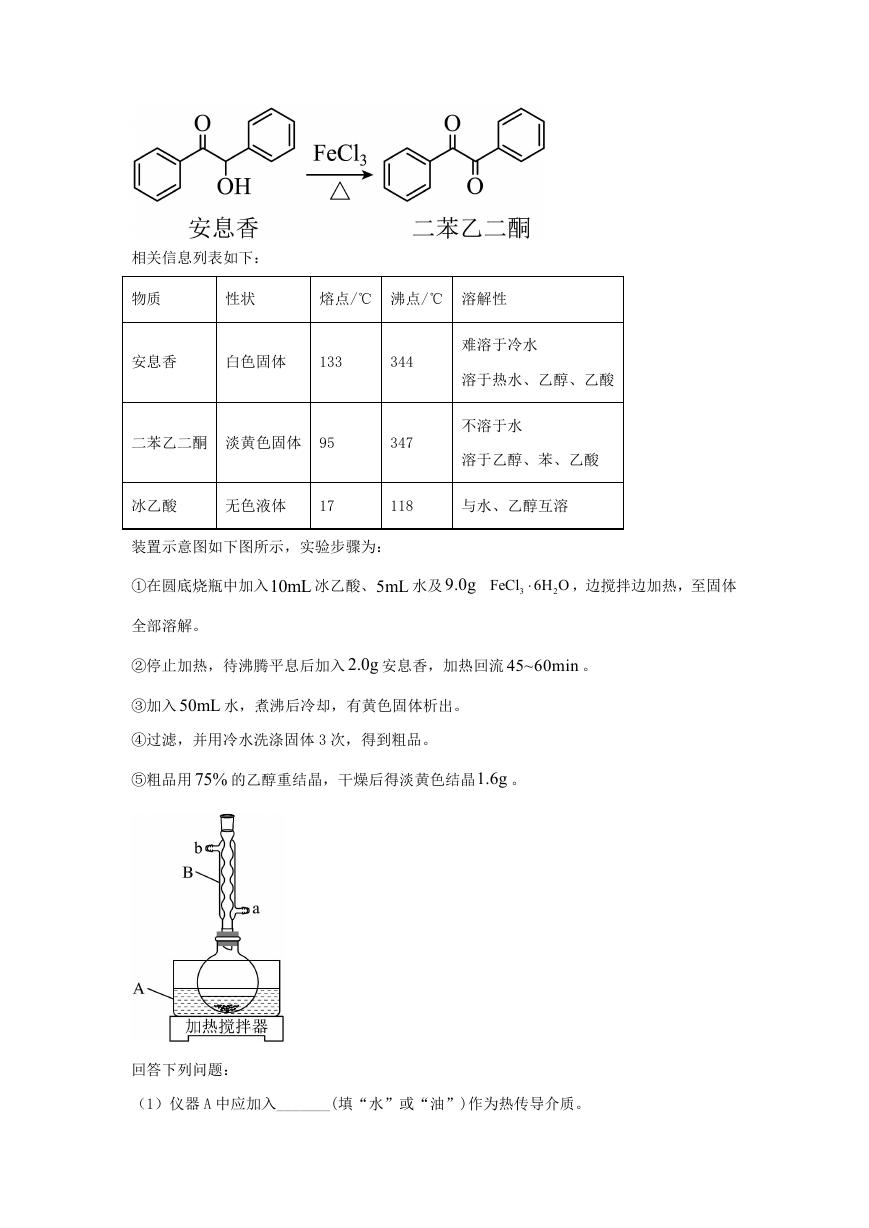
7. 向 AgCl 饱和溶液(有足量 AgCl 固体)中滴加氨水,发生反应
+
3
Ag +NH
Ag NH
-1
lg c(M)/ mol L
+
或
Ag NH
-Cl 、
与
3
Ag NH
3 2
+
)。
3
+
和
+
+NH
-1
lg c NH / mol L
的关系如下图所示(其中 M 代表 +Ag 、
Ag NH
Ag NH
,
3
3
3
3
2
+
下列说法错误的是
A. 曲线 I 可视为 AgCl 溶解度随 3NH 浓度变化曲线
B. AgCl 的溶度积常数
spK =c Ag
+
c Cl =10
-
-9.75
�
C. 反应
Ag NH
+
3
+NH
3
Ag NH
3
2
+
的平衡常数 K的值为 3.81
10
D.
c NH =0.01mol L 时,溶液中
-1
3
c Ag NH
+
2
3
>c Ag NH
+
3
>c Ag
+
8. 铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、
硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:
已知:最高价铬酸根 在酸性介质中以
回答下列问题:
Cr O 存在,在碱性介质中以 2-
4CrO 存在。
2-
7
2
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为
_______(填化学式)。
(2)水浸渣中主要有 2SiO 和_______。
(3)“沉淀”步骤调 pH 到弱碱性,主要除去的杂质是_______。
(4)“除硅磷”步骤中,使硅、磷分别以
MgSiO 和
3
MgNH PO 的形式沉淀,该步需要
4
4
控制溶液的 pH 9 以达到最好的除杂效果,若 pH<9 时,会导致_______;pH>9 时,会导
致_______。
(5)“分离钒”步骤中,将溶液 pH 调到 1.8 左右得到 2
5V O 沉淀, 2
5V O 在 pH 1 时,溶
解为 +
2VO 或 3+VO 在碱性条件下,溶解为 -
3VO 或 3-
4VO ,上述性质说明 2
5V O 具有
_______(填标号)。
A.酸性
B.碱性
C.两性
(6)“还原”步骤中加入焦亚硫酸钠(
Na S O )溶液,反应的离子方程式为_______。
2 2
5
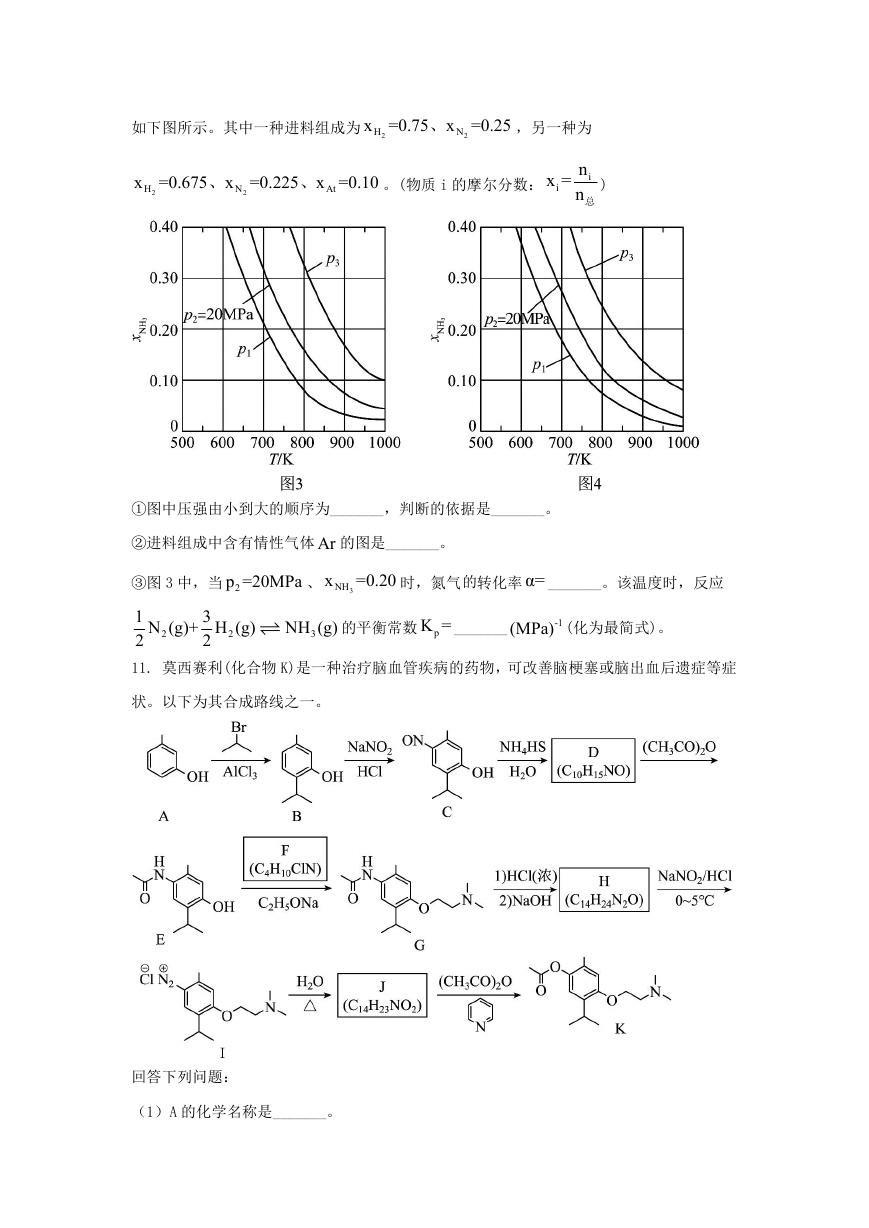
9. 实验室由安息香制备二苯乙二酮的反应式如下:
�
相关信息列表如下:
物质
性状
熔点/℃ 沸点/℃ 溶解性
安息香
白色固体
133
344
二苯乙二酮 淡黄色固体 95
347
难溶于冷水
溶于热水、乙醇、乙酸
不溶于水
溶于乙醇、苯、乙酸
冰乙酸
无色液体
17
118
与水、乙醇互溶
装置示意图如下图所示,实验步骤为:
①在圆底烧瓶中加入10mL 冰乙酸、5mL 水及 9.0g
全部溶解。
FeCl 6H O
3
2
,边搅拌边加热,至固体
②停止加热,待沸腾平息后加入 2.0g 安息香,加热回流 45~60min 。
③加入 50mL 水,煮沸后冷却,有黄色固体析出。
④过滤,并用冷水洗涤固体 3 次,得到粗品。
⑤粗品用 75% 的乙醇重结晶,干燥后得淡黄色结晶1.6g 。
回答下列问题:
(1)仪器 A 中应加入_______(填“水”或“油”)作为热传导介质。
�
(2)仪器 B 的名称是_______;冷却水应从_______(填“a”或“b”)口通入。
(3)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是_______。
(4)在本实验中,
FeCl 为氧化剂且过量,其还原产物为_______;某同学尝试改进本实验:
3
采用催化量的
FeCl 并通入空气制备二苯乙二酮。该方案是否可行_______?简述判断理由
3
_______。
(5)本实验步骤①~③在乙酸体系中进行,乙酸除作溶剂外,另一主要作用是防止_______。
(6)若粗品中混有少量未氧化的安息香,可用少量_______洗涤的方法除去(填标号)。若要
得到更高纯度的产品,可用重结晶的方法进一步提纯。
a.热水
b.乙酸
c.冷水
d.乙醇
(7)本实验的产率最接近于_______(填标号)。
a.85%
b.80%
c. 75%
d. 70%
10. 氨是最重要的化学品之一,我国目前氨的生产能力位居世界首位。回答下列问题:
(1)根据图 1 数据计算反应
1
2
N (g)+ H (g)=NH (g)
2
2
的 H _______
kJ mol
-1
。
3
3
2
(2)研究表明,合成氨反应在 Fe 催化剂上可能通过图 2 机理进行(*表示催化剂表面吸附位,
2N * 表示被吸附于催化剂表面的 2N )。判断上述反应机理中,速率控制步骤(即速率最慢步
骤)为_______(填步骤前的标号),理由是_______。
(3)合成氨催化剂前驱体(主要成分为 3
4
Fe O )使用前经 2H 还原,生成 α-Fe 包裹的 3
Fe O 。
4
已知 α-Fe 属于立方晶系,晶胞参数 a=287pm ,密度为
7.8g cm
-3
,则 α-Fe 晶胞中含有 Fe
的原子数为_______(列出计算式,阿伏加德罗常数的值为 AN )。
(4)在不同压强下,以两种不同组成进料,反应达平衡时氨的摩尔分数与温度的计算结果
�
如下图所示。其中一种进料组成为
x =0.75
H
2
、
x =0.25
N
2
,另一种为
x =0.675
H
2
、
x =0.225
N
2
、
x =0.10
At
。(物质 i 的摩尔分数:
x =
i
n
i
n总
)
①图中压强由小到大的顺序为_______,判断的依据是_______。
②进料组成中含有情性气体 Ar 的图是_______。
3NHx
=0.20 时,氮气的转化率 α= _______。该温度时,反应
③图 3 中,当 2p =20MPa 、
1
2
11. 莫西赛利(化合物 K)是一种治疗脑血管疾病的药物,可改善脑梗塞或脑出血后遗症等症
的平衡常数 pK = _______
(MPa) (化为最简式)。
-1
N (g)+ H (g)
NH (g)
3
3
2
2
2
状。以下为其合成路线之一。
回答下列问题:
(1)A 的化学名称是_______。
�
(2)C 中碳原子的轨道杂化类型有_______种。
(3)D 中官能团的名称为_______、_______。
(4)E 与 F 反应生成 G 的反应类型为_______。
(5)F的结构简式为_______。
(6)I 转变为 J 的化学方程式为_______。
(7)在 B 的同分异构体中,同时满足下列条件的共有_______种(不考虑立体异构);
①含有手性碳;②含有三个甲基;③含有苯环。
其中,核磁共振氢谱显示为 6 组峰,且峰面积比为3 3 3 2 2 1
: : : : : 的同分异构体的结构简式
为_______。
参考答案
1. C
2. B
3. A
4. C
5. C
6. D
7. B
8.
【答案】(1)Na2CrO4
(2)Fe2O3
(3)SiO 2-
3
(4)
①. 不能形成
MgNH PO 沉淀
4
4
②. 不能形成
MgSiO 沉淀
3
(6)2Cr2O 2-
7 +3S2O 2-
5 +10H+=4Cr3++6SO 2-
4 +5H2O
(5)C
9.
【答案】(1)油
(2)
①. 球形冷凝管
②. a
(3)防暴沸 (4) ①. FeCl2 ②. 可行
③. 空气可以将还原产物 FeCl2 又氧
化为 FeCl3,FeCl3 可循环参与反应
(5)抑制氯化铁水解
(6)a
�












 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc