2020 年天津高考化学试题及答案
本试卷分为第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共 100 分,考试用时 60 分钟。第Ⅰ卷 1
至 4 页,第Ⅱ卷 5 至 8 页。
答卷前,考生务必将自己的姓名、考生号、考场号和座位号填写在答题卡上,并在规定位置粘贴考试
用条形码。答卷时,考生务必将答案涂写在答题卡上,答在试卷上的无效。考试结束后,将本试卷和答题
卡一并交回。
祝各位考生考试顺利!
注意事项:
第 I 卷
1.每题选出答案后,用铅笔将答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选
涂其他答案标号。
2.本卷共 12 题,每题 3 分,共 36 分。在每题给出的四个选项中,只有一项是最符合题目要求的。
以下数据可供解题时参考:
相对原子质量:H1
O16
S32
Co 59
Cu 64
Zn 65
Ba 137
1.在全国人民众志成城抗击新冠病毒期间,使用的“84 消毒液”的主要有效成分是
A.NaOH
B.NaCl
C. NaClO
D. Na2CO3
2.晋朝葛洪的《肘后备急方》中记载:“青蒿一握,以水二升渍,绞取汁,尽服之……”,受此启发为人
类做出巨大贡献的科学家是
A.屠呦呦 B.钟南山 C.侯德榜
D.张青莲
3.下列说法错误的是
A.淀粉和纤维素均可水解产生葡萄糖
B.油脂的水解反应可用于生产甘油
C.氨基酸是组成蛋白质的基本结构单元
D.淀粉、纤维素和油脂均是天然高分子
4.下列离子方程式书写正确的是
A.CaCO3 与稀硝酸反应: 2
3
CO 2H H O CO
2
2
B.FeSO4 溶液与溴水反应: 2
2Fe
Br
2
3
2Fe
2Br
C.NaOH 溶液与过量 H2C2O4 溶液反应:
H C O 2OH C O 2H O
2
4
2
2
4
2
2
D.C6H5ONa 溶液中通入少量 CO2:
2
2C H O CO H O 2C H OH CO
3
6
5
2
2
6
5
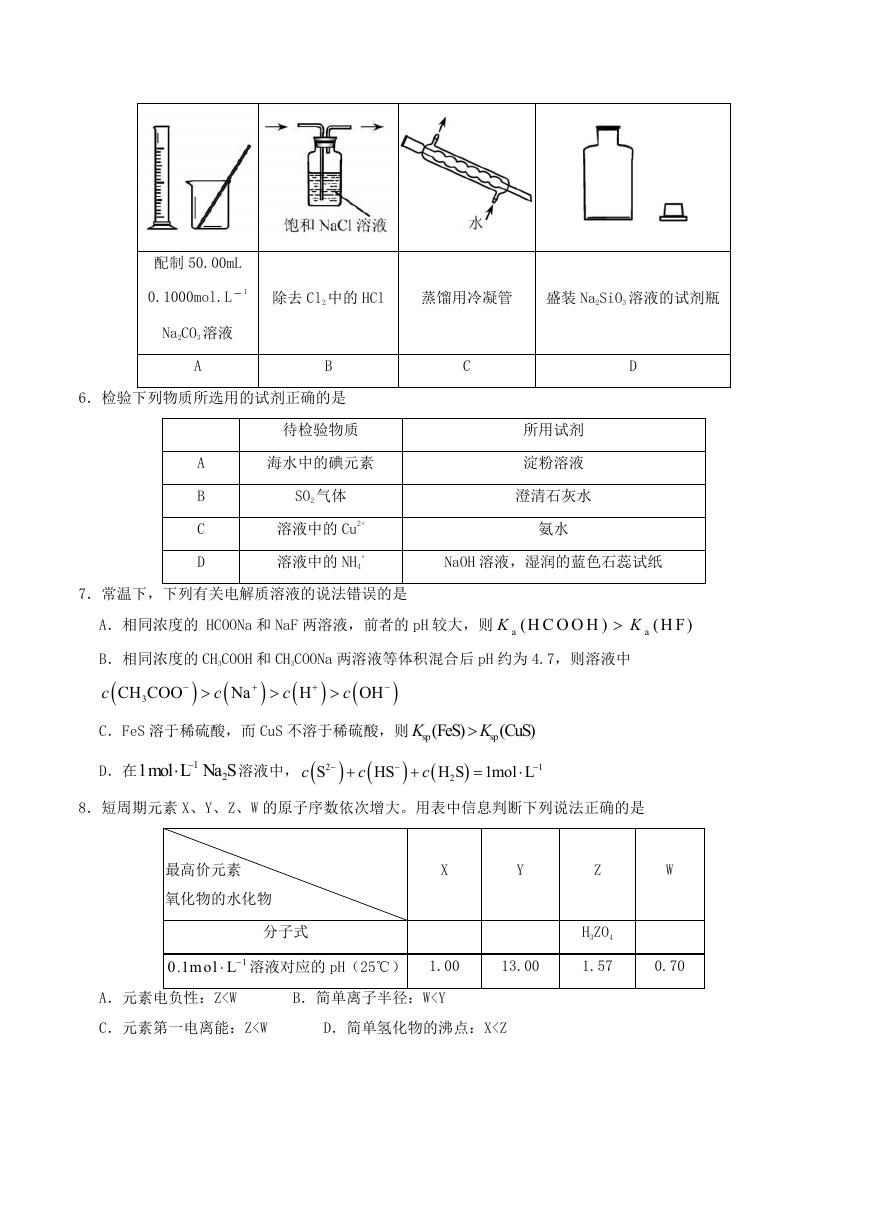
5.下列实验仪器或装置的选择正确的是
�
配制 50.00mL
0.1000mol.L−1
Na2CO3 溶液
除去 Cl2 中的 HCl
蒸馏用冷凝管
盛装 Na2SiO3 溶液的试剂瓶
A
B
C
D
6.检验下列物质所选用的试剂正确的是
待检验物质
海水中的碘元素
SO2 气体
溶液中的 Cu2+
溶液中的 NH4
+
A
B
C
D
所用试剂
淀粉溶液
澄清石灰水
氨水
NaOH 溶液,湿润的蓝色石蕊试纸
7.常温下,下列有关电解质溶液的说法错误的是
K
A.相同浓度的 HCOONa 和 NaF 两溶液,前者的 pH 较大,则 a
(H C O O H )
K
(H F)
a
B.相同浓度的 CH3COOH 和 CH3COONa 两溶液等体积混合后 pH 约为 4.7,则溶液中
c
3CH COO
c
Na
c
H
c
OH
K
C.FeS 溶于稀硫酸,而 CuS 不溶于稀硫酸,则 sp
(FeS)
K
sp
(CuS)
D.在
1mol L Na S
2
1
溶液中,
c
2
S
c
HS
c
H S
2
1
1mol L
8.短周期元素 X、Y、Z、W 的原子序数依次增大。用表中信息判断下列说法正确的是
最高价元素
氧化物的水化物
分子式
X
Y
Z
W
H3ZO4
1.57
0.70
13.00
0.1mol L
溶液对应的 pH(25℃) 1.00
1
A.元素电负性:Z
9.关于
的说法正确的是
A.分子中有 3 种杂化轨道类型的碳原子
B.分子中共平面的原子数目最多为 14
C.分子中的苯环由单双键交替组成
D.与 Cl2 发生取代反应生成两种产物
10.理论研究表明,在 101kPa 和 298K 下, HCN(g)
HNC(g)
异构化反应过程的能量变化如图所示。下
列说法错误的是
A.HCN 比 HNC 稳定
B.该异构化反应的
H
59.3kJ mol
1
C.正反应的活化能大于逆反应的活化能
D.使用催化剂,可以改变反应的反应热
11.熔融钠−硫电池性能优良,是具有应用前景的储能电池。下图中的电池反应为
2Na
(x=5~3,难溶于熔融硫)。下列说法错误..的是
x 放电
S
充电
Na Sx
2
A.Na2S4 的电子式为
Na [: S : S : S : S :] Na
B.放电时正极反应为
C.Na 和 Na2Sx分别为电池的负极和正极
..
..
..
..
S 2Na
x
2
2e Na Sx
2
�
D.该电池是以
12.已知
Co H O
2
2
A l O
N a
呈粉红色,
2
6
3
为隔膜的二次电池
CoCl
4
2
呈蓝色,
ZnCl
4
2
为无色。现将 CoCl2 溶于水,加入浓盐
酸后,溶液由粉红色变为蓝色,存在以下平衡:
Co H O
2
2
6
4Cl
CoCl
4
2
6H O
2
H
用该溶液做实验,溶液的颜色变化如下:
以下结论和解释正确的是
A.等物质的量的
Co H O
2
6
2
和
CoCl
4
2
中σ键数之比为 3:2
B.由实验①可推知△H<0
C.实验②是由于 c(H2O)增大,导致平衡逆向移动
D.由实验③可知配离子的稳定性:
ZnCl
2
4
CoCl
2
4
第Ⅱ卷
注意事项:
1.用黑色墨水的钢笔或签字笔将答案写在答题卡上。
2.本卷共 4 题,共 64 分
13.(15 分)Fe、Co、Ni 是三种重要的金属元素。回答下列问题:
(1)Fe、Co、Ni 在周期表中的位置为,基态 Fe 原子的电子排布式为。
(2)CoO 的面心立方晶胞如图 1 所示。设阿伏加德罗常数的值为 NA,则 CoO 晶体的密度为 g﹒cm−3:三种
元素二价氧化物的晶胞类型相同,其熔点由高到低的顺序为。
(3)Fe、Co、Ni 能与 Cl2 反应,其中 Co 和为 Ni 均生产二氯化物,由此推断 FeCl3、CoCl3 和 Cl2 的氧化性由
强到弱的顺序为,Co(OH)3 与盐酸反应有黄绿色气体生成,写出反应的离子方程式:。
�
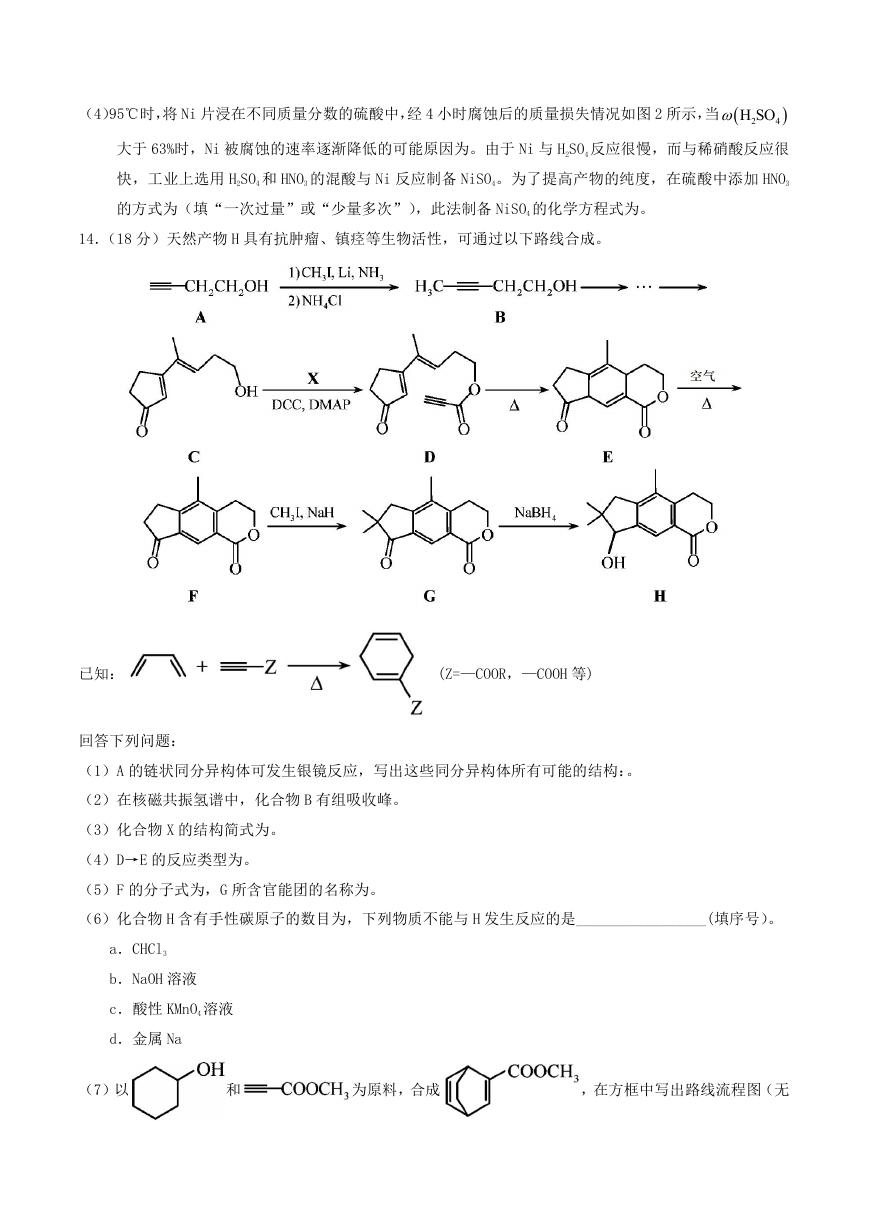
(4)95℃时,将 Ni 片浸在不同质量分数的硫酸中,经 4 小时腐蚀后的质量损失情况如图 2 所示,当
H SO
2
4
大于 63%时,Ni 被腐蚀的速率逐渐降低的可能原因为。由于 Ni 与 H2SO4 反应很慢,而与稀硝酸反应很
快,工业上选用 H2SO4 和 HNO3 的混酸与 Ni 反应制备 NiSO4。为了提高产物的纯度,在硫酸中添加 HNO3
的方式为(填“一次过量”或“少量多次”),此法制备 NiSO4 的化学方程式为。
14.(18 分)天然产物 H 具有抗肿瘤、镇痉等生物活性,可通过以下路线合成。
已知:
(Z=—COOR,—COOH 等)
回答下列问题:
(1)A 的链状同分异构体可发生银镜反应,写出这些同分异构体所有可能的结构:。
(2)在核磁共振氢谱中,化合物 B 有组吸收峰。
(3)化合物 X 的结构简式为。
(4)D→E 的反应类型为。
(5)F 的分子式为,G 所含官能团的名称为。
(6)化合物 H 含有手性碳原子的数目为,下列物质不能与 H 发生反应的是_________________(填序号)。
a.CHCl3
b.NaOH 溶液
c.酸性 KMnO4 溶液
d.金属 Na
(7)以
和
为原料,合成
,在方框中写出路线流程图(无
�
机试剂和不超过 2 个碳的有机试剂任选)。
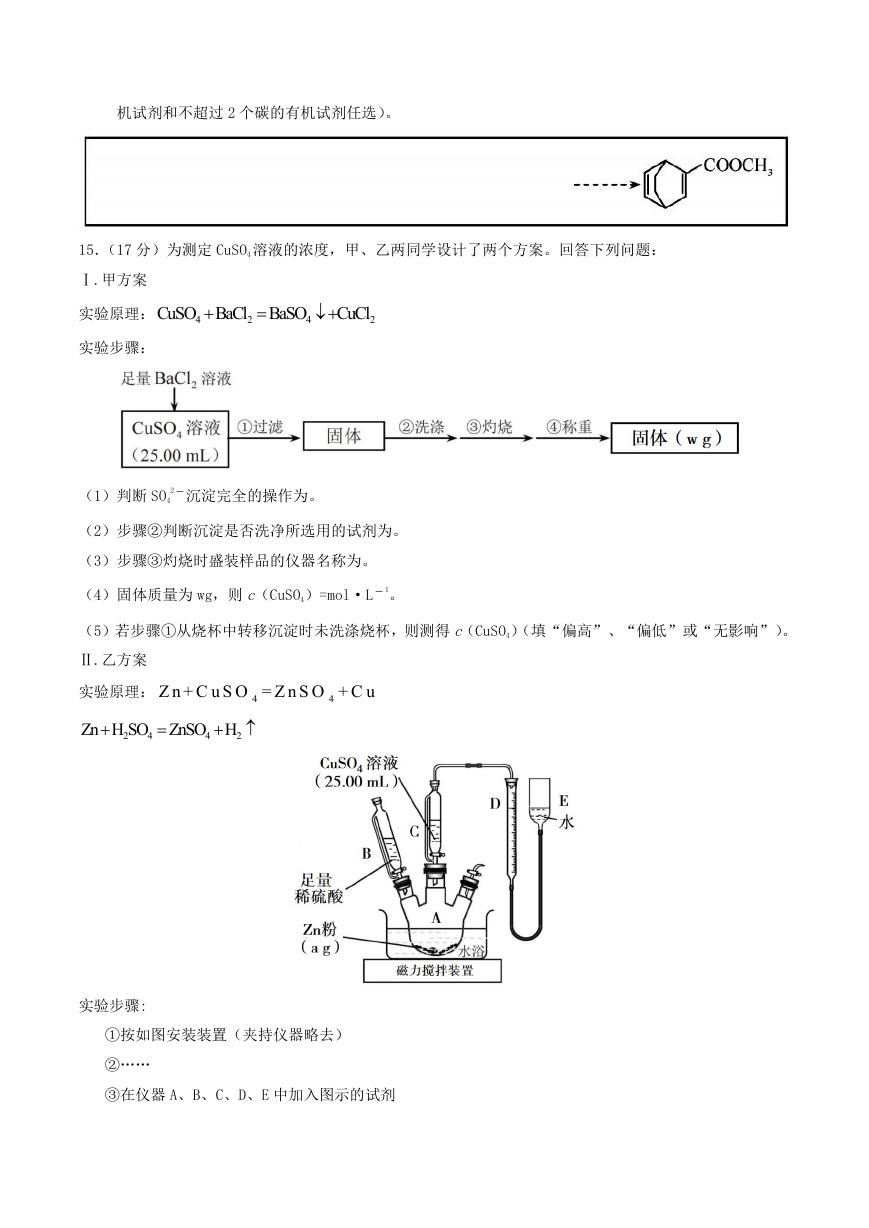
15.(17 分)为测定 CuSO4 溶液的浓度,甲、乙两同学设计了两个方案。回答下列问题:
Ⅰ.甲方案
实验原理:
实验步骤:
CuSO BaCl BaSO
4
4
2
CuCl
2
(1)判断 SO4
2−沉淀完全的操作为。
(2)步骤②判断沉淀是否洗净所选用的试剂为。
(3)步骤③灼烧时盛装样品的仪器名称为。
(4)固体质量为 wg,则 c(CuSO4)=mol·L−1。
(5)若步骤①从烧杯中转移沉淀时未洗涤烧杯,则测得 c(CuSO4)(填“偏高”、“偏低”或“无影响”)。
Ⅱ.乙方案
实验原理:
Z n + C u S O = Z n S O + C u
4
4
Zn H SO ZnSO H
2
4
2
4
实验步骤:
①按如图安装装置(夹持仪器略去)
②……
③在仪器 A、B、C、D、E 中加入图示的试剂
�
④调整 D、E 中两液面相平,使 D 中液面保持在 0 或略低于 0 刻度位置,读数并记录。
⑤将 CuSO4 溶液滴入 A 中搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生
⑥待体系恢复到室温,移动 E 管,保持 D、E 中两液面相平,读数并记录
⑦处理数据
(6)步骤②为。
(7)步骤⑥需保证体系恢复到室温的原因是(填序号)。
a.反应热受温度影响
b.气体密度受温度影响
c.反应速率受温度影响
(8)Zn 粉质量为 ag,若测得 H2 体积为 bmL,已知实验条件下
2H
1
d g L
,则
c(CuSO4)_____________mol·L−1(列出计算表达式)。
(9)若步骤⑥E 管液面高于 D 管,未调液面即读数,则测得 c(CuSO4)(填“偏高”、“偏低”或“无影响”)。
(10)是否能用同样的装置和方法测定 MgSO4 溶液的浓度:(填“是”或“否”)。
16.(14 分)利用太阳能光解水,制备的 H2 用于还原 CO2 合成有机物,可实现资源的再利用。回答下列问题:
Ⅰ.半导体光催化剂浸入水或电解质溶液中,光照时可在其表面得到产物
(1)图 1 为该催化剂在水中发生光催化反应的原理示意图。光解水能量转化形式为。
(2)若将该催化剂置于 Na2SO3 溶液中,产物之一为
2-
4SO ,另一产物为。若将该催化剂置于 AgNO3 溶液中,
产物之一为 O2,写出生成另一产物的离子反应式。
Ⅱ.用 H2 还原 CO2 可以在一定条件下合成 CH3OH(不考虑副反应)
C O (g )+ 3 H (g )
2
2
C H O H (g )+ H O (g ) Δ
< 0H
3
2
(3)某温度下,恒容密闭容器中,CO2 和 H2 的起始浓度分别为 a mol·L−1 和 3 a mol·L−1,反应平衡时,
CH3OH 的产率为 b,该温度下反应平衡常数的值为。
(4)恒压下,CO2 和 H2 的起始物质的量比为 1∶3 时,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜
时甲醇的产率随温度的变化如图 2 所示,其中分子筛膜能选择性分离出 H2O。
�
①甲醇平衡产率随温度升高而降低的原因为。
②P 点甲醇产率高于 T 点的原因为。
③根据图 2,在此条件下采用该分子筛膜时的最佳反应温度为°C。
Ⅲ.调节溶液 pH 可实现工业废气 CO2 的捕获和释放
(5) 2
3CO 的空间构型为。已知 25℃碳酸电离常数为 Ka1、Ka2,当溶液 pH=12 时,
H CO : HCO : CO
1: ______ : ______
。
c
c
c
2
3
3
2
3
化学参考答案
I 卷共 12 题,每题 3 分,共 36 分。
1
C
2
A
3
D
4
B
5
B
6
C
7
A
8
A
9
A
10
D
11
C
12
D
Ⅱ卷共 4 题,共 64 分。
13.(共 15 分)
(1)第四周期第Ⅷ族
2
1s 2s 2p 3s 3p 3d 4s 或
6
2
6
6
2
2
[A r]3d
6
2
s4
(2)
23
3 10
aN
A
3
NiO CoO FeO
C oC l >C l >FeC l
3
2
(3)
3
2Co(OH)
3
6H Cl
+2
2
2Co
Cl
2
6H O
2
(4)随 H2SO4 质量分数增加,Ni 表面逐渐形成致密氧化膜
少量多次
3Ni+3H SO 2HNO 3NiSO 2NO 4H O
或
3
2
4
4
2
2H O
2
Ni H SO 2HNO NiSO 2NO
2
4
3
4
2
14.(共 18 分)
(1) 2
H C = C H C H C H O
2
(2)4
(3)
(4)加成反应
�













 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc