2023 年甘肃高考化学真题及答案
可能用到的相对原子质量:H 1
C 12
O 16
一、选择题:本题共 13 小题,每小题 6 分,共 78 分。在每小题给出的四个选项中,只
有一项是符合题目要求的。(化学部分为第 7~13 题)
1.下列应用中涉及到氧化还原反应的是
A.使用明矾对水进行净化
B.雪天道路上撒盐融雪
C.暖贴中的铁粉遇空气放热
D.荧光指示牌被照发光
2.下列反应得到相同的产物,相关叙述错误的是
A.①的反应类型为取代反应
B.反应②是合成酯的方法之一
C.产物分子中所有碳原子共平面
D.产物的化学名称是乙酸异丙酯
3.下列装置可以用于相应实验的是
A
B
C
D
制备 2CO
A.A
分离乙醇和
乙酸
B.B
验证 2SO 酸性
测量 2O 体积
C.C
D.D
4.一种矿物由短周期元素 W、X、Y 组成,溶于稀盐酸有无色无味气体生成。W、X、Y
原子序数依次增大。简单离子 2-X 与 2+Y 具有相同的电子结构。下列叙述正确的是
A.X 的常见化合价有 -1、 -2
B.原子半径大小为 Y>X>W
C.YX 的水合物具有两性
D.W 单质只有 4 种同素异形体
5.一些化学试剂久置后易发生化学变化。下列化学方程式可正确解释相应变化的是
�
A 硫酸亚铁溶液出现棕黄色沉淀
B 硫化钠溶液出现浑浊颜色变深
C 溴水颜色逐渐褪去
D 胆矾表面出现白色粉末
6FeSO +O +2H O=2Fe SO +2Fe(OH)
4
2
2
2
2
3
4
Na S+2O =Na SO
2
2
2
4
4Br +4H O=HBrO +7HBr
2
2
4
CuSO 5H O=CuSO +5H O
4
2
4
2
A.A
B.B
C.C
D.D
6.室温钠-硫电池被认为是一种成本低、比能量高的能源存储系统。一种室温钠-硫电
池的结构如图所示。将钠箔置于聚苯并咪唑膜上作为一个电极,表面喷涂有硫黄粉末的
炭化纤维素纸作为另一电极。工作时,在硫电极发生反应:
1
2
S8+e-→
1
2
S 2
8
,
1
2
S 2
8
+e-→S 2
4
,2Na++
x
4
S 2
4
+2(1-
x
4
)e-→Na2Sx
下列叙述错误的是
A.充电时 Na+从钠电极向硫电极迁移
B.放电时外电路电子流动的方向是 a→b
C.放电时正极反应为:2Na++
x
8
S8+2e-→Na2Sx
D.炭化纤维素纸的作用是增强硫电极导电性能
7.一定温度下,AgCl 和 Ag2CrO4 的沉淀溶解平衡曲线如图所示。
�
下列说法正确的是
A.a 点条件下能生成 Ag2CrO4 沉淀,也能生成 AgCl 沉淀
B.b 点时,c(Cl-)=c(CrO 2
4
),Ksp(AgCl)=Ksp(Ag2CrO4)
C.Ag2CrO4+2Cl- 2AgCl+CrO 2
4
的平衡常数 K=107.9
D.向 NaCl、Na2CrO4 均为 0.1mol·L-1 的混合溶液中滴加 AgNO3 溶液,先产生 Ag2CrO4 沉
淀
二、非选择题:本题共 4 小题,共 58 分。(必做题:26~28 题,选做题:35-36 题)
8.元素分析是有机化合物的表征手段之一。按下图实验装置(部分装置略)对有机化合
物进行 C、H 元素分析。
回答下列问题:
(1)将装有样品的 Pt 坩埚和 CuO 放入石英管中,先_______,而后将已称重的 U 型管 c、
d 与石英管连接,检查_______。依次点燃煤气灯_______,进行实验。
(2)O2 的作用有_______。CuO 的作用是_______(举 1 例,用化学方程式表示)。
(3)c 和 d 中的试剂分别是_______、_______(填标号)。c 和 d 中的试剂不可调换,理由
是_______。
A.CaCl2
B.NaCl
C.碱石灰(CaO+NaOH)
D.Na2SO3
(4)Pt 坩埚中样品 CxHyOz反应完全后,应进行操作:_______。取下 c 和 d 管称重。
�
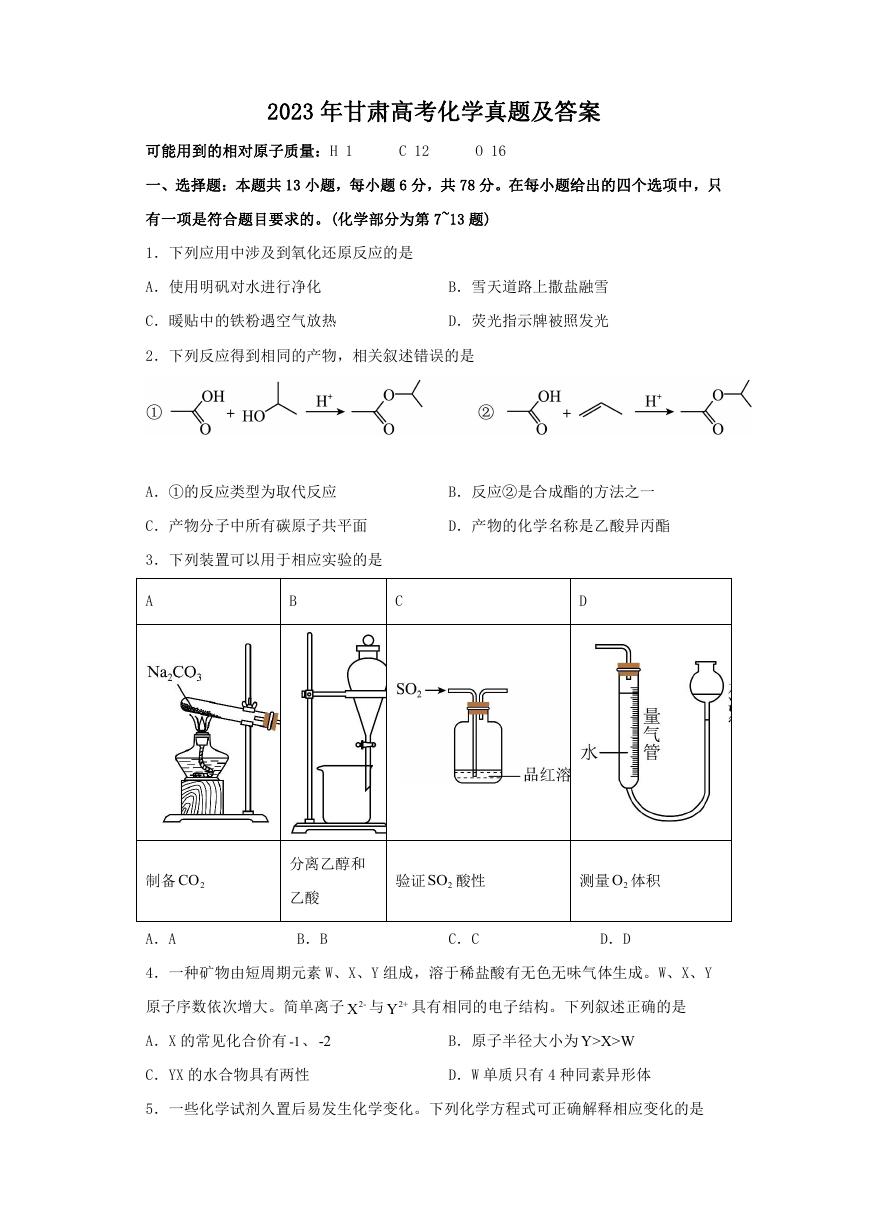
(5)若样品 CxHyOz为 0.0236g,实验结束后,c 管增重 0.0108g,d 管增重 0.0352g。质
谱测得该有机物的相对分子量为 118,其分子式为_______。
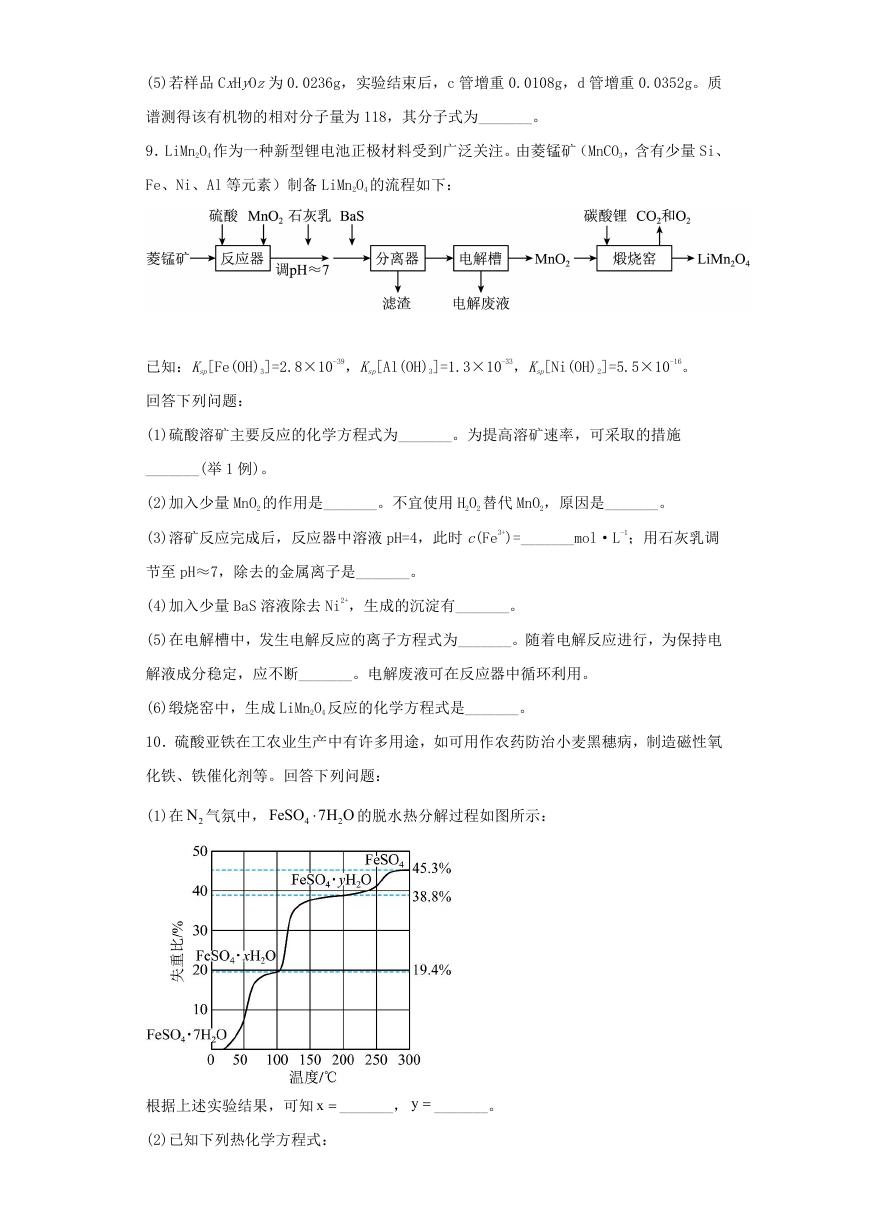
9.LiMn2O4 作为一种新型锂电池正极材料受到广泛关注。由菱锰矿(MnCO3,含有少量 Si、
Fe、Ni、Al 等元素)制备 LiMn2O4 的流程如下:
已知:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Al(OH)3]=1.3×10-33,Ksp[Ni(OH)2]=5.5×10-16。
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为_______。为提高溶矿速率,可采取的措施
_______(举 1 例)。
(2)加入少量 MnO2 的作用是_______。不宜使用 H2O2 替代 MnO2,原因是_______。
(3)溶矿反应完成后,反应器中溶液 pH=4,此时 c(Fe3+)=_______mol·L-1;用石灰乳调
节至 pH≈7,除去的金属离子是_______。
(4)加入少量 BaS 溶液除去 Ni2+,生成的沉淀有_______。
(5)在电解槽中,发生电解反应的离子方程式为_______。随着电解反应进行,为保持电
解液成分稳定,应不断_______。电解废液可在反应器中循环利用。
(6)缎烧窑中,生成 LiMn2O4 反应的化学方程式是_______。
10.硫酸亚铁在工农业生产中有许多用途,如可用作农药防治小麦黑穗病,制造磁性氧
化铁、铁催化剂等。回答下列问题:
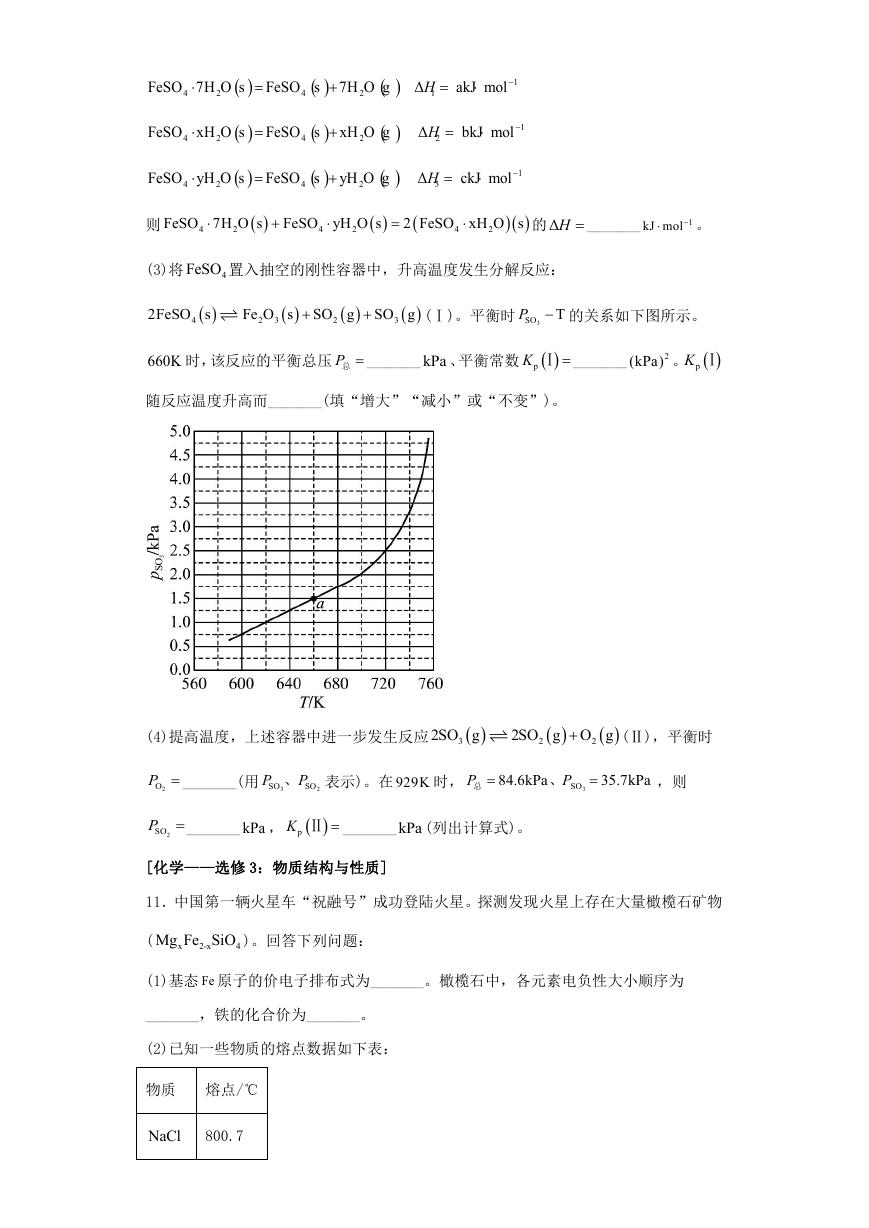
(1)在 2N 气氛中,
FeSO 7H O
4
2
的脱水热分解过程如图所示:
根据上述实验结果,可知 x _______, y _______。
(2)已知下列热化学方程式:
�
FeSO 7H O s
2
4
FeSO xH O s
2
4
FeSO yH O s
2
4
FeSO s
4
FeSO s
4
FeSO s
4
7H O g Δ
2
H
1
akJ mol
1
xH O g Δ
2
H
2
bkJ mol
1
yH O g Δ
2
H
3
ckJ mol
1
则
FeSO 7H O s
4
2
FeSO yH O s
4
2
2 FeSO xH O s
4
2
的ΔH _______
kJ mol
1
。
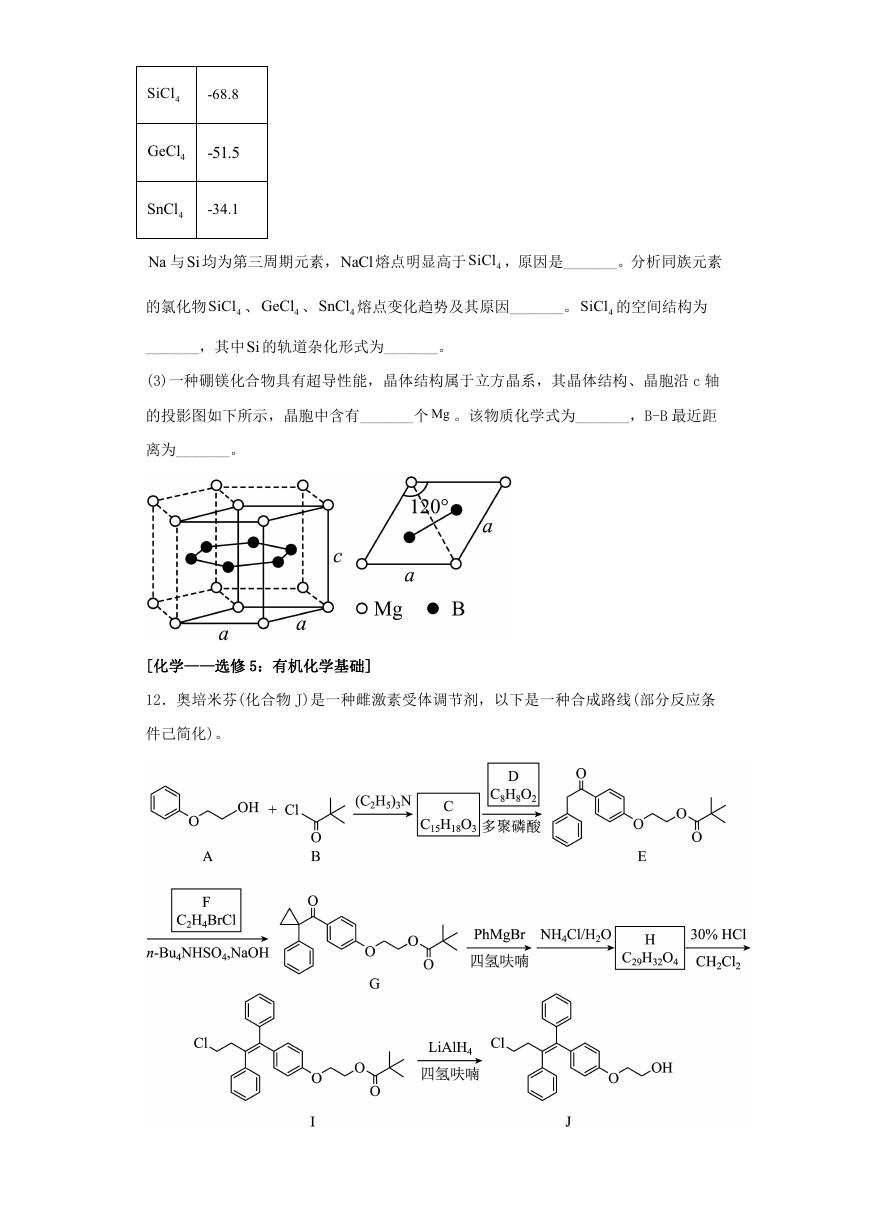
(3)将
FeSO 置入抽空的刚性容器中,升高温度发生分解反应:
4
2FeSO s
4
Fe O s
2
3
SO g
2
SO g
3
(Ⅰ)。平衡时 3SO
P 的关系如下图所示。
T
660K 时,该反应的平衡总压 P 总 _______ kPa 、平衡常数
pK
Ⅰ _______
(kPa) 。
pK Ⅰ
2
随反应温度升高而_______(填“增大”“减小”或“不变”)。
(4)提高温度,上述容器中进一步发生反应
2SO g
3
2SO g O g
2
2
(Ⅱ),平衡时
2OP _______(用 3
P
SO
P、 表示)。在 929K 时,
SO
2
P
总
84.6kPa
P
、
3SO
35.7kPa
,则
2SOP _______ kPa ,
pK
Ⅱ _______ kPa (列出计算式)。
[化学——选修 3:物质结构与性质]
11.中国第一辆火星车“祝融号”成功登陆火星。探测发现火星上存在大量橄榄石矿物
Mg Fe SiO )。回答下列问题:
(
x
2-x
4
(1)基态 Fe 原子的价电子排布式为_______。橄榄石中,各元素电负性大小顺序为
_______,铁的化合价为_______。
(2)已知一些物质的熔点数据如下表:
物质 熔点/℃
NaCl
800.7
�
SiCl
4
-68.8
4GeCl
-51.5
SnCl
4
-34.1
Na 与Si 均为第三周期元素,NaCl 熔点明显高于 4
SiCl ,原因是_______。分析同族元素
的氯化物 4
SiCl 、
4GeCl 、
SnCl 熔点变化趋势及其原因_______。 4
SiCl 的空间结构为
4
_______,其中Si 的轨道杂化形式为_______。
(3)一种硼镁化合物具有超导性能,晶体结构属于立方晶系,其晶体结构、晶胞沿 c 轴
的投影图如下所示,晶胞中含有_______个 Mg 。该物质化学式为_______,B-B 最近距
离为_______。
[化学——选修 5:有机化学基础]
12.奥培米芬(化合物 J)是一种雌激素受体调节剂,以下是一种合成路线(部分反应条
件己简化)。
�
已知:
回答下列问题:
(1)A 中含氧官能团的名称是_______。
(2)C 的结构简式为_______。
(3)D 的化学名称为_______。
(4)F 的核磁共振谱显示为两组峰,峰面积比为 1∶1,其结构简式为_______。
(5)H 的结构简式为_______。
(6)由 I 生成 J 的反应类型是_______。
(7)在 D 的同分异构体中,同时满足下列条件的共有_______种;
①能发生银镜反应;②遇 FeCl3 溶液显紫色;③含有苯环。
其中,核磁共振氢谱显示为五组峰、且峰面积比为 2∶2∶2∶1∶1 的同分异构体的结构
简式为_______。
�
�












 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc