2020 山东省威海市中考化学真题及答案
一、选择(本题包括 10 小题,每小题 2 分,共 20 分。每小题只有一个选项符合题意)
1.下列过程主要发生化学变化的是
A.用水银温度计测量体温
B.用消毒液对环境进行消毒
C.佩戴口罩预防疾病传染
D.教室和宿舍经常通风
2.垃圾分类投放已成为新时尚。某同学清理教室时收集到如下垃圾:
①废纸 ②铝制易拉罐
③废口罩
④矿泉水瓶 ⑤废电池,应投入图 1 所示标志垃
圾箱的是
A.①②④
B.①②③④
C.①②③⑤
D.①②③④⑤
3.下列对物质变化的认识不正确的是
A.在物理变化中分子的能量、间隔、相互作用均不变
B.水的天然循环只发生物理变化
C.物质能否发生化学变化是由构成物质的微粒决定的
D.研究化学变化的意义在于实现物质和能量的转化
4.下列对物质的分类,不正确的是
�
A.单质
B.化合物
C.化合物
D.混合物
5.学习了化学,我们掌握了宏观辨识与微观探析物质的本领。对以下物质的辨别方法及微
观解释,不正确的是
A.用带火星木条辨别氧气与二氧化碳——氧分子能助燃,二氧化碳分子不支持燃烧
B.用氯化钡溶液辨别硝酸银溶液与硫酸钠溶液—一银离子与氯离子结合生成氯化银,钡离
子与硫酸根离子结合生成硫酸钡
C.用燃烧法辨别碳纤维与蚕丝纤维一一碳纤维由碳原子构成,蚕丝纤维由蛋白质分子构成
D.用酸碱指示剂辨别稀盐酸与氢氧化钠溶液一一盐酸中含有氢离子,氢氧化钠溶液中含有
氢氧根离子
6.下列除去物质中杂质(括号内为杂质)的方法,不正确的是
选项 物质(杂质) 除杂方法
CuO(Cu)
将物质在空气中加热
B
C
MnO2(NaCl) 将物质加水溶解,过滤,洗涤,干燥
CO(CO2)
将混合气体依次通过足量的氢氧化钠溶液和浓硫酸
�
NaCl(Na2CO3) 将物质溶解后,加适量石灰水,过滤,蒸发结晶
7.下列关于物质组成与构成的说法,不正确的是
A.原子中核外电子,特别是最外层电子,是决定原子构成物质的关键因素
B.原子在分子中的配置(原子的种类、数量和排列方式)决定了分子的种类
C.化学元素只有一百多种,却组成了所有的化学物质
D.原子得失电子变成离子后,元素的种类发生了改变
8.下列与动植物生命活动有关的说法正确的是
A.蛋白质是人体生命活动主要供能物质
B.水、空气、食物和阳光是人体生命活动所需的最基本的化学物质
C.绿色植物光合作用将无机物转化为有机物
D.用氯化铅代替氯化钠作为食品添加剂
9.氢氧化钠和碳酸钠的溶解度如表 1 所示。
氢氧化钠
碳酸钠
溶剂
20℃
40℃
20℃
40℃
水
109g
129g
21.8g
49g
酒精
17.3g
40g
难溶
难溶
表 1 氢氧化钠和碳酸钠溶解度
下列有关分析和推理不正确的是
A.氢氧化钠易溶于水和酒精
B.温度相同,同种物质在不同溶剂中溶解度不同
C.40℃碳酸钠饱和水溶液溶质质量分数为 49%
D.20℃时,将足量二氧化碳通入饱和氢氧化钠酒精溶液中,溶液变浑浊
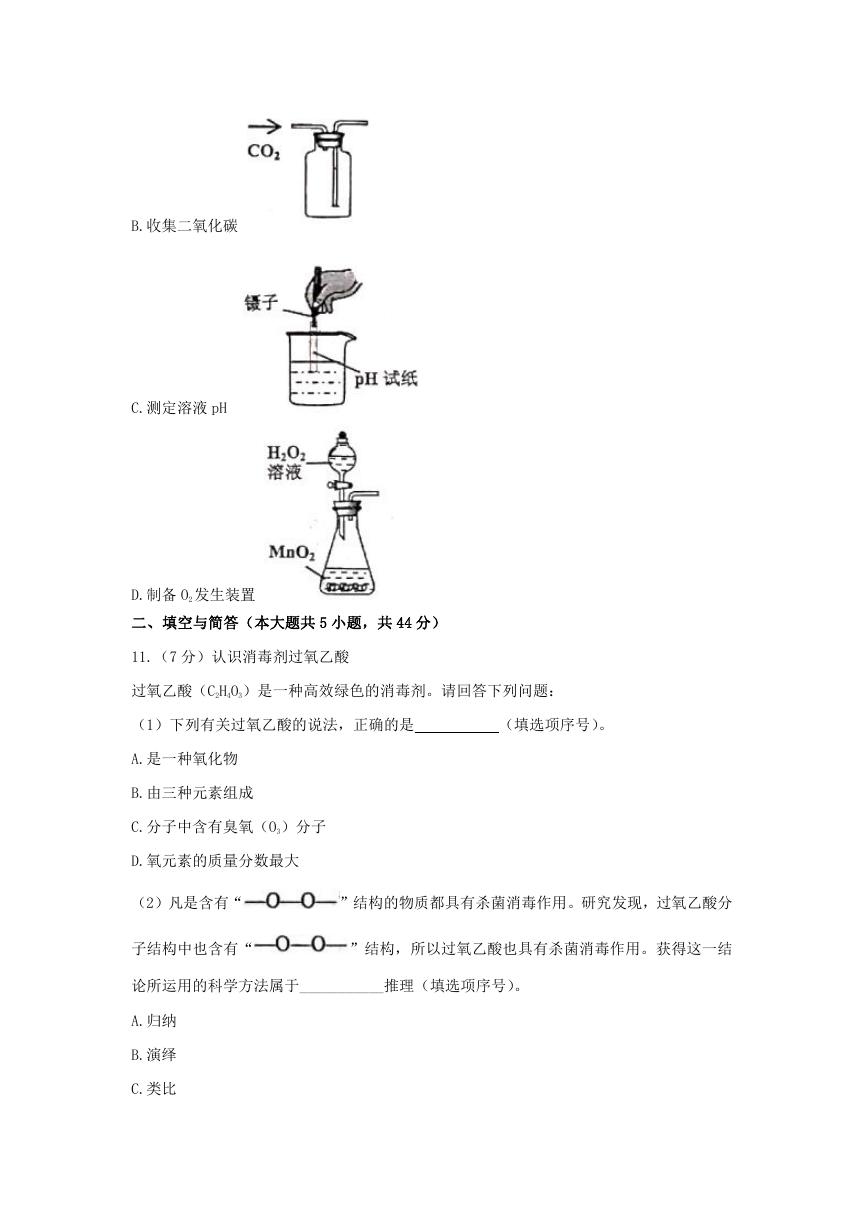
10.化学是一门以实验为基础的科学,下图所示实验或操作正确的是
A.稀释浓硫酸
�
B.收集二氧化碳
C.测定溶液 pH
D.制备 O2 发生装置
二、填空与简答(本大题共 5 小题,共 44 分)
11.(7 分)认识消毒剂过氧乙酸
过氧乙酸(C2H4O3)是一种高效绿色的消毒剂。请回答下列问题:
(1)下列有关过氧乙酸的说法,正确的是
(填选项序号)。
A.是一种氧化物
B.由三种元素组成
C.分子中含有臭氧(O3)分子
D.氧元素的质量分数最大
(2)凡是含有“
”结构的物质都具有杀菌消毒作用。研究发现,过氧乙酸分
子结构中也含有“
”结构,所以过氧乙酸也具有杀菌消毒作用。获得这一结
论所运用的科学方法属于___________推理(填选项序号)。
A.归纳
B.演绎
C.类比
�
(3)过氧乙酸具有如下性质:
A.无色易挥发液体
B.有酸性
C.有很强的腐蚀性
D.易溶于水和乙醇
E.不稳定,易分解放出氧气
F.有毒性
其中属于化学性质的有
(填选项序号)。
(4)醋酸(C2H4O2)与过氧化氢在室温下混合均匀,即可反应生成过氧乙酸和水,写出该反
应的化学方程式
。
(5)配制 1L 溶质质量分数为 0.5%的过氧乙酸溶液。现有以下物品:
水、溶质质量分数 20%的过氧乙酸溶液、量筒(规格分别为 1000mL、50mL)、塑料桶、铁桶、
木棍、口罩、护目镜、橡皮手套。
①需要 20%的过氧乙酸溶液
mL(计算时,将水、20%和 0.5%过氧乙酸溶液的密
度都近似为 1g/cm3)。
②戴好防护用品,用
mL 量筒量取所需 20%的过氧乙酸溶液倒入塑料桶中,按
比例兑水,用木棍搅拌后,盖好桶盖备用。
③ 请 你 根 据 ( 3 ) 中 过 氧 乙 酸 的 性 质 分 析 , 进 行 配 制 时 , 不 用 铁 桶 的 理 由
是
。
12.(3 分)口罩中的化学
口罩成为新冠肺炎疫情防控的必需品。
(1)佩戴口罩隔离新冠肺炎病毒,跟化学实验基本操作中的
原理相似。
(2)口罩中的鼻梁条起着将口罩固定在鼻梁上的作用,其材质常见的有:铝、塑料、镀锌
铁等。
①上述材料属于金属材料的是
。
②铁表面镀锌因其能
,从而防止铁的锈蚀。
13.(18 分)探秘物质的构成
科学理论的建立与发展是一代代科学家不懈努力的结果。人们对物质构成的认识,经历了
漫长的探索过程。
�
(1)原子的构成:汤姆森、卢瑟福等科学家都是根据实验证据进行推理,再用原子模型来
表征原子的内部结构。
①汤姆森之前,科学家对原子的认识是
。1897 年,汤姆森在实验中发现
所有原子都能释放出一种带负电的粒子,这种粒子就是
。如果你在当时
的实验现场,根据这一实验结果,你推理获得的结论是
。
②卢瑟福等科学家在汤姆森研究的基础上,根据 a粒子轰击金箔实验结论,提出了原子的
模型。
③在化学变化中,构成原子的微粒
不变,
可变。
(2)分子的构成:十九世纪初,科学家们提出早期的分子学说,部分观点如下:
观点 1:一切物质都是由分子构成,分子是由原子构成。
观点 2:单质分子由相同种类原子组成,化合物分子由不同种类原子组成。
观点 3:分子不能用物理方法分割,化学方法可使它解离。
观点 4:分子质量等于组成它的原子质量总和。
根据以上材料回答问题:
1 按现代分子理论,观点 1 是否正确?
2 从元素角度谈谈你对观点 2 的认识
。
。
3 根据观点 3,从微观角度分析“氢气和氧气反应生成水”,反应中发生改变的微粒是
_____________ ( 用 符 号 表 示 , 下 同 ) , 不 变 的 微 粒 是
________________________________。
④原子、分子质量很小,为计算和使用方便引入相对原子质量,结合观点 4 判断下列说法
正确的是______________(填字母序号)。
A.相对原子质量是采用以小比小使数值变大的计量原理
B.相对原子质量是一个原子质量与一个碳-12 原子质量 1/12 的比值
C.相对分子质量等于组成它的所有原子的相对原子质量之和
D.1 个分子质量一定大于 1 个原子质量
(3)离子的构成:2019 年度诺贝尔化学奖授予在可充电锂离子电池研究领域做出突出贡献
的三位科学家。
①锂 的原 子 结 构示 意 图如 图 2 所 示, 写 出 金属 锂 (Li) 与稀 盐 酸 反应 的 化学 方 程 式
___________________。
�
②某种可充电锂离子电池以钴酸锂( LiCoO2)为正极,以碳素材料为负极。在钴酸锂中钴
( Co ) 元 素 的 化 合 价 为 ______________________ 。 根 据 物 质 组 成 分 类 , 钴 酸 锂 属 于
____________________。
(4)万物皆原子,原子是构成一切化学物质的基本单元。图 3 是氢、氖、钠和氯的原子结
构示意图:
请你以氖气、氯化氢和氯化钠三种物质为例,从原子直接或间接构成物质的角度,简要谈
谈你对“原子是构成一切化学物质的基本单元”的理解。
______________________________________________________________________________
__
14.(6 分)化学与航天
2019 年 12 月 27 日长征五号系列运载火箭(以下简称“胖五”)发射成功。请回答下列问题:
(1)“胖五”两种发动机分别采用液氢、液氧做推进剂和煤油、液氧做推进剂,而旧的长
征火箭采用的推进剂是有毒的偏二甲肼(N2H4)和液态四氧化二氮(N2O4),其燃烧时还会因
泄露和不充分燃烧产生大量氮的氧化物。
①“胖五”的两种推进剂中属于可燃物的是_____________________。
②科学家发现,煤在一定条件下加氢制得煤油,称之为煤的液化,属于__________变化。
③写出煤油(以 C12H16 为例)完全燃烧的化学方程式_______________________。
④从环境保护的角度分析,“胖五”的两种发动机采用的推进剂优点是_________________。
(2)铝合金在火箭制造中被广泛应用。
�
①铝合金中的铝化学性质活泼,原因是_______________________________。
②铝在岩石圈中以化合物形式存在,工业采用电解氧化铝的方法冶炼铝,写出反应的化学
方程式_______________________。
15.(10 分)探究瓜子中二氧化硫的含量
有媒体报道:某品牌瓜子被查出二氧化硫残留量超标。为了测定购买的瓜子中二氧化硫的
含量,小莉进行以下探究活动。
(1)查阅资料
①二氧化硫是无色气体,化学性质与二氧化碳相似,但能与氧气反应。
②二氧化硫可用作干果的防腐剂。我国食品添加剂标准规定,二氧化硫在干果中残留量≤
04g/kg。
③在沸水浴加热的条件下,瓜子中的二氧化硫可以全部释放出来。
④氮气化学性质不活泼,一般条件下不和其它物质发生反应。
(2)实验小莉利用下图所示装置进行实验。
1 实 验 原 理 : 乙 装 置 用 于 吸 收 瓜 子 样 品 释 放 出 的 二 氧 化 硫 , 碱 溶 液 可 选 用
__________________,发生反应的化学方程式为______________________;丙装置的作
用 是 吸 收 氮 气 流 带 出 的 水 蒸 气 , 发 生 反 应 的 化 学 方 程 式 为
____________________________。
2 实验步骤:
第一步:在 U 型管中放入瓜子样品 500g,按图示连接好仪器,向其中通入氮气。
第二步:通入氮气一段时间后,称得乙、丙装置总质量为 458.5g。
第三步:再次连接好仪器,持续通入氮气,同时向烧杯中加入沸水给瓜子加热,至二氧化
硫释放完全。
第四步:实验结束后,称得乙、丙装置总质量为 458.6g(假定实验中不产生其它与碱溶液
�















 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc