2018 年山西省中考化学真题及答案
第Ⅰ卷 选择题(共 50 分)
可能用到的相对原子质量:H-1
N-14
O-16
Zn-65
一、选择题(本大题共 10 个小题,每小题 2 分,共 20 分。在每小题给出的四个选项中,只
有一项符合题目要求,请选出并在答题卡上将该选项涂黑。)
1. “绿水青山就是金山银山”,已成为国家意志和全民共识,建设天蓝、地绿、水清的美丽
中国,我任重而道远。下列做法与我国绿色发展理念不相符的是 ( )
A. 私挖滥采
C. 低碳出行
2. 空气是一种宝贵的自然资源,下列气体中既能支持燃烧又能供给呼吸的是 ( )
A. 氧气
C. 二氧化碳
3. 某无土栽培所需的营养液成分是含有 N、P、K、Ca 等元素的无机盐,该配方适用于苦瓜、
黄瓜、生菜的种植。可作营养液成分的是 ( )
B. 降低能耗
D. 保护生态
B. 氮气
D. 稀有气体
A. P2O5
B. KOH
C. NH4Cl
4. 规范实验操作是我们完成实验的基本保障,你认为以下操作正确的是
D. CaCO3
( )
( )
C. SO2
D. H2SO3
5. 1869 年门捷列夫编制了元素周期表。硫元素也排列其中,其化合价分别为-2、0、+4、
+6 价,依次对应的化学式错误的是
A. H2S
B. S
6. 色氨酸(C11H12N2O2)是氨基酸中的一种,在人体内含量太低会影响睡眠质量。一般可通
过食补黄豆、黑芝麻、海蟹和肉松等得以改善。有关色氨酸的叙述正确的是
A. 它的分子内含四种元素
B. 它含有氮分子
C. 它共含有 27 个原子
D. 其中的碳属于人体所需的常量元素
7. 生活中的自来水通常用氯气(Cl2)进行杀菌消毒处理,发生反应的化学方程式是 Cl2+
H2O===X+HClO,则 X 的化学式为 ( )
A. H2
8. 厉害了,我的国!我国航天技术迅猛发展,“天舟一号”与在轨运行的“天宫二号”空间
实验室首次成功交会对接,有力推动了我国空间站建设的进程。空间站里的 O2 源自电解水,
所得 H2 与 CO2 反应生成 H2O 和 CH4,该反应的微观示意图如下。依据图示,下列叙述错误
的是 ( )
( )
B. ClH
C. HCl
D. ClO2
�
第 8 题图
A. 反应前后分子种类不变
B. 原子可以构成分子
C. 反应中分子可以再分
D. 反应前后原子种类不变
9. 验证镁、铜的金属活动性顺序,下列试剂不能选用的是 ( )
A. MgSO4 溶液
C. 稀盐酸
10. 利用溶解度曲线,可以获得许多有关物质溶解度的信息。如图是 a、b 两物质的溶解度
曲线。有关叙述正确的是 ( )
B. KCl 溶液
D. ZnCl2 溶液
第 10 题图
A. a 的溶解度大于 b 的溶解度
B. 当 a 物质中混有少量 b 物质时,可以用蒸发结晶的方法除去 b
C. 10 ℃时,取相同质量的 a、b 两物质分别配成饱和溶液所需水的质量是 a 大于 b
D. 将 t ℃时 a、b 的饱和溶液升温至 40 ℃,其溶液中溶质的质量分数为 a 大于 b
第Ⅱ卷 非选择题(共 100 分)
可能用到的相对原子质量:H-1
N-14
O-16
Zn-65
二、生活、生产应用题(本大题共 5 个小题。化学方程式每空 2 分,其余每空 1 分,共 16
分。)
【关注生活现象】
11. 能源既是国家经济发展的命脉,也是国家发展战略的重要支柱。我省多地有效调整能源
结构,稳步发展安全高效的能源体系,合理利用如下三种发电方式,并取得了显著成效。
第 11 题图
(1)与 C 相比,A、B 发电的共同优点是________________(写一条)。
(2)A 的能量转化方式是把________能经过一系列变化转化成电能。
2. 食盐是重要的调味品,其主要成分的化学式是________。蒸馒头时,既能除去面团中的
酸又能使馒头变得松软,可加入小苏打,其化学式是________。
�
13. 当你漫步阿根廷的布宜诺斯艾丽斯时,会被这里精美绝伦的雕塑所吸引,“花之魂”就
是世界 10 大奇异雕塑之一(图甲),它是由钢和铝(6%~16%)加工而成的巨型“花朵”。傍晚
时分“花朵”霓虹闪烁,将城市的夜晚打扮得流光溢彩,美轮美奂。
第 13 题图
(1)钢铝加工而成的“花之魂”比铁雕塑性能优良之处________________________(写一条)。
(2)目前金属耗速过快,替代材料越来越多。列举生活中常用的一种合成材料
______________________________。
(3)图乙是铝的原子结构示意图,铝原子在化学反应中易________电子(填“得”或“失”)。
14. 在山西省人民医院消化科的宣传栏里,有这样一则宣传:
幽门螺旋杆菌——消化道传染病
检测方法(如图 2):被检者空腹,先用约 20 mL 凉开水口服一粒尿素胶囊(尿素中碳的相对
原子质量为 14)。
静坐 25 分钟后,用一次性吹气管
向二氧化碳吸收卡中吹气,再将吹完气的样品交给医生检测。
图 1
图 2
(1)观察图 1,集体就餐时,为避免疾病传播应该注意的是________________(写一条)。
(2)胶囊中尿素的相对分子质量是________。农业生产所使用的化肥中,尿素可用作________
肥。
【关注生产实际】
15. 科学精神与社会责任,是化学学科素养更高层面的价值追求。在一次实践活动中,小红
和同学们一起参观了某钢铁公司,大家对矿石选取、冶铁和炼钢的工艺流程(如图)、生铁和
钢的区别等,有了全新的认识。
�
第 15 题图
(1)用赤铁矿石冶铁的反应原理是______________________(用化学方程式表示)。
(2)分析工艺流程,三脱装置中发生反应的化学方程式是_______________(写一个)。
(3)向精炼炉中吹入氩气使钢水循环流动,各成分均匀混合,相当于化学实验中________的
作用(填一种 仪器的名称)。
(4)在钢水铸件机中,高温钢加工成钢制零件时,充入氮气的作用是________________。
三、科普阅读题(本大题共 1 个小题。每空 1 分,共 7 分。)
16. 南海——我们的“聚宝盆”
南海是中国四大海域中最大、最深、自然资源最为丰富的海区。近 30 年来,菲律宾、越南
等五国已经与西方 200 多家石油公司合作,在南海海域合作钻探了约 1380 口钻井,年石油
产量达 5000 万吨。相当于大庆油田最辉煌时的年开采量。
材料 1 油气资源:南海中南部油气地质资源量占 53%,
可采资源量占 66%,若被他国掠夺,中国海域将失去约 2/3 的可采油气资源。西沙群岛、中
沙群岛的水下有上千米的新生代沉积物,是大有希望的海底石油和天然气产地。
材料 2 矿产资源:南海蕴藏 5 万亿吨以上的锰、约 3100 亿吨镁、170 亿吨锡和铜、29 亿
吨镍及锰、8 亿吨钴、5 亿吨银、800 万吨金、60 亿吨铀等,比陆地矿产资源丰富得多。
材料 3 水产资源:南海海洋鱼类有 1500 多种,大多数种类在西、南、中沙群岛海域,很
多具有极高的经济价值。海龟、海参、龙虾、螺、贝、海带等都很丰富。
综合分析上述材料,回答下列问题:
(1)南海丰富的资源中,油气属于________(填“纯净物”或“混合物”)。对石油加热炼制
时,根据各成分的________不同可得到的产品有________________________(写一种)。
(2)天然气可压缩储存于钢瓶中,用分子的观点解释其变化____________________。
(3)材料 2 中所述锰、镁、铜等是指________(填“元素”或“原子”)。
(4)海洋鱼类、海参、龙虾富含的营养素是________。
(5)南海自古就是中国的!我们要捍卫祖国的领土、领海和资源的完整。在资源的开发利用
方面你的一点建议是__________________。
四、物质组成与变化分析题(本大题共 1 个小题。化学方程式每空 2 分,其余每空 1 分,共
6 分。)
17. 思维导图是激发大脑潜能,练就科学思维的有效方法。A~D 是初中化学常见的四种物
质,A 可用于金属除锈,B 难溶于水。它们相互之间的关系如图所示,“——”表示两种物质
之间可以相互反应,“―→”表示一种物质可生成另一种物质。分析推理,回答问题:
�
第 17 题图
(1)A 的化学式为________。A 与 D 反应的实质为__________________________________。
(2)A 生成 B 的化学方程式______________________________________。
(3)C 与 D 反应的化学方程式____________________________________。
五、实验探究题(本大题共 2 个小题。化学方程式每空 2 分,其余每空 1 分,共 15 分。)
【基本实验】
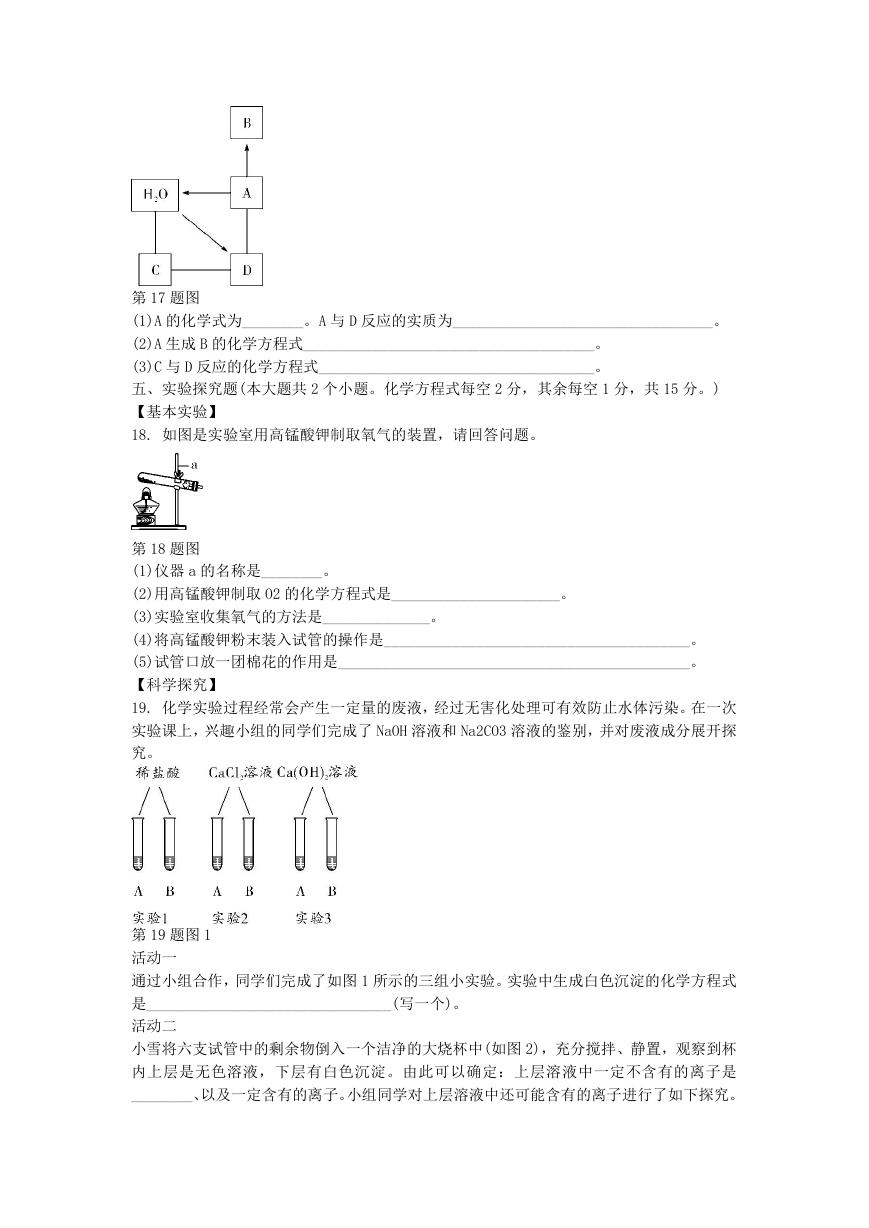
18. 如图是实验室用高锰酸钾制取氧气的装置,请回答问题。
第 18 题图
(1)仪器 a 的名称是________。
(2)用高锰酸钾制取 O2 的化学方程式是______________________。
(3)实验室收集氧气的方法是______________。
(4)将高锰酸钾粉末装入试管的操作是________________________________________。
(5)试管口放一团棉花的作用是______________________________________________。
【科学探究】
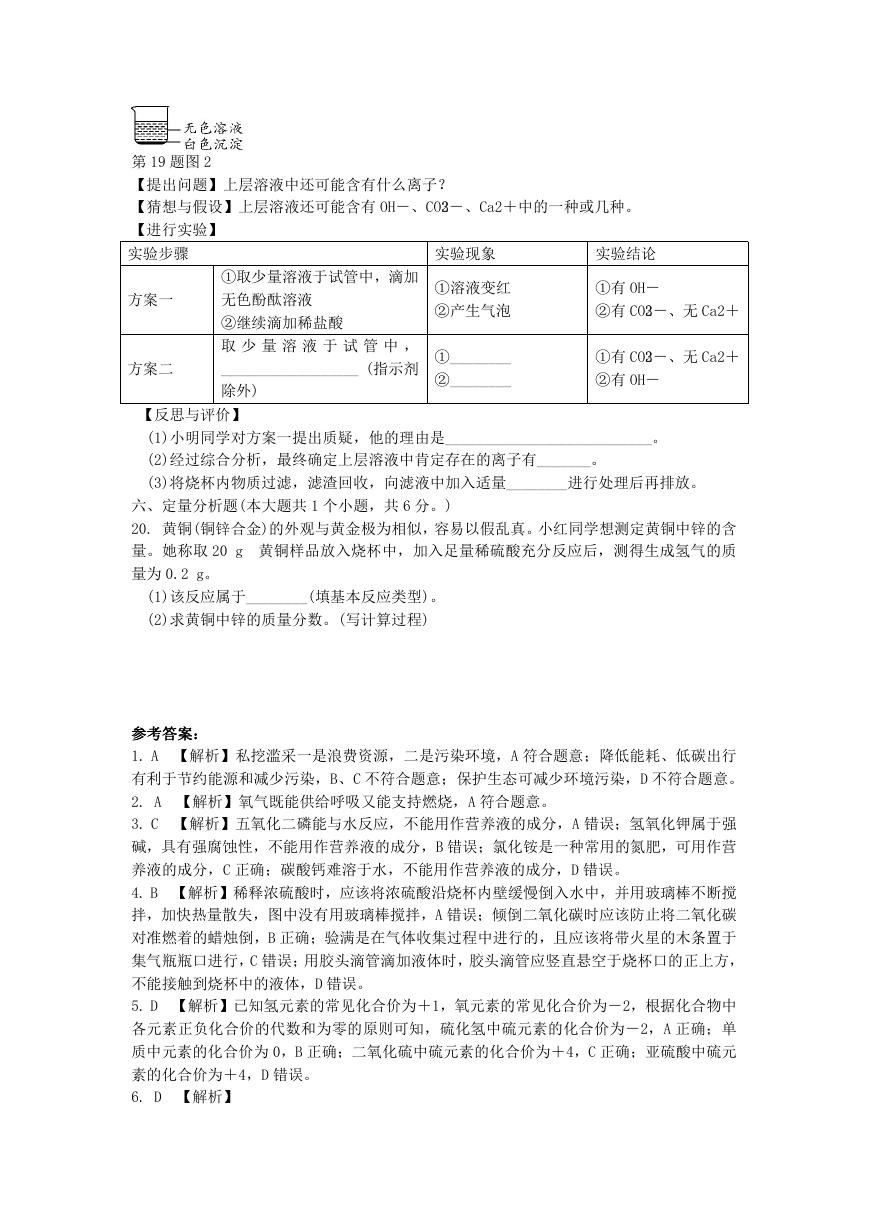
19. 化学实验过程经常会产生一定量的废液,经过无害化处理可有效防止水体污染。在一次
实验课上,兴趣小组的同学们完成了 NaOH 溶液和 Na2CO3 溶液的鉴别,并对废液成分展开探
究。
第 19 题图 1
活动一
通过小组合作,同学们完成了如图 1 所示的三组小实验。实验中生成白色沉淀的化学方程式
是________________________________(写一个)。
活动二
小雪将六支试管中的剩余物倒入一个洁净的大烧杯中(如图 2),充分搅拌、静置,观察到杯
内上层是无色溶液,下层有白色沉淀。由此可以确定:上层溶液中一定不含有的离子是
________、以及一定含有的离子。小组同学对上层溶液中还可能含有的离子进行了如下探究。
�
第 19 题图 2
【提出问题】上层溶液中还可能含有什么离子?
【猜想与假设】上层溶液还可能含有 OH-、CO2-3 、Ca2+中的一种或几种。
【进行实验】
实验步骤
方案一
方案二
实验现象
实验结论
①取少量溶液于试管中,滴加
无色酚酞溶液
②继续滴加稀盐酸
取 少 量 溶 液 于 试 管 中 ,
__________________ (指示剂
除外)
①溶液变红
②产生气泡
①________
②________
①有 OH-
②有 CO2-3 、无 Ca2+
①有 CO2-3 、无 Ca2+
②有 OH-
【反思与评价】
(1)小明同学对方案一提出质疑,他的理由是___________________________。
(2)经过综合分析,最终确定上层溶液中肯定存在的离子有_______。
(3)将烧杯内物质过滤,滤渣回收,向滤液中加入适量________进行处理后再排放。
六、定量分析题(本大题共 1 个小题,共 6 分。)
20. 黄铜(铜锌合金)的外观与黄金极为相似,容易以假乱真。小红同学想测定黄铜中锌的含
量。她称取 20 g 黄铜样品放入烧杯中,加入足量稀硫酸充分反应后,测得生成氢气的质
量为 0.2 g。
(1)该反应属于________(填基本反应类型)。
(2)求黄铜中锌的质量分数。(写计算过程)
参考答案:
1. A 【解析】私挖滥采一是浪费资源,二是污染环境,A 符合题意;降低能耗、低碳出行
有利于节约能源和减少污染,B、C 不符合题意;保护生态可减少环境污染,D 不符合题意。
2. A 【解析】氧气既能供给呼吸又能支持燃烧,A 符合题意。
3. C 【解析】五氧化二磷能与水反应,不能用作营养液的成分,A 错误;氢氧化钾属于强
碱,具有强腐蚀性,不能用作营养液的成分,B 错误;氯化铵是一种常用的氮肥,可用作营
养液的成分,C 正确;碳酸钙难溶于水,不能用作营养液的成分,D 错误。
4. B 【解析】稀释浓硫酸时,应该将浓硫酸沿烧杯内壁缓慢倒入水中,并用玻璃棒不断搅
拌,加快热量散失,图中没有用玻璃棒搅拌,A 错误;倾倒二氧化碳时应该防止将二氧化碳
对准燃着的蜡烛倒,B 正确;验满是在气体收集过程中进行的,且应该将带火星的木条置于
集气瓶瓶口进行,C 错误;用胶头滴管滴加液体时,胶头滴管应竖直悬空于烧杯口的正上方,
不能接触到烧杯中的液体,D 错误。
5. D 【解析】已知氢元素的常见化合价为+1,氧元素的常见化合价为-2,根据化合物中
各元素正负化合价的代数和为零的原则可知,硫化氢中硫元素的化合价为-2,A 正确;单
质中元素的化合价为 0,B 正确;二氧化硫中硫元素的化合价为+4,C 正确;亚硫酸中硫元
素的化合价为+4,D 错误。
6. D 【解析】
�
选项 正误 解析
A
B
C
D
×
×
×
√
元素是宏观概念,用于描述物质的宏观组成,分子是微观概念,分子由原
子构成
色氨酸能用化学式表示,属于纯净物,不含氮分子
色氨酸由分子构成,一个色氨酸分子是由 27 个原子构成
色氨酸中含有碳元素,碳是人体所需的常量元素
7. C 【解析】根据质量守恒定律:化学反应前后原子的种类和数目不变可知,一个 X 分子
是由一个氢原子和一个氯原子构成的,所以 X 的化学式为 HCl,C 正确。
8. A 【解析】
选项 正误 解析
A
B
C
D
×
√
√
√
该反应是氢气与二氧化碳反应生成水和甲烷,反应前后分子的种类发生了
变化
图中氢分子由氢原子构成,二氧化碳分子由碳原子和氧原子构成,水分子
由氢原子和氧原子构成,甲烷分子由碳原子和氢原子构成,所以原子可以
构成分子
由于反应前后分子的种类发生了变化,故化学反应中分子可以再分
由图可知反应前后原子的种类和数目都没有发生变化
9. B 【解析】判断金属活动性强弱的依据:一是金属能否与稀盐酸或稀硫酸发生置换反应,
二是一种金属能否与另一种金属的盐溶液发生置换反应。可根据铜能否与硫酸镁溶液发生置
换反应比较镁、铜的活动性强弱,A 不符合题意;钾的金属活动性比镁和铜都强,镁、铜和
氯化钾溶液均不会发生反应,故无法利用氯化钾溶液能否与镁或铜反应比较镁和铜的活动性
强弱,B 符合题意;镁可与稀盐酸反应产生氢气,铜与稀盐酸不反应,故可利用稀盐酸来验
证镁、铜的金属活动性顺序,C 不符合题意;锌的金属活动性介于镁与铜之间,根据“两金
夹一盐”可得到镁的活动性较锌强,锌的金属活动性较铜强,故镁的活动性较铜强,D 不符
合题意。
10. C 【解析】
选项 正误 解析
A
B
C
D
×
×
√
×
t ℃时两种物质的溶解度曲线相交,该温度下两种物质的溶解度相等,温
度高于 t℃时,a 的溶解度比 b 的大,温度低于 t℃时,a 的溶解度比 b 的
小
a 的溶解度曲线较 b 的陡,说明 a 的溶解度受温度影响更明显,所以 a 物
质中含有少量 b 物质时,可通过冷却热的饱和溶液(或降温结晶)的方法除
去 b
10 ℃时 a 的溶解度比 b 的小,该温度下用等质量的两种物质分别配制成各
自的饱和溶液需水的质量是 a 大于 b
a、b 的溶解度都随温度升高而增大,所以将两种物质的饱和溶液升温都会
变成各自的不饱和溶液,溶液的溶质质量分数不变,由于 t ℃时两种物质
的溶解度相等,该温度下两种物质的饱和溶液中溶质质量分数相等,所以
将 t ℃时两种物质饱和溶液升温至 40 ℃时,所得溶液均为不饱和溶液,
且溶质质量分数相等
11. (2 分)(1)节约资源(或绿色环保或无废渣废气排放等合理即可)(1 分)
【解析】(1)A 是风力发电,B 是太阳能发电,C 是燃煤发电,风能和太阳能都属于可再生的
清洁能源,煤是化石能源,所以与 C 相比,A、B 的优点是节约资源,绿色环保,无污染等。
(2)风力发电是将风能经一系列变化转化为电能。
(2)风(1 分)
�
NaHCO3(1 分)
(3)失(1 分)
(2)塑料(或合
12. (2 分)NaCl(1 分)
【解析】食盐的主要成分是氯化钠,氯化钠的化学式为 NaCl;小苏打是碳酸氢钠的俗称,
碳酸氢钠的化学式为 NaHCO3。
13. (3 分)(1)耐腐蚀(或不易生锈或硬度大或经久耐用)(合理即可)(1 分)
成纤维或合成橡胶或聚乙烯)(合理即可)(1 分)
【解析】(1)钢铝属于合金,其耐腐蚀能力、硬度比铁高,所以钢铝加工而成的“花之魂”
较铁雕塑具有更不易生锈,耐腐蚀能力强,经久耐用,硬度大等优点。(2)合成材料包括塑
料、合成纤维、合成橡胶,塑料种类多,如聚乙烯塑料,聚氯乙烯塑料等,合成纤维的种类
也很多,如涤纶,锦纶,芳纶等。(3)铝原子最外层有三个电子,在化学反应中铝原子易失
去电子形成阳离子。
14. (3 分)(1)用公筷(或分餐制)(合理即可)(1 分)
【解析】(1)为防止疾病传播,集体用餐时应该采取分餐制或利用公筷等就餐方式。(2)相对
分子质量是化学式中所有原子与其个数的乘积之和,故尿素的相对分子质量为 14+16+(14
+2)×2=62;常见化肥根据化肥为植物提供氮、磷、钾三种元素的情况分类,尿素只含氮、
磷、钾三种元素中的氮元素,属于氮肥。
(2)62(1 分) 氮(1 分)
高温
15. (6 分)(1)3CO+ Fe2O3 =====
2Fe+3CO2(2 分)
点燃
(2)S+O2=====
点燃
SO2 [或 4P+5O2=====
高温
2P2O5 或 Si+O2=====
SiO2(本题的反应条件写成“加热”、“高温”、“点燃”都得分,未写反
应条件扣 1 分)](2 分)
【解析】(1)赤铁矿的主要成分是三氧化二铁,用赤铁矿炼铁的反应原理用化学方程式可表
(4)做保护气(或隔绝氧气)(合理即可)(1 分)
(3)玻璃棒(1 分)
高温
示为 3CO+ Fe2O3=====
2Fe+3CO2。(2)三脱装置就是脱硫、脱磷、脱硅,原理是硫、磷、
点燃
硅与氧气反应,反应的化学方程式分别是 S+O2=====
点燃
SO2 、4P+5O2=====
2P2O5、Si+
高温
O2=====
SiO2。(3)吹入氩气的作用是使各成分混合均匀,其作用是搅拌,即相当于化学实
(3)元素(1 分)
(4)蛋白质(1 分)
验中玻璃棒的作用。(4)钢水的主要成分是铁,铁在高温条件下能与空气中的氧气反应,所
以用钢水铸件时,充入氮气的作用是隔绝氧气,作保护气,防止钢被氧化。
16. (7 分)(1)混合物(1 分) 沸点(1 分) 汽油(或柴油或石蜡或沥青等合理即可)(1 分)
(2)(压强增大,)分子间间隔变小(1 分)
(5)合理开发(或谨慎开采或有计划开采) (合理即可)(1 分)
【解析】(1)油气包括石油和天然气,属于混合物;石油的主要成分是有机物,根据不同组
分的沸点不同,通过分馏可得出汽油、柴油、煤油、石蜡、沥青等产品。(2)天然气是气体
物质,相同条件下气体物质分子间的间隔最大,容易被压缩,由于分子间存在间隔,通过加
压可使分子间的间隔变小,所以天然气可压缩储存于钢瓶中。(3)元素常用于描述物质的宏
观组成,材料 2 中所述锰、镁、铜是用于描述矿产资源的宏观组成,故指的是元素。(4)鱼、
虾中富含的营养素是蛋白质。(5)资源开发利用中应该合理开发,谨慎开采,有计划开采,
综合利用等。
17. (6 分)(1)H2SO4(或 HCl)(1 分) 氢离子与氢氧根离子生成水分子(或 H+与 OH-生成
(2)H2SO4+BaCl2=== BaSO4↓+2HCl (或 HCl+
H2O 分子或 H+与 OH-生成 H2O)(1 分)
AgNO3=== AgCl↓+HNO3)(合理即可)(2 分)
(3)CO2+Ca(OH)2=== CaCO3↓+H2O (或 SO2
+2NaOH=== Na2SO3+H2O)(合理即可)(2 分)
【解析】
�














 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc