2011 浙江省温州市中考化学真题及答案
本卷可能用到的相对原予质量有:H-1
O-l6
Na-23
Cl-35.5
卷 I
一、选择题(本题有 20 小题,每小题 4 分,共 80 分。每小题只有一个选项是正确的,不
选、多选、错选均不给分)
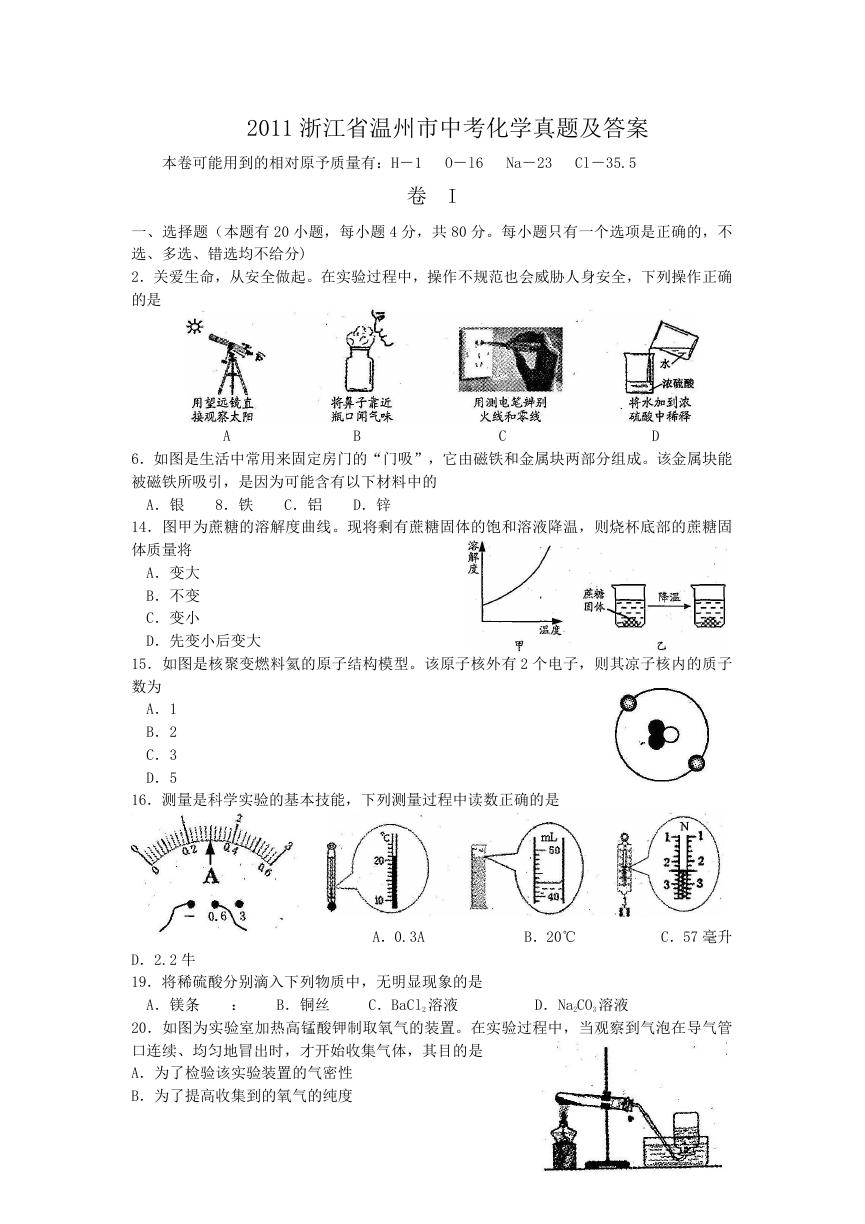
2.关爱生命,从安全做起。在实验过程中,操作不规范也会威胁人身安全,下列操作正确
的是
A
B
C
D
6.如图是生活中常用来固定房门的“门吸”,它由磁铁和金属块两部分组成。该金属块能
被磁铁所吸引,是因为可能含有以下材料中的
A.银
8.铁
C.铝
D.锌
14.图甲为蔗糖的溶解度曲线。现将剩有蔗糖固体的饱和溶液降温,则烧杯底部的蔗糖固
体质量将
A.变大
B.不变
C.变小
D.先变小后变大
15.如图是核聚变燃料氦的原子结构模型。该原子核外有 2 个电子,则其凉子核内的质子
数为
A.1
B.2
C.3
D.5
16.测量是科学实验的基本技能,下列测量过程中读数正确的是
A.0.3A
B.20℃
C.57 毫升
D.2.2 牛
19.将稀硫酸分别滴入下列物质中,无明显现象的是
A.镁条
:
B.铜丝
C.BaCl2 溶液
D.Na2CO3 溶液
20.如图为实验室加热高锰酸钾制取氧气的装置。在实验过程中,当观察到气泡在导气管
口连续、均匀地冒出时,才开始收集气体,其目的是
A.为了检验该实验装置的气密性
B.为了提高收集到的氧气的纯度
�
C.防止水槽中的水倒吸使试管破裂
D.防止高锰酸钾颗粒进入导气管
卷 Ⅱ
二、简答题(本题有 7 小题,每空 3 分,共 60 分)
23.小明在妈妈生日那天用自己的零花钱为妈妈买了蛋糕,点起蜡烛,送上祝福。
(1)蜡烛燃烧时生成了二氧化碳和水。由此推断,蜡烛中一定含有的元素有________
(2)丽两支蜡烛中间吹气,结桌囊巍两支蜡烛的火焰向中间
靠拢 ,这是 因为蜡烛 中间的 气体流 速变大 ,导致压 强变
__________。
(3)蛋糕中的营养物质进入消化系统后,主要在________
内被消化和吸收。(填写一种消化器官)
24.某晶牌变色眼镜的镜片在强光下会变成暗棕色,当光线变暗时,镜片几乎变成无色透
明。原来,变色眼镜是在普通镜片中加入了适量的溴化银和氧化铜的微晶粒。
(1)当强光照射时,溴化银分解为银和溴,使镜片呈现暗棕色。此过程中,光能转化成
________能。
(2)当光线变暗时,银和溴(Br2)在氧化铜的催化作用下,重
新化合生成溴化银(AgBr),镜片的颜色变浅。该反应的化学方
程式为____________________。
(3)光进入眼球时,瞳孔根据光线的强弱可进行调节。完成
这一反射活动的神经结构叫做____________。
25.受日本福岛核电站事故影响,2011 年 4 月,我国 21 个省市空气中都监测到微量的人工
放射性元素铯(CS)。小明对铯元素产生好奇,查阅资料得到如下信息:
(1)铯单质色白质软、熔点低,在空气中能迅速氧化生成氧化铯,铯不与氮气反应,但在
高澄下能与氢气反应。根据以上信息,请写出铯单质的一种化学性质:____________
(2)自然界中铯主要以氯化铯(CsCl)存在。其中氯的化合价是一 l 价,则氧化铯的化学式
为____________。
(3)未来的新型航天工具——“铯离子火箭”的原理是:铯蒸气在火箭中被“加工”成铯
离子,经磁场加速,从喷管向尾部喷射出去,由于力的作用是________的,从而使火箭获
得前进的动力。
26.在综合实践活动中,小明制作了如图所示的简易棉花糖机。取少量蔗糖置于侧壁扎有
几排小孔的易拉罐内,闭合开关,电动机带动易拉罐转动,并用酒精灯对易拉罐底部进行
加热。
(1)加热过程中,蔗糖颗粒变成液态糖浆,糖浆从易拉罐侧壁的小孔中
被甩出后,由于糖浆具有________继续前进;遇冷变成丝状糖絮,用筷子
收集到棉花糖。
(2)上述制取棉花糖的整个过程中,蔗糖发生的物态变化有__________。
(3)小明发现在操作过程中因无法改变电路中的电流大小,导致不能调
节易拉罐的专速,从而影响糖浆变成糖絮的效果。请你针对电路装置提出
一条可行的改进措施:_________。
27.为了纪念化学在自然科学领域取得的成就和贡献,联合国大会决定,将 2011 年定为“国
际化学年”,主题为“化学——人类的生活,人类的未来”。
(1)化学的魅力在于实验。小明在学校科技节上表演了“化学魔术”,他先用蘸有无色酚
�
酞的笔在白纸上写字,把纸晾干。表演时选用一种无色溶液喷洒在纸上,立即显示出红色
的字。他可以选用_________溶液。(填写一种具体物质) 。
(2)化学对人类健康作出了卓越的贡献。化学物质阿司匹林(C9H8O4)就是一种解热镇痛药,
阿司匹林中氢和氧元素的质量比是___________。
(3)食品添加剂也是一类化学物质。最近,关于食品添加剂的问题,引发了大众对食品安
全的讨论。下列属于支持使用食品添加剂的观点有_____________。(可多选)
A.世界各国都在使用食品添加剂,目前被滥用并带来危害的实际上是非法添加物(如
瘦肉精等),而不是食品添加剂。
B.食品添加剂尤其是多种添加剂的混合使用对人体是否有害,需要长期跟踪研究和毒
性试验。
C.科学使用食品添加剂能够改善食品的品质,延长保质期,让食品更安全。
D.大量研究表明,当前许多不明原因的“现代病”可能与化学食品添加剂有关。
三、实验探究题(本题有 5 小题,每空 2 分,共 30 分)
28.科学兴趣小组想研究影响过氧化氢(H2O2)分解速度的因素。在四支试管中分别加入 0.2
克二氧化锰 (MnO2)粉末,然后加入等量的不同溶质质量分数的过氧化氢溶液,观察气泡产
生的速度,记录如下:
实验次数
1
2
3
4
H2O2溶液的溶质质量分数 1% 5% 10% 15%
MnO2质量
0.2克 0.2克 0.2克 0.2克
气泡产生的速度
+
++
+++
++++
(1)该实验研究的问题是:过氧化氢分解的速度与_________的关系。
(2)为了检验产生的气体是否为氧气,请你写出检验的方法:____________________。
(3)实验完毕,可利用过滤法回收剩余溶液中的二氧化锰粉末。在过滤过程中,下列仪器不
需要的有______________。
.
A.玻璃棒
B.酒精灯
C.天平
D.烧杯
E.漏斗
30.淀粉酶的种类有多种。某科学兴趣小组从浸泡后的绿豆中提取淀粉酶溶液,为了研究
酸碱性对该淀粉酶催化作用的影响,以淀粉琼脂为材料进行实验,步骤如下:
①取 5 片大小相同的滤纸小圆片,编为 l~5 号。将其分别在五种不同成分的溶液(各溶液
成分如左下表)中浸泡后取出,按如图甲所示放置在盛有淀粉琼脂薄片的培养皿中,盖上盖
子。
滤纸编号
溶液成分
1
2
3
4
5
淀粉酶溶液
淀粉酶溶液+稀盐酸
’
淀粉酶溶液+稀碳酸钠溶液
稀盐酸
稀碳酸钠溶液
�
②将培养皿置于 37℃的恒温箱中,半小时后取出,将碘液均匀滴入培养皿中,约 l 分钟
后用清水缓缓冲去多余酌碘液。
③实验结果发现:l 号、2 号和 3 号滤纸小圆片周围出现了大小不等的清晰区(即没有变
蓝色的区域),其中 3 号周围的清晰区面积最大,4 号和 5 号周围以及其余部位均显蓝色,
如图乙所示。
______________________。
(1)为什么 1 号、2 号和 3 号滤纸小圆片周围会出现清晰区?
(2)为 了 判 断 酸 性 对 该 淀 粉 酶 催化 作 用 的 影 响 , 应 选 择 第 2 号 与 哪 几 号 进 行 对 照?
__________________________。(填写滤纸编号)
(3)实验结果表明,—垒一(选填“弱酸性”、“中性”或“弱碱性”)条件下,该淀粉酶
的催化作用最强。
31.绿色植物的呼吸作用会产生二氧化碳,小明猜惑:种子的萌发过程可能也会产生二氧
化碳,他设计了如图 的实验装置。打开 D 装置中的阀门,水位下降,空气就会依次进入
装置。
A
B
C
D
(1)A 装置的作用是_____________。
(2)如果观察到____________现象,则小明的猜想是正确的。
(3)请指出 D 装置的一个优点:_____________________。
32.某科学兴趣小组想探究风力火箭发射高度是否受
火箭的质量、箭尾空心锥体的锥角大小的影响,设计
了如图实验装置。大功率鼓风机提供风力火箭升空的
动力,推动火箭向高空发射。
兴趣小组成员制作了若干个风力火箭作品,在无
风环境中进行实验,分别记录火箭发射的高度(以楼层
高度表示)。每个作品均重复 3 次实验,计算出平均
值.,记录数据并绘制成 图甲和图乙所示的柱状图。
(1)每个作品均做 3 次实验,并取其平均值的目的是_______________。
�
(2)分析图甲可得出的结论是______________________。
(3)观察图乙发现,锥角对火箭发射高度影响不大,请分析其中的原因:_____________。
四、分析计算题(本题有 4 小题,第 33 题 6 分,第 34 题 7 分,第 35 题 8 分,第 36 题 9 分,
共 30 分)
35.在一定量的氢氧化钠稀溶液中逐渐滴加溶质质量分数毒.0.73%的稀盐酸,反应过程
中不断搅拌并及时测量不同时刻溶液的温度与 pH,记录数据如下表:
反应时间(秒)
滴入稀盐酸体积(毫升)
0
0
25
4
50
8
75
12
100
125
150
175
200
16
20
24
28
32
pH
13.2
13.0
12.7
12.4
12.1
7.0
2.0
1.6
1.3
温度(℃)
36.9
37.5
38.0
38.5
38.8
39.2
39.0
38.8
38.6
(1)观察上表发现,当反应时间在__________秒时,氢氧化钠与盐酸恰好中和。
(2)分析上表数据发现,在逐渐滴加稀盐酸的过程中,溶液的温度先升高后降低,请分析
原因:________________。
(3)结合上表中滴入稀盐酸体积与 pH 的变化数据,试计算氢氧化钠稀溶液中溶质的质量。
(稀盐酸的密度取 l.0 克/毫升;化学方程式为:NaOH+HCI=NaCl+H2O)
�
�
�
�















 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc