2021 年吉林辽源中考化学真题及答案
可能用到的相对原子质量:O-16
S-32
一、单项选择题(每小题 1 分,共 10 分)
1. 华夏造物历史悠久,《天工开物》中记载的下列造物过程涉及化学变化的是
A. 炼生铁
B. 晒海盐
C. 钉木舟
D. 织衣布
【答案】A
2. 空气成分中可用于医疗急救的是
A. 氮气
B. 氧气
C. 稀有气体
D. 二氧化碳
【答案】B
3. 下列各种“水”中属于纯净物的是
A. 矿泉水
B. 自来水
C. 湖泊水
D. 蒸馏水
【答案】D
4. 下列实验操作正确的是
A. 量取液体
B. 验满气体
C. 滴加液体
D. 测溶液 pH
【答案】B
5. 下列对物质用途的描述错误的是
A. 用生石灰作发热剂
B. 干冰用于人工降雨
C. 用氢氧化钠治疗胃酸过多
D. 碳酸氢钠用于焙制糕点
【答案】C
6. 2021 年“世界环境日”的主题是“人与自然和谐共生”。下列说法符合这一主题的是
A. 任意使用农药和化肥
C. 提倡使用可降解塑料
B. 大量开采煤和石油
D. 随意丢弃废旧电池
�
【答案】C
7. 甲醛在催化剂作用下与氧气反应的微观示意图如下、下列说法错误的是
A. 该反应中分子种类不变
B. 反应物的分子个数比为 1:1
C. 化学反应前后元素质量不变
D. 生成物是 CO2 和 H2O,减少污染
【答案】A
8. 结合 KNO3 和 NH4C1 的溶解度曲线判断,下列叙述错误的是
A. t1℃时,两种物质的溶解度相等
B. 两种物质的溶解度都随温度升高而增大
C. 升高温度可将接近饱和的 KNO3 溶液变成饱和溶液
D. 将 t2℃的饱和 NH4Cl 溶液降温到 t1℃,溶液质量减小
【答案】C
9. 下列对实验结果分析正确的是
A. 测定空气里氧气含量时,若装置漏气,会导致测定结果偏高
B. 除去粗盐中难溶性杂质的过程中,若蒸发时液体溅出,会导致产率偏低
C. 验证质量守恒定律时,若不采用密闭装置,一定会导致反应前后质量总和不相等
D. 配制一定溶质质量分数的溶液,若装瓶时洒出一部分,会导致溶质质量分数变小
【答案】B
10. 请结合图示分析,下列说法正确的是
�
A. 能实现转化①的金属也一定能和稀硫酸反应
B. 转化②只能通过铁与硫酸铜溶液
反应实现
C. 通过与 C 或 CO 发生置换反应可实现转化③
D. 反应④中能观察到溶液变为浅绿
色
【答案】A
二、填空题(每空 1 分,共 10 分)
11. 生理盐水是 0.9%的氯化钠溶液。请用化学用语填空。
(1)生理盐水中溶质的化学式为______。
(2)生理盐水中金属阳离子为______。
(3)标出 H2O 中氢元素的化合价______。
【答案】
①. NaCl
②. Na+
③.
1
2H O
12. 水在生活、生产中应用非常广泛。请回答下列问题。
(1)净水时利用活性炭的______性除去臭味。
(2)除去水中不溶性杂质的操作是______。
(3)生活中可用______区分软水和硬水。
【答案】
①. 吸附
②. 过滤
③. 肥皂水
13. 请根据如图回答下列问题。
(1)图中 a=______。
(2)碳的相对原子质量为______。
(3)硅原子核外有______个电子层。
(4)碳元素和硅元素的化学性质______。(填“相似”或“不相似”)
�
【答案】
①. 6
②. 12.01
③. 3
④. 相似
三、简答题(每空 1 分,化学方程式 2 分,共 12 分)
14. 请用化学知识解释下列问题。
(1)博物馆把贵重的书画保存在充满 N2 的圆桶中,使用 N2 的原因是______。
(2)从微观角度解释,变瘪的乒乓球放在热水中又鼓起来的原因是______。
【答案】
①. N2 的化学性质不活泼
②. 气体分子间的间隔变大
15. 燃料经过一次次的变革,有效地改善了大气环境,提高了人们生活质量。
(1)从燃烧条件分析,在生活中木柴比煤容易被点燃的原因是______。
(2)在煤、石油、天然气中,比较清洁的燃料是______。
(3)氢气作为理想能源的优点之一是______。
【答案】
①. 木柴的着火点低
②. 天然气
③. 热值高(或原料广或无污染)
16. “海水稻”是一种可在海边、滩涂等盐碱地生长的特殊水稻,目前已在我国开始推广种
植。这是“杂交水稻之父”袁隆平院士留给世界的巨大遗产。
(1)水稻经加工后即成大米,大米中富含的营养素是______。
(2)盐碱地土壤溶液的 pH______7。(填“>”或“=”或“<”)
(3)“海水稻”生长过程中需要施加化肥。下列属于复合肥料的是______。
A.CO(NH2)2 B.Ca3(PO4)2 C.KNO3
【答案】
①. 糖类
②. >
③. C
17. 人类文明的发展和社会的进步与材料关系密切。请回答下列问题。
(1)有的五角钱硬币的制作材料是黄铜(铜锌合金),黄铜属于______(填“金属材料”或
“合成材料”)。
(2)黄铜的外观与黄金相似,可采用灼烧的方法来鉴别,其依据的现象是金属表面是否
______;也可用 AgNO3 溶液来鉴别,请写出其中一个反应的化学方程式______。
【 答 案 】
① . 金 属 材 料
② . 变 黑
③ . Zn+2AgNO3=Zn(NO3)2+2Ag ( 或
Cu+2AgNO3=Cu(NO3)2+2Ag)
四、实验与探究题(每空 1 分,化学方程式 2 分,共 12 分)
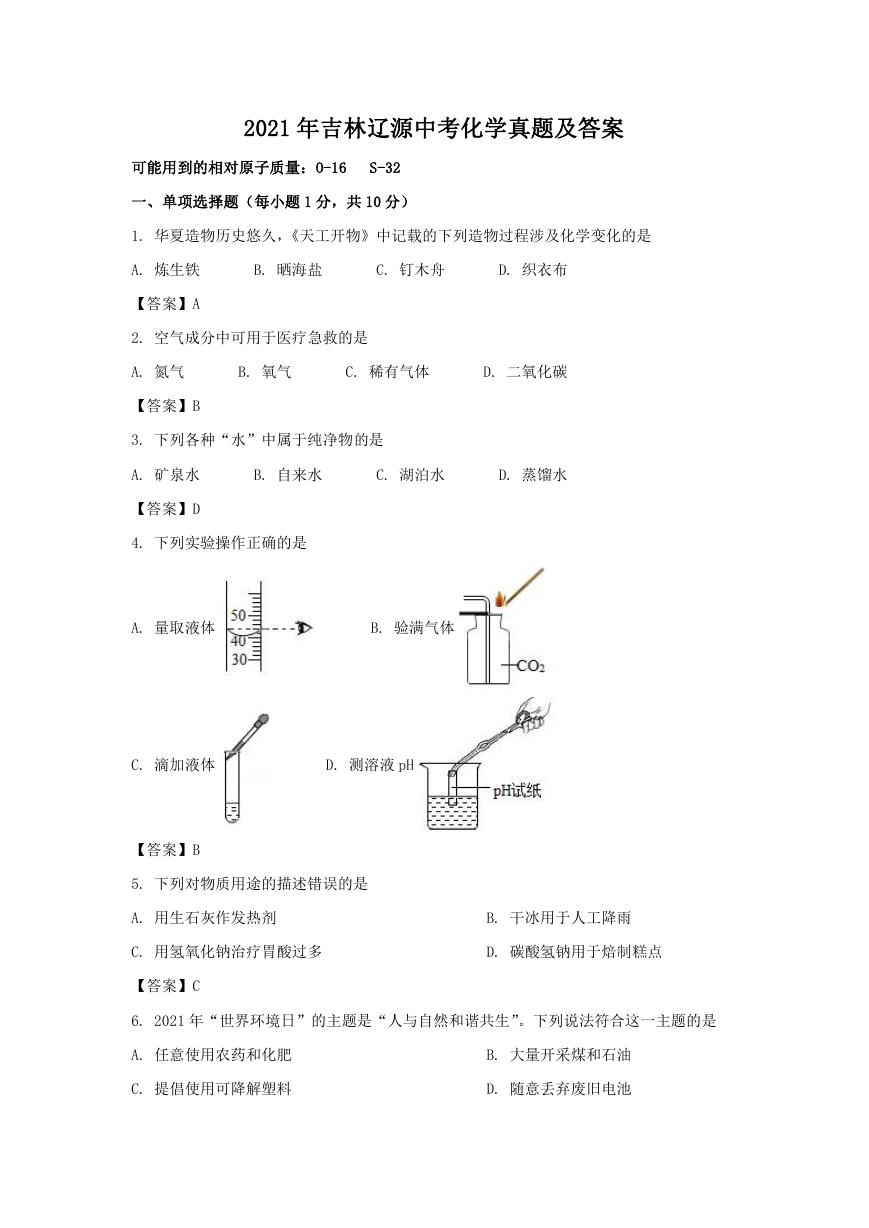
18. 根据下图回答问题。
�
(1)标号为 a 的仪器名称是______。
(2)实验室用过氧化氢溶液与二氧化锰混合制取氧气,应选择的气体发生装置是______,
该反应的化学方程式为______。
(3)若选择装置 B 和 C 组合制取某种干燥的气体,能够完成的实验是______。
①氯酸钾与二氧化锰混合加热制取氧气
②锌粒与稀硫酸反应制取氢气
③大理石与稀盐酸反应制取二氧化碳
【答案】
①. 酒精灯
②. B
③.
MnO
2
2H O
2
2
2H O O
2
2
④. ②
19. 学习了常见的酸、碱、盐后,同学们对碱的化学性质进行整理归纳,并在教师的指导下
进行如下实验活动。
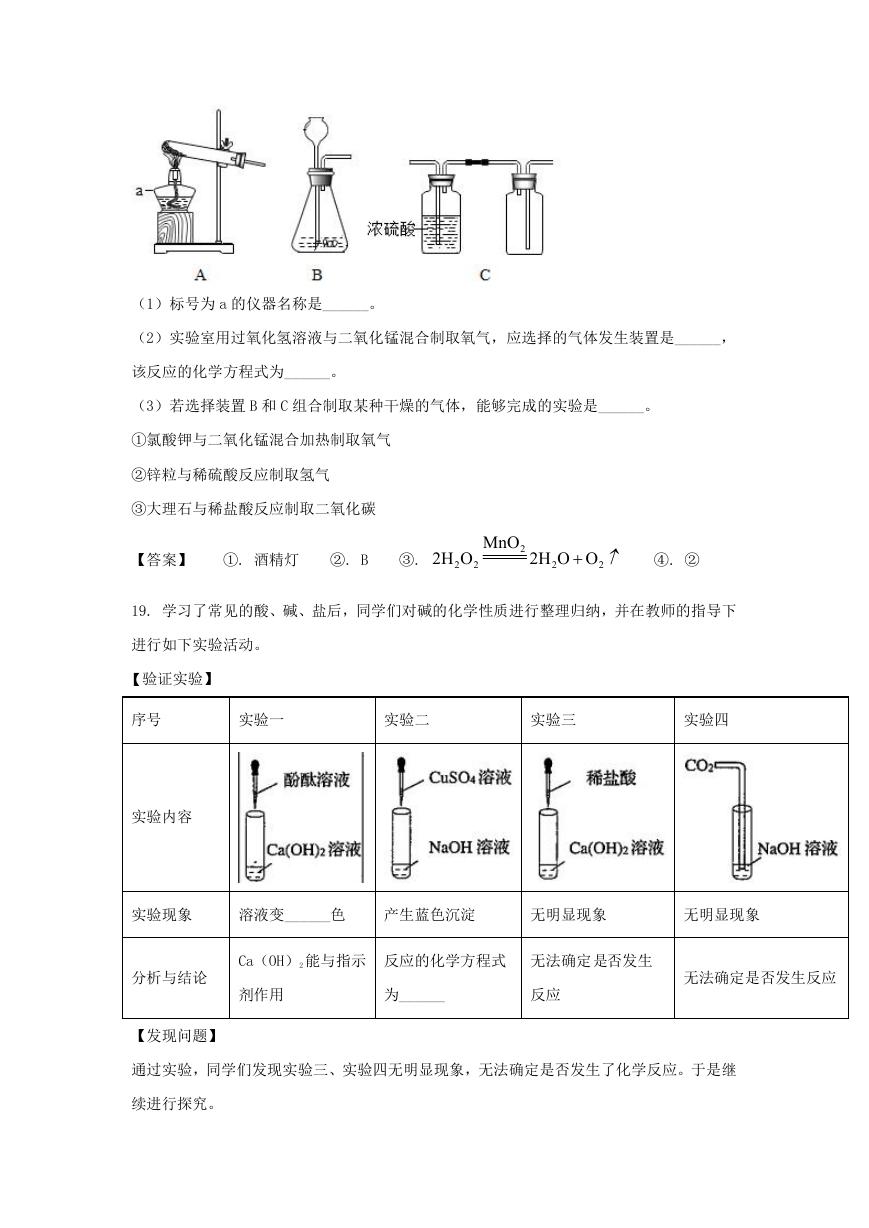
【验证实验】
序号
实验一
实验二
实验三
实验四
实验内容
实验现象
溶液变______色
产生蓝色沉淀
无明显现象
无明显现象
Ca(OH)2 能与指示
反应的化学方程式
无法确定 是否发生
剂作用
为______
反应
无法确定是否发生反应
分析与结论
【发现问题】
通过实验,同学们发现实验三、实验四无明显现象,无法确定是否发生了化学反应。于是继
续进行探究。
�
【探究实验】
Ⅰ、取少量实验三中的剩余溶液,滴加______溶液,溶液仍为无色,证明稀盐酸和 Ca(OH)
2 溶液发生了化学反应,判断依据是溶液中______完全反应了。
Ⅱ、取少量实验四中的剩余溶液,滴加______溶液(填盐类物质),观察到产生白色沉淀,
证明 CO2 和 NaOH 溶液发生了化学反应。
【拓展延伸】
同学们针对实验四又进行了如图所示的对比实验:
将充满 CO2 的两支相同的试管分别倒扣入盛有不同液体的两个烧杯中,根据试管内液面上升
的高度不同,确定二者之间发生了反应。请在图中“______”处填上适当的内容。
【总结提升】
(1)通过上述实验验证了碱溶液的化学性质。
(2)没有明显现象的化学反应,可以通过检验反应物消失(或减少)或有新物质生成的方
法证明反应发生。
【答案】
①. 红
②.
CuSO +2NaOH=Cu OH
4
2
Na SO
2
4
③. 酚酞
④. Ca(OH)2
⑤. CaCl2
⑥. 50mL 水
五、计算题(共 6 分
20. 在实验室中做硫在氧气中燃烧的实验,会生成有毒的 SO2 气体。
(1)为防止造成污染,进行实验时,可在集气瓶里预先放少量的______吸收 SO2。
(2)0.5g 硫粉在氧气中完全燃烧,理论上可生成 SO2 的质量是多少?(请利用化学方程式
计算)
【答案】(1)水(或 H2O)
(2)解:设 0.5g 硫粉在氧气中完全燃烧,理论上可生成 SO2 的质量是 x;
�
点燃
2
SO
2
64
x
0.5g
x
S +O
32
0.5g
32
64
=1g
x
=
答:0.5g 硫粉在氧气中完全燃烧,理论上可生成 SO2 的质量是 1g。
�












 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc