2020 江苏省常州市中考化学真题及答案
说明:1.本试卷 1~2 页为选择题,共 40 分,3~6 页为非选择题,共 60 分。全卷满分为 100
分。考试时间为 100 分钟。考生须将答案书写在答题卡上,写在试卷上的一律无
效。
2.答题前,考生务必将自己的姓名、考试证号填写在试卷上,并填写答题卡上的考
生信息。考试结束后,请将本试卷和答题卡一并交回。考试时不允许使用计算器。
3.可能用到的相对原子质量:Ar(H)=1
Ar(C)=12
40
Ar(Mg)=24
Ar(S)=32
Ar(Fe)=56
Ar(Cu)=64
Ar(O)=16
Ar(Cl)=35.5
Ar(Na)=23
Ar(Ca)=
一、选择题(本题包括 20 小题,共 40 分。每小题只有一个选项....符合题意)
1.下列属于化学变化的是
A.酒精挥发
B.蜡烛熔化
C.木炭燃烧
D.电灯发光
2.空气中含量最高的气体是
A.氮气
B.氧气
C.二氧化碳
D.水蒸气
3.下列物质加入水中,不能..形成溶液的是
A.蔗糖
B.硝酸钾
C.植物油
D.高锰酸钾
4.下列各物质的俗名与化学式对应不正确...的是
A.食盐:NaCl
C.碳铵:NH4HCO3
5.下列仪器不能..加热的是
B.纯碱:NaOH
D.熟石灰:Ca(OH)2
A.燃烧匙
B.试管
C.蒸发皿
D.量筒
6.下列物质中,属于氧化物的是
A.O2
B.NaNO3
C.CuO
D.KOH
7.中国居民营养与健康调查表明,人体内元素失衡是重要的致病因素。下列疾病可能与缺
铁有关的是
A.佝偻病
B.侏儒症
8.下列关于原子的叙述中,错误..的是
C.贫血症
D.大脖子病
A.原子呈电中性
C.原子由原子核与核外电子构成
B.原子是实心球体
D.原子可以构成分子
9.下列实验操作中,正确的是
A
B
C
D
10.锂电池是新型高能电池。某种锂电池的总反应可以表示为:Li+MnO2== LiMnO2,该反应
属于
A.化合反应
B.分解反应
C.置换反应
D.复分解反应
�
11.实验室制取 CO2 应选择的装置是
A.①③
D.②⑤
12.“蜂窝煤”比煤球更有利于煤的完全燃烧、提高燃烧效率,这主要是因为
B.②③
C.②④
A.降低了煤的着火点
C.提高了氧气的浓度
B.升高了煤的着火点
D.增大了煤与氧气的接触面积
13.下列物质能使紫色石蕊试液变红的是
A.氯化钠
B.碳酸钠
C.氢氧化钙
D.碳酸
14.X、Y、Z 三种金属中,只有 Z 不能和稀盐酸反应;将 Y 放入 X 的盐溶液中,Y 表面有 X
析出。则 X、Y、Z 三种金属的活动性顺序为
A.Z>Y>X
B.X>Z>Y
C.Y>Z>X
D.Y>X>Z
15.下列各组离子在溶液中一定能大量共存的是
A.Na+ Cl-
C.H+
Cl-
OH-
CO3
2-
Ca2+
B.K+
CO3
D.Na+ Fe3+ OH-
2-
16.在一定条件下,下列转化不能..由一步反应实现的是
A.Fe2O3→FeCl2
B.H2CO2→CO2
C.CuCl2→Cu
D.Mg→MgO
17.上海世博会中国国家馆以“东方之冠,鼎盛中华,天下粮仓,富庶百姓”的构思,表
达了中国文化的精神与气质,它由钢筋混凝土等建成。钢筋混凝土属于
A.金属材料
C.有机合成材料 D.复合材料
B.无机非金属材料
18.“低碳经济”已成为经济发展的重要模式,实现“低碳经济”的一种策略是节能。下列
制备氢气的方法最节能的是
A.电解水:2H2O
2H2↑+O2↑
B.焦炭与水蒸气反应:C+H2O
C.太阳光分解水:2H2O TiO2
太阳光
H2+CO
2H2↑+O2↑
D.天然气与水蒸气反应:CH4+H2O
CO+3H2
19.稀释质量分数为 98%(密度为 1.84g/ mL)的浓硫酸配制 500 mL 质量分数为 20%的稀
硫酸(密度为 1.14g/ mL),稀释时需用的水的体积约为
C.456.0 mL
A.436.8 mL
B.453.7mL
D.458.3mL
20.如右图,一木块漂浮于 X 中,向 X 中缓缓加入(或通入)少量物质 Y 后最终木块上浮,
则 X 与 Y 可能是(溶液的体积变化忽略不计)
序号
①
②
③
④
X
水
Y
食盐
氢氧化钙溶液
二氧化碳
稀硫酸
硫酸铜溶液
镁粉
铁粉
A.②④
B.①③
C.①②③
D.②③④
�
二、(本题包括 4 小题,共 18 分)
21.(5 分)(1)用化学符号表示:
①2 个氢原子:
▲
②3 个铝离子:
▲
(2)构成物质的微粒有:A.原子;B.分子;C.离子。试判断构成下列物质的微粒,并
用相应的序号..填空。
①氧气:
▲
②铁:
▲
③氯化钠:
▲
22.(4 分)用符合下列要求的物质的序号..填空:
可选物质:A.蛋白质;B.天然气;C.氢气;D.干冰;E.维生素;F.生石灰
(1)“西气东输”的“气”是:
▲
;
(2)可用于人工降雨的是:
▲
;
(3)牛奶中的主要营养物质是:
▲
;
(4)溶于水时显著放热的是:
▲
。
23.(5 分)右图是某锌锰干电池的剖面图。
(1)锌锰干电池工作时可以将化学能转化为 ▲
能;
(2)碳棒具有
▲
性,可作为干电池的电极;
(3)MnO2 可作为实验室用双氧水制 O2 的
▲
;
(4)废旧电池中的锌可回收利用,用于实验室与稀硫酸反应制取氢气。写出该反应的
化学方程式:
▲
。
24.(4 分)甲、乙两种固体的溶解度曲线如右图所示。
(1)
▲
℃时,甲和乙的溶解度相等;
(2)40℃时,若将 40g 乙(不含结晶水)放入 160g 水中充分溶解,
所得溶液的溶质质量分数为 ▲ ,该溶液是 ▲ 溶液
(填“饱和”或“不饱和”);
(3)40℃时,将甲、乙两物质的饱和溶液各 100g 降温至 20℃,析
出晶体(均不含结晶水)的质量关系是:
m(甲)
▲
m(乙) (填“﹥”、“﹦”或“﹤”)。
三、(本题包括 2 小题,共 8 分)
25.(5 分)(1)磁铁矿的主要成分是:
▲
;(填化学式)
(2)写出 CO 与 Fe2O3 在高温条件下反应的化学方程式:
▲
;
(3)高炉炼铁得到的主要产品是
▲
;(填序号)
A.纯铁
B.生铁
C.钢
(4)铁生锈的主要条件是铁与水和
▲
直接接触。
26.(3 分)16g Fe2O3 与 184g 稀 H2SO4 恰好完全反应,求所得 Fe2(SO4)3 溶液的溶质质量分数。
�
四、(本题包括 2 小题,共 16 分)
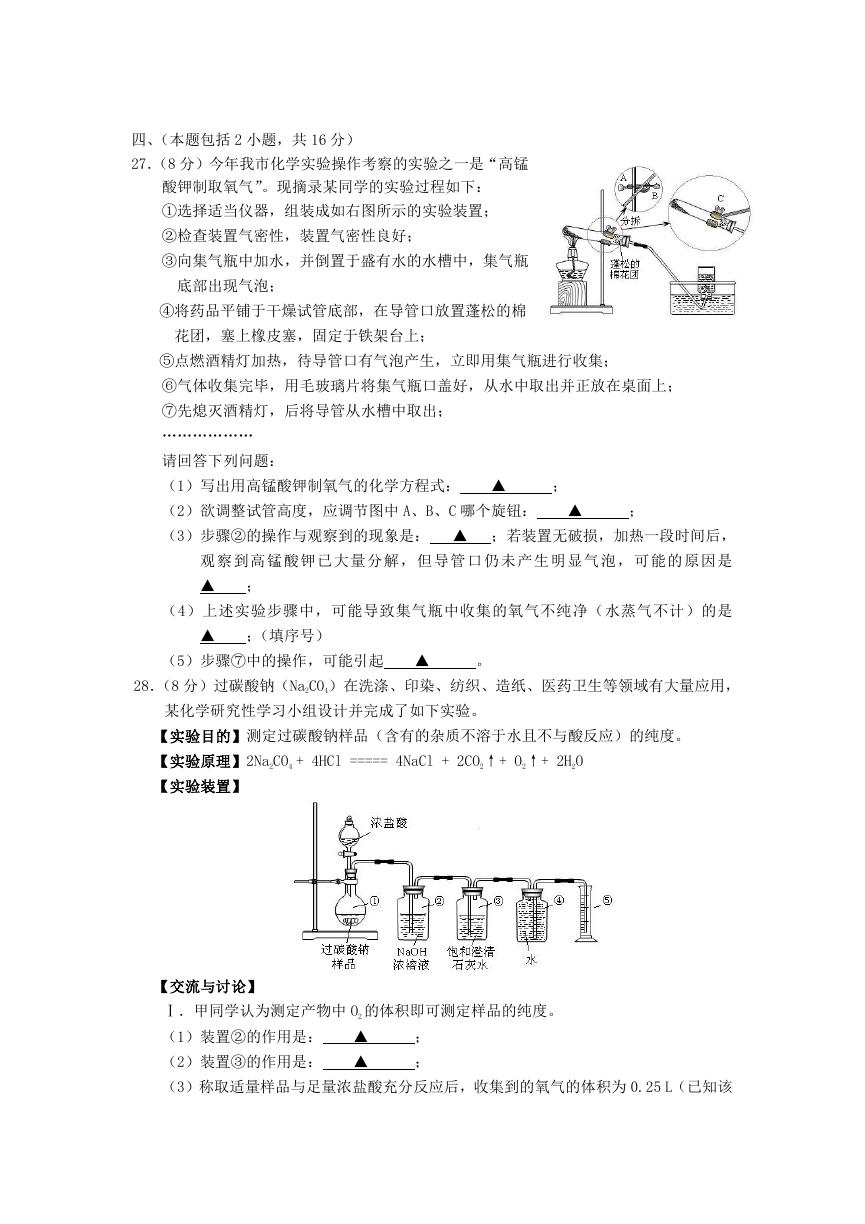
27.(8 分)今年我市化学实验操作考察的实验之一是“高锰
酸钾制取氧气”。现摘录某同学的实验过程如下:
①选择适当仪器,组装成如右图所示的实验装置;
②检查装置气密性,装置气密性良好;
③向集气瓶中加水,并倒置于盛有水的水槽中,集气瓶
底部出现气泡;
④将药品平铺于干燥试管底部,在导管口放置蓬松的棉
花团,塞上橡皮塞,固定于铁架台上;
⑤点燃酒精灯加热,待导管口有气泡产生,立即用集气瓶进行收集;
⑥气体收集完毕,用毛玻璃片将集气瓶口盖好,从水中取出并正放在桌面上;
⑦先熄灭酒精灯,后将导管从水槽中取出;
………………
请回答下列问题:
(1)写出用高锰酸钾制氧气的化学方程式:
▲
;
(2)欲调整试管高度,应调节图中 A、B、C 哪个旋钮:
▲
;
(3)步骤②的操作与观察到的现象是: ▲ ;若装置无破损,加热一段时间后,
观察 到高锰 酸钾 已大量 分解, 但导管 口仍 未产生 明显气 泡,可 能的 原因是
▲
;
(4)上述实验步骤中,可能导致集气瓶中收集的氧气不纯净(水蒸气不计)的是
▲
;(填序号)
(5)步骤⑦中的操作,可能引起
▲
。
28.(8 分)过碳酸钠(Na2CO4)在洗涤、印染、纺织、造纸、医药卫生等领域有大量应用,
某化学研究性学习小组设计并完成了如下实验。
【实验目的】测定过碳酸钠样品(含有的杂质不溶于水且不与酸反应)的纯度。
【实验原理】2Na2CO4 + 4HCl ===== 4NaCl + 2CO2↑+ O2↑+ 2H2O
【实验装置】
【交流与讨论】
Ⅰ.甲同学认为测定产物中 O2 的体积即可测定样品的纯度。
(1)装置②的作用是:
(2)装置③的作用是:
▲
▲
;
;
(3)称取适量样品与足量浓盐酸充分反应后,收集到的氧气的体积为 0.25 L(已知该
�
实验条件下氧气的密度为 1.28g/L),则称取的样品质量应大于
▲
g;
Ⅱ.乙同学认为测定产物中 CO2 的质量(即反应前后装置②的质量差)就可测定样品的
纯度。但利用上述实验装置测得 CO2 的质量并计算样品的纯度,结果会偏高,你认
为原因可能是
;(填序号)
▲
A.浓盐酸易挥发,产生的氯化氢气体被装置②吸收
B.二氧化碳气体逸出时带出的水蒸气在装置②中冷凝而被吸收
C.装置①、②内空气中的二氧化碳被装置②吸收
Ⅲ.丙同学提出了一种新方案,得到了大家的一致认可:称取样品 12.5g,滴加足量浓
盐酸至样品反应完全,再将烧瓶中所有的液体蒸发、结晶、烘干,称得氯化钠固
体 11.7 g。则该样品的纯度为
▲
。
五(本题包括 2 小题,共 12 分)
29.(6 分)某化学课外兴趣小组为探究 Na 与 CO2 的反
应进行了如下实验(实验部分装置如右图所示):
向盛有 Na 的装置 A 中通入纯净、干燥的 CO2,当
观察到装置 B 中刚好出现浑浊时,点燃酒精灯,
同时继续缓缓通入 CO2,Na 剧烈燃烧,产生白烟,
燃烧结束后装置 A 中有黑色固体和白色固体生成。
【资料卡】
(1)K、Ca、Na 等活泼金属的氧化物均可与水反应生成对应的碱;
(2)钠为银白色金属,过氧化钠为淡黄色固体。
【提出问题】白色固体含有什么物质?
【猜想与假设】
假设 1:白色固体含有
▲
假设 2:白色固体含有 Na2O;
;
【实验设计】
实验步骤
实验现象
实验结论
①取少量白色固体放入足量水中
白色固体完全溶解
②取①中少量溶液,加入
▲
产生大量气泡
③另取①中少量溶液,
▲
▲
假设 1 成立
假设 2 成立
【反思提高】
Na 在 CO2 中燃烧存在多个反应、生成多种物质。请你写出其中生成物仅为一种白色固
体与一种黑色固体的反应的化学方程式:
▲
。
30.(6 分)研究人员提出使用含汽油的混合燃料的方案,
以解决汽车尾气的问题。该方案的一种模拟过程如右图
所示,常温下,C、D 均为气体。
(1)写出 C 的化学式:
(2)写出下列反应的化学方程式:
▲
;
反应①:
反应②:
▲
▲
;
;
(3)在模拟转化关系图中,你认为可以循环重复使用
的物质是
▲
。(填字母)
�
六、(本题包括 2 小题,你只需选做其中一个小题,若两小题全做则以 31 题计分,共 6 分)
31.(6 分)第 17 届省运会在我市召开。
(1)为确保运动员身体健康,工作人员会向游泳池中加入
▲
(填化学式),
使得池水呈蓝色,该物质可以杀菌消毒的原理是
▲
;
(2)径赛发令枪所使用的“火药”通常是氯酸钾(KClO3)和红磷,发令时两种物质发
生反应产生大量白烟。该反应如下,请你进行配平:
▲
KClO3 + ▲ P ==== ▲ KCl + ▲ P2O5
(3)“兴奋剂” 已成为竞技体育的一大“毒瘤”。某兴奋剂的化学式为 C20H26O2,该兴
奋剂由
▲
种元素组成,碳元素的质量分数约为
▲
(4)城运会期间,倡导使用可降解的各种塑料制品,其目的是为了减少
;(保留 1 位小数)
▲ 污
染。
32.(6 分)元宵节是我国的重要传统节日,“接汉疑星落,依楼似月悬。”是唐代著名诗
人卢照邻对其盛况的写照,我国许多地方至今仍保留着燃灯放焰、共吃元宵的风俗。
(1)某红焰烟花的配方中包括硫、木炭粉、硝酸锶【Sr(NO3)2】等。
①硝酸锶中 Sr 的化合价为:
②写出硫燃烧的化学方程式:
▲
▲
;
;
(2)燃放孔明灯(如右图)祈福成为了元宵节的新风尚。小新同学想自制
孔明灯,为了使它能飞得更高、更远、更安全,选择作为灯罩的材料
应质轻且
;
(3)我市已禁止燃放孔明灯,因为孔明灯燃烧时外焰温度高达 300 多度,
而
;选择的燃料应燃烧热值大且
▲
▲
▲
一旦飘落到加油站、液化气站、油库等地,孔明灯会
引发火灾。(填序号)
A.提供可燃物
B.供给氧气 C.使温度达到可燃物的着火点
�
常州市二○一○年初中毕业、升学统一考试
化学试题参考答案及评分标准
一、选择题(本题包括 20 小题,共 40 分)
1.C
6.C
11.B
16.A
3.C
8.B
l3.D
l8.C
二、(本题包括 4 小题,共 20 分)
2.A
7.C
l2.D
l7.D
4.B
9.B
l4.D
l9.B
5.D
l0.A
l5.A
20.B
21.(5 分)(1)①2H ②3Al3+ (2)①B ②A ③C(各 1 分)
22.(4 分)(1)B (2)D
(4)F(各 1 分)
23.(5 分)(1)电 (2)导电 (3)催化剂(各 1 分)
(3)A
(4)Zn+H2SO4==ZnSO4+H2↑(2 分)
24.(4 分)(1)20
(2)20% 不饱和 (3)>(各 1 分)
三、(本题包括 2 小题,共 8 分)
25.(5 分)(1)Fe3O4(1 分) (2) 3CO+Fe2O3
高温 2Fe+3CO2(2 分)
(3)B(1 分)
(4)氧气(1 分)
26.(3 分)解:设反应生成的 Fe2(SO4)3 的质量为 x
Fe2O3+3H2SO4===Fe2(SO4)3+3H2O
160
16g
400
x
160
g16
400
x
x=40g
溶质的质量分数为:
40
g
g
184
g
16
%20%100
答:所得溶液的溶质质量分数为 20%。
四、(本大题包括 2 小题,共 16 分)
27.(8 分)
(1 分)
(1 分)
(1 分)
(1) 2KMnO4
(3)用手捂住大试管,导管口冒气泡,松手后导管口形成稳定的水柱(1 分)
△ K2MnO4+MnO2+O2↑(2 分) (2)A(1 分)
橡皮塞没有塞紧(1 分)
(4)③⑤ (答对一个给 1 分,有错倒扣 1 分)(2 分)
(5)倒吸(或大试管破裂)(1 分)
28.(8 分)
I.(1)除去 CO2 和 HCl 气体(1 分)
(2)验证 CO2 是否被除尽(1 分)
(3)2.44(2 分)
II.ABC(答对 2 个给 1 分,全答对给 2 分)(2 分)
III.97.6%(2 分)
五、(本大题包括 2 小题,共 12 分)
29.(6 分)
�
假设 1:Na2CO3(1 分)
【实验设计】②足量稀盐酸(1 分)
③加入足量氯化钙溶液,待沉淀完全后,加入 2~3 滴酚酞试液(1 分) 溶液呈红色
(1 分)
【反思提高】4Na+3CO2
△ 2Na2CO3+C(或 4Na+CO2
△ 2Na2O+C)
30.(6 分)
(1)CO2(1 分)
(2)①CaH2+2H2O====Ca(OH)2+2H2↑(2 分)
②Ca(OH)2+CO2====CaCO3↓+H2O(2 分)
(3)AC(1 分)
六、(本题包括 2 小题。你只需选做其中一个小题,若两小题全做则以 31 题计分,共 6 分)
31.(6 分)
(1)CuSO4 重金属离子可使细菌蛋白质失去生理功能
(2)5,6,5,3
(3)三 80.5%
(4)白色(每空 1 分)
32.(6 分)
(1)①+2(1 分)
(2)不易燃烧
(3)C(1 分)
②S+O2
点燃 SO2 (2 分)
燃烧时间长(各 1 分)
说明:1.凡合理答案均相应给分。
2.对化学用语的评分仍要严格。具体要求为:
(1)书写化学方程式时,化学式有错不得分;配平、条件、生成物状态有错、
计量数不是最简比、没画“=”(有机反应除外)等扣 l 分。
(2)化学专用名词写错别字,整体扣 l 分。
(3)元素符号书写不规范,整体扣 1 分。
3.解计算题格式必须规范。解题过程中,无设和答步骤、设未知量带单位、运算过
程中物理量的数值不带单位、解得未知量的单位带括号等共扣 1 分。
4.最小得分值为 1 分。
�















 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc