2016 上海高考化学真题及答案
考生注意:
1.本试卷满分 150 分,考试时间 120 分钟。
2.本考试设试卷和答题纸两部分,试卷包括试题与答题要求;所有答案必须涂或写在答题纸上,做在
试卷上一律不得分。
3.答题前,考生务必在答题纸上用钢笔或圆珠笔在答题纸正面清楚地填写姓名、准考证号,并将核对
后的条形码贴在指定位置上,在答题纸反面清楚地填写姓名。
4.答题纸与试卷在试题编号上一一对应的,答题时应特别注意,不能错位。
相对原子质量:H-1
C-12
N-14
O-16
Na-23
S-32Cl-35.5
Fe-56
一、选择题(本题共 10 分,每小题 2 分,每题只有一个正确选项)
1.轴烯是一类独特的星形环烃。三元轴烯(
)与苯
A.均为芳香烃 B.互为同素异形体
C.互为同系物
D.互为同分异构体
2.下列化工生产过程中,未涉及氧化还原反应的是
A.海带提碘 B.氯碱工业
C.氨碱法制碱 D.海水提溴
3.硼的最高价含氧酸的化学式不可能是
A.HBO2
B.H2BO3
C.H3BO3
D.H2B4O7
4.下列各组物质的熔点均与所含化学键的键能有关的是
A.CaO 与 CO2B.NaCl 与 HClC.SiC 与 SiO2
D.Cl2 与 I2
5.烷烃
的命名正确的是
A.4-甲基-3-丙基戊烷 B.3-异丙基己烷
C.2-甲基-3-丙基戊烷 D.2-甲基-3-乙基己烷
二、选择题(本题共 36 分,每小题 3 分,每题只有一个正确选项)
6.能证明乙酸是弱酸的实验事实是
�
A.CH3COOH 溶液与 Zn 反应放出 H2
B.0.1 mol/L CH3COONa 溶液的 pH 大于 7
C.CH3COOH 溶液与 NaCO3 反应生成 CO2
D.0.1 mol/L CH3COOH 溶液可使紫色石蕊变红
7.已知 W、X、Y、Z 为短周期元素,原子序数依次增大。W、Z 同主族,X、Y、Z 同周期,其中只有 X 为金属
元素。下列说法一定正确的是
A.原子半径:X>Y>Z>W
B.W 的含氧酸的酸性比 Z 的含氧酸的酸性强
C.W 的气态氢化物的稳定性小于 Y 的气态氢化物的稳定性
D.若 W 与 X 原子序数差为 5,则形成化合物的化学式为 X3W2
8.图 1 是铜锌原电池示意图。图 2 中,x 轴表示实验时流入正极的电子的物质的量,y 轴表示
A.铜棒的质量 B.c(Zn2+)
C.c(H+)D.c(SO4
2-)
9.向新制氯水中加入少量下列物质,能增强溶液漂白能力的是
A.碳酸钙粉末 B.稀硫酸 C.氯化钙溶液 D.二氧化硫水溶液
10.一定条件下,某容器中各微粒在反应前后变化的示意图如下,其中 和 代表不同元素的原子。
关于此反应说法错误的是
A.一定属于吸热反应 B.一定属于可逆反应
C.一定属于氧化还原反应 D.一定属于分解反应
11.合成导电高分子化合物 PPV 的反应为:
下列说法正确的是
A.PPV 是聚苯乙炔
�
B.该反应为缩聚反应
C.PPV 与聚苯乙烯的最小结构单元组成相同
D.1 mol
最多可与 2 mol H2 发生反应 学.科.网
12.下列各组混合物,使用氢氧化钠溶液和盐酸两种试剂不能分离的是
A.氧化镁中混有氧化铝
B.氯化铝溶液中混有氯化铁
C.氧化铁中混有二氧化硅 D.氯化亚铁溶液中混有氯化铜
13.O2F2 可以发生反应:H2S+4O2F2→SF6+2HF+4O2,下列说法正确的是
A.氧气是氧化产物
B.O2F2 既是氧化剂又是还原剂
C.若生成 4.48 L HF,则转移 0.8 mol 电子
D.还原剂与氧化剂的物质的量之比为 1:4
14.在硫酸工业生产中,为了有利于 SO2 的转化,且能充分利用热能,采用了中间有热交
换器的接触室(见右图)。下列说法错误的是
A.a、b 两处的混合气体成分含量相同,温度不同
B.c、d 两处的混合气体成分含量相同,温度不同
C.热交换器的作用是预热待反应的气体,冷却反应后的气体
D.c 处气体经热交换后再次催化氧化的目的是提高 SO2 的转化率
15.下列气体的制备和性质实验中,由现象得出的结论错误的是
选项
试剂
试纸或试液
现象
结论
A
B
C
D
浓氨水、生石
红色石蕊试
灰
纸
变蓝
浓盐酸、浓硫
酸
pH 试纸
变红
浓盐酸、二氧
淀粉碘化钾
化锰
试液
变蓝
亚硫酸钠、硫
酸
品红试液
褪色
NH3 为碱性
气体
HCl 为酸性
气体
Cl2 具有氧
化性
SO2 具有还
原性
�
16.实验室提纯含少量氯化钠杂质的硝酸钾的过程如右图所示。
下列分析正确的是
A.操作Ⅰ是过滤,将固体分离除去
B.操作Ⅱ是加热浓缩。趁热过滤,除去杂质氯化钠
C.操作Ⅲ是过滤、洗涤,将硝酸钾晶体从溶液中分离出来
D.操作Ⅰ~Ⅲ总共需两次过滤
17.某铁的氧化物(FexO)1.52 g 溶于足量盐酸中,向所得溶液中通入标准状况下 112 ml Cl2,恰好将 Fe2+
完全氧化。x 值为
A.0.80
B.0.85 C.0.90
D.0.93
三、选择题(本题共 20 分,每小题 4 分,每小题有一个或两个正确选项。只有一个正确选项的,多选不给
分;有两个正确选项的,选对一个给 2 分,选错一个,该小题不给分)
18.一定条件下,一种反应物过量,另一种反应物仍不能完全反应的是
A.过量的氢气与氮气 B.过量的浓盐酸与二氧化锰
C.过量的铜与浓硫酸 D.过量的锌与 18 mol/L 硫酸
19.已知:SO3
2-,且所有离子
2-+I2+H2O→SO4
2-+2I-+2H+。某溶液中可能含有 Na+、NH4
+、Fe2+、K+、I-、SO3
2-、SO4
物质的量浓度相等。向该无色溶液中滴加少量溴水,溶液仍呈无色。下列关于该溶液的判断正确的是
A.肯定不含 I-
B.肯定不含 SO4
2-
C.肯定含有 SO3
2-D.肯定含有 NH4
+
20.已知 NaOH+Al(OH)3→Na[Al(OH)4]。向集满 CO2 的铝制易拉罐中加入过量 NaOH 浓溶液,立即封闭罐口,易
拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。上述实验过程中没有发生的离子反应是
A. CO2+2OH−→CO3
2−+H2OB.Al2O3+2OH−+3 H2O→2 [Al(OH)4]−
C. 2 Al+2OH−+6H2O→2 [Al(OH)4]−+3 H2↑
D. Al3++4 OH−→[Al(OH)4]−
21.类比推理是化学中常用的思维方法。下列推理正确的是
A.CO2 是直线型分子,推测 CS2 也是直线型分子
B.SiH4 的沸点高于 CH4,推测 H2Se 的沸点高于 H2S
C.Fe 与 Cl2 反应生成 FeCl3,推测 Fe 与 I2 反应生成 FeI3
D.NaCl 与浓 H2SO4 加热可制 HCl,推测 NaBr 与浓 H2SO4 加热可制 HBr
22.称取(NH4)2SO4 和 NH4HSO4 混合物样品 7.24 g,加入含 0.1 molNaOH 的溶液,完全反应,生成 NH3 1792 ml
(标准状况),则(NH4)2SO4 和 NH4HSO4 的物质的量比为
�
A.1:1
B.1:2
c.1.87:1
D. 3.65:1
四、(本题共 12 分)
NaCN 超标的电镀废水可用两段氧化法处理:
(1)NaCN 与 NaClO 反应,生成 NaOCN 和 NaCl
(2)NaOCN 与 NaClO 反应,生成 Na2CO3、CO2、NaCl 和 N2
已知 HCN(Ki=6.3×10-10)有剧毒;HCN、HOCN 中 N 元素的化合价相同。
完成下列填空:
23.第一次氧化时,溶液的 pH 应调节为____________(选填“酸性”、“碱性”或“中性”);原因是
______________________。
24.写出第二次氧化时发生反应的离子方程式。
_______________________________________
25.处理 100 m3 含 NaCN 10.3 mg/L 的废水,实际至少需 NaClO___g(实际用量应为理论值的 4 倍),才能使
NaCN 含量低于 0.5 mg/L,达到排放标准。学科.网
26.(CN)2 与 Cl2 的化学性质相似。(CN)2 与 NaOH 溶液反应生成_________、__________和 H2O。
27.上述反应涉及到的元素中,氯原子核外电子能量最高的电子亚层是___________;H、C、N、O、Na 的原
子半径从小到大的顺序为_______。
28.HCN 是直线型分子,HCN 是___________分子(选填“极性”或“非极性”)。HClO 的电子式为___________。
五、(本题共 12 分)
随着科学技术的发展和环保要求的不断提高,CO2 的捕集利用技术成为研究的重点。
完成下列填空:
29.目前国际空间站处理 CO2 的一个重要方法是将 CO2 还原,所涉及的反应方程式为:
CO2(g)+4H2(g)
CH4(g)+2H2O(g)
已知 H2 的体积分数随温度的升高而增加。
若温度从 300℃升至 400℃,重新达到平衡,判断下列表格中各物理量的变化。(选填“增大”、“减小”
或“不变”)
v正
v逆
平衡常数 K
转化率α
30.相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
[CO2]/mol·L-1
[H2]/mol·L-1
[CH4]/mol·L-1
[H2O]/mol·L-1
�
a
m
平
衡Ⅰ
平
衡Ⅱ
b
n
c
x
d
y
a、b、c、d与 m、n、x、y之间的关系式为_________。
31.碳酸:H2CO3,Ki1=4.3×10-7,Ki2=5.6×10-11
草酸:H2C2O4,Ki1=5.9×10-2,Ki2=6.4×10-5
0.1 mol/L Na2CO3 溶液的 pH____________0.1 mol/L Na2C2O4 溶液的 pH。(选填“大于”“小于”或“等
于”)
等浓度广东草酸溶液和碳酸溶液中,氢离子浓度较大的是___________。
若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是_____。(选填
编号)
a.[H+]>[HC2O4
-]>[HCO3
-]>[CO3
2-]
c. [H+]>[HC2O4
-]>[C2O4
2-]>[CO3
2-]
b. [HCO3
-]>[HC2O4
-]>[C2O4
2-]>[CO3
2-]
d. [H2CO3] >[HCO3
-]>[HC2O4
-]>[CO3
2-]
32.人体血液中的碳酸和碳酸氢盐存在平衡:H++ HCO3
-
H2CO3,当有少量酸性或碱性物质进入血液中时,
血液的 pH 变化不大,用平衡移动原理解释上述现象。学.科网
________________________________
六、(本题共 12 分)
乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验常用 a 装置来制备。
完成下列填空:
33.实验时,通常加入过量的乙醇,原因是______________。加入数滴浓硫酸即能起催化作用,但实际用量
多于此量,原因是_______________;浓硫酸用量又不能过多,原因是____________。
34.饱和 Na2CO3 溶液的作用是_______________。
�
35.反应结束后,将试管中收集到的产品倒入分液漏斗中,_________、________,然后分液。
36.若用 b 装置制备乙酸乙酯,其缺点有__________、__________。由 b 装置制得的乙酸乙酯产品经饱和碳
酸钠溶液和饱和食盐水洗涤后,还可能含有的有机杂质是________,分离乙酸乙酯与该杂质的方法是
_______________。
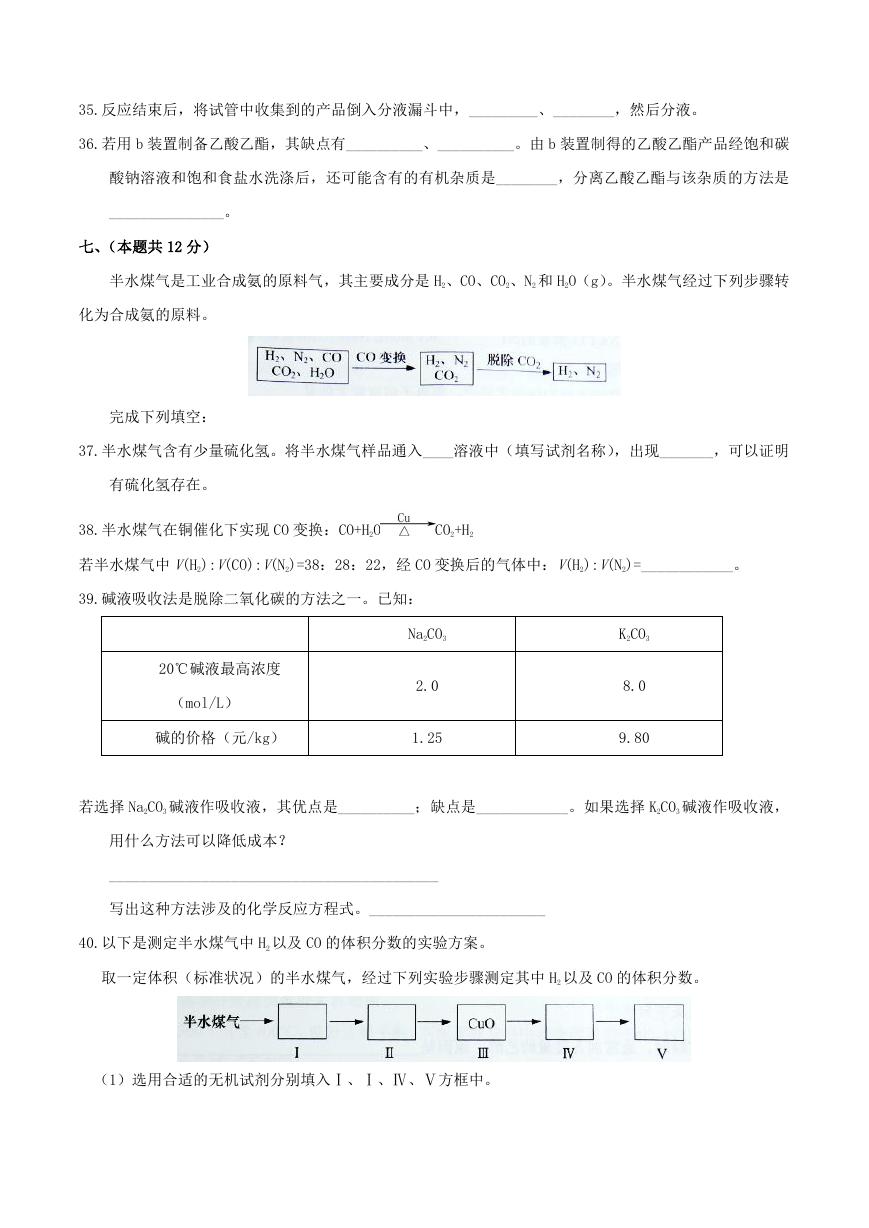
七、(本题共 12 分)
半水煤气是工业合成氨的原料气,其主要成分是 H2、CO、CO2、N2 和 H2O(g)。半水煤气经过下列步骤转
化为合成氨的原料。
完成下列填空:
37.半水煤气含有少量硫化氢。将半水煤气样品通入____溶液中(填写试剂名称),出现_______,可以证明
有硫化氢存在。
38.半水煤气在铜催化下实现 CO 变换:CO+H2O
CO2+H2
若半水煤气中 V(H2):V(CO):V(N2)=38:28:22,经 CO 变换后的气体中:V(H2):V(N2)=____________。
39.碱液吸收法是脱除二氧化碳的方法之一。已知:
20℃碱液最高浓度
(mol/L)
碱的价格(元/kg)
Na2CO3
2.0
1.25
K2CO3
8.0
9.80
若选择 Na2CO3 碱液作吸收液,其优点是__________;缺点是____________。如果选择 K2CO3 碱液作吸收液,
用什么方法可以降低成本?
___________________________________________
写出这种方法涉及的化学反应方程式。_______________________
40.以下是测定半水煤气中 H2 以及 CO 的体积分数的实验方案。
取一定体积(标准状况)的半水煤气,经过下列实验步骤测定其中 H2 以及 CO 的体积分数。
(1)选用合适的无机试剂分别填入Ⅰ、Ⅰ、Ⅳ、Ⅴ方框中。
�
(2)该实验方案中,步骤________(选填“Ⅳ”或“Ⅴ”)可以确定半水煤气中 H2 的体积分数。学科&
网
八、(本题共 9 分)
异戊二烯是重要的有机化工原料,其结构简式为 CH2=C(CH3)CH=CH2。
完成下列填空:
41.化合物 X 与异戊二烯具有相同的分子式,与 Br/CCl4 反应后得到 3-甲基-1,1,2,2-四溴丁烷。X 的结构简
式为_______________。
42.异戊二烯的一种制备方法如下图所示:
A 能发生的反应有___________。(填反应类型)
B 的结构简式为______________。
43.设计一条由异戊二烯制得有机合成中间体
的合成路线。
(合成路线常用的表示方式为:
)
九、(本题共 13 分)
M 是聚合物胶黏剂、涂料等的单体,其一条合成路线如下(部分试剂及反应条件省略):
完成下列填空:
44.反应①的反应类型是____________。反应④的反应条件是_____________。
45.除催化氧化法外,由 A 得到
所需试剂为___________。
46.已知 B 能发生银镜反应。由反应②、反应③说明:在该条件下,_______________。
47.写出结构简式,C________________
D________________
�















 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc