2011 年江苏高考化学真题及答案
满分 120 分,考试时间 100 分钟
可能用到的相对的原子质量:H 1
C 12
N 14
O 16
Na 23
Mg 24
Al 27
S 32
Cl 35.5 Ca 40
Mn 55
Fe 56
Cu 64
Br 80
Ag 108
第Ⅰ卷(选择题 共 40 分)
一、单项选择题(本题包括 10 小题,每小题 2 分,共计 20 分。每小题只有一个....选项符合题
意)
1.化学与人类生活、社会可持续发展密切相关,下列措施有利于节能减排、保护环境的是
①加快化石燃料的开采与使用;②研发易降解的生物农药;③应用高效洁净的能源转换
技术;④田间焚烧秸秆;⑤推广使用节能环保材料。
A.①③⑤
B.②③⑤
C.①②④
D.②④⑤
2.下列有关化学用语表示正确的是
A.N2 的电子式:N ‥‥‥ N
B.S2-的结构示意图: +16 2 8 6
C.质子数为 53,中子数为 78 的碘原子: 131
COOH
53I
D.邻羟基苯甲酸的结构简式:
OH
3.下列有关物质的性质和该性质的应用均正确的是
A.常温下浓硫酸能使铝发生钝化,可在常温下作用铝制贮藏贮运浓硫酸
B.二氧化硅不与任何酸反应,可用石英制造耐酸容器
C.二氧化氯具有还原性,可用于自来水的杀菌消毒
D.铜的金属活泼性比铁的弱,可在海轮外壳上装若干铜块以减缓其腐蚀
4.常温下,下列各组离子在指定溶液中一定能大量共存的是
A.1.0
mol·L-1 的 KNO3 溶液:H+、Fe2+、Cl-、SO 2-
4
B.甲基橙呈红色的溶液:NH+
4、Ba2+、AlO-
C.pH=12 的溶液:K+、Na+、CH3COO-、Br-
D.与铝反应产生大量氢气的溶液:Na+、K+、CO 2-
2 、Cl-
3 、NO-
3
5.短周期元素 X、Y、Z、W、Q 在元素周期表中的相对位置如图 1 所示。下列说法正确的是
A.元素 X 与元素 Z 的最高正化合价之和的数值等于 8
B.原子半径的大小顺序为:rX>rY>rZ>rW>rQ
C.离子 Y2-和 Z 3+的核外电子数和电子层数都不相同
D.元素 W 的最高价氧化物对应的水化物的酸性比 Q 的强
Z
6.下列表示对应化学反应的离子方程式正确的是
A.FeCl3 溶液与 Cu 的反应:Cu+Fe3+===Cu2++Fe2+
B.NO2 与水的反应:3NO2+H2O===2NO-
C.醋酸溶液与水垢中的 CaCO3 反应:CaCO3+2H+===Ca2++H2O+CO2↑
3 +NO+2H+
X
Y
W
图 1
Q
�
D.向 NaAlO2 溶液中通入过量 CO2:2AlO-
2 +CO2+3H2O===2A(OH)3↓+CO 2-
3
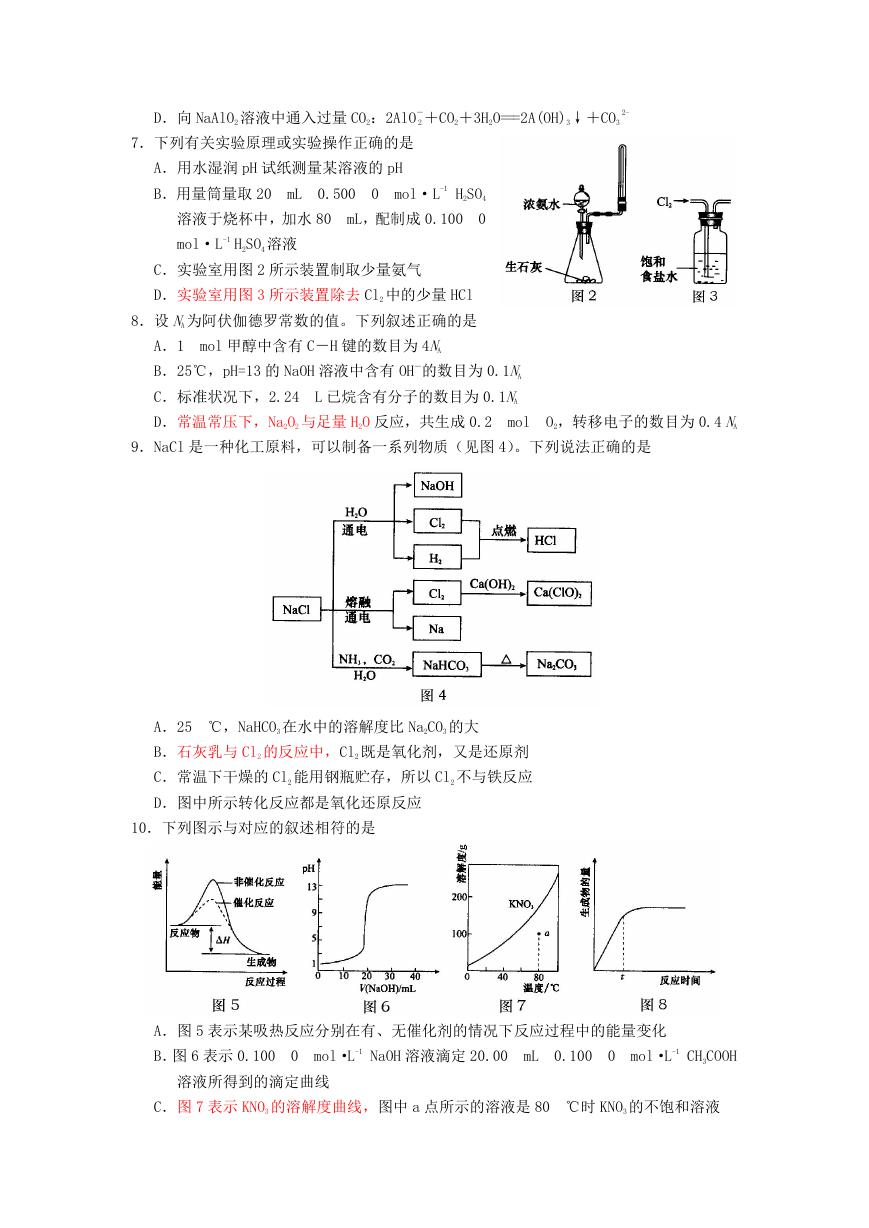
7.下列有关实验原理或实验操作正确的是
A.用水湿润 pH 试纸测量某溶液的 pH
B.用量筒量取 20
mL
0.500
0
mol·L-1 H2SO4
溶液于烧杯中,加水 80
mL,配制成 0.100
0
mol·L-1 H2SO4 溶液
C.实验室用图 2 所示装置制取少量氨气
D.实验室用图 3 所示装置除去 Cl2 中的少量 HCl
8.设 NA 为阿伏伽德罗常数的值。下列叙述正确的是
A.1
mol 甲醇中含有 C-H 键的数目为 4NA
B.25℃,pH=13 的 NaOH 溶液中含有 OH-的数目为 0.1NA
C.标准状况下,2.24
L 已烷含有分子的数目为 0.1NA
D.常温常压下,Na2O2 与足量 H2O 反应,共生成 0.2 mol
O2,转移电子的数目为 0.4 NA
9.NaCl 是一种化工原料,可以制备一系列物质(见图 4)。下列说法正确的是
A.25 ℃,NaHCO3 在水中的溶解度比 Na2CO3 的大
B.石灰乳与 Cl2 的反应中,Cl2 既是氧化剂,又是还原剂
C.常温下干燥的 Cl2 能用钢瓶贮存,所以 Cl2 不与铁反应
D.图中所示转化反应都是氧化还原反应
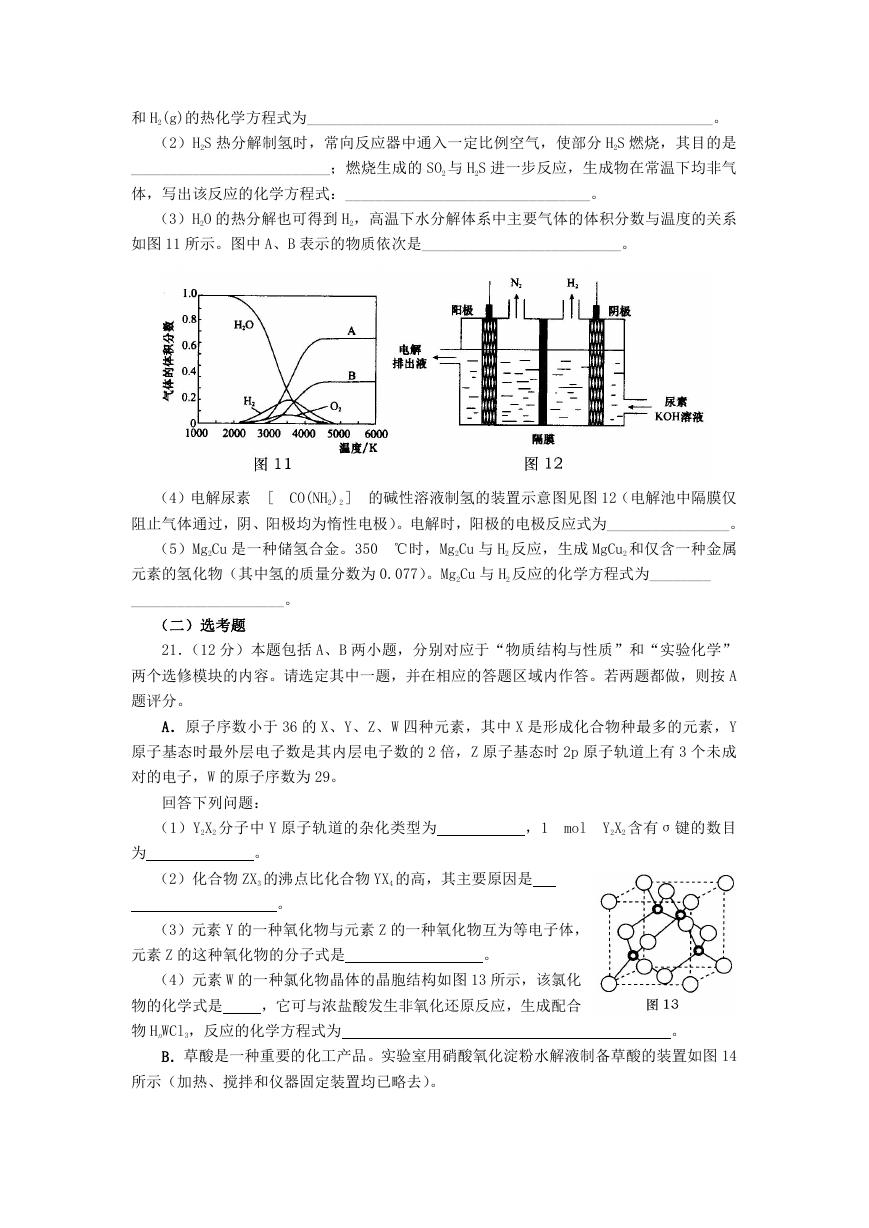
10.下列图示与对应的叙述相符的是
A.图 5 表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化
B.图 6 表示 0.100
0
mol·L-1 NaOH 溶液滴定 20.00
mL
0.100
0
mol·L-1 CH3COOH
溶液所得到的滴定曲线
C.图 7 表示 KNO3 的溶解度曲线,图中 a 点所示的溶液是 80 ℃时 KNO3 的不饱和溶液
�
D.图 8 表示某可逆反应生成物的量随反应时间变化的曲线,由图知 t时反应物转化率最
大
二、不定项选择题(本题包括 5 小题,每小题 4 分,共计 20 分。每小题只有一个或两个
.....选
项符合题意。若正确答案只包括一个选项,多选时,该题得 0 分;若正确答案包括两个
选项时,只选一个且正确的得 2 分,选两个且都正确的得满分,但只要选错一个,该小
题就得 0 分)
11.β-紫罗兰酮是存在于玫瑰花、番茄等中的一种天然香料,它经多步反应可合成维生素
A1。
下列说法正确的是
A.β-紫罗兰酮可使酸性 KMnO4 溶液褪色
B.1
mol 中间体 X 最多能与 2
mol H2 发生加成反应
C.维生素 A1 易溶于 NaOH 溶液
D.β-紫罗兰酮与中间体 X 互为同分异构体
12.下列说法正确的是
A.一定温度下,反应 MgCl2(1)===Mg(1)+Cl2(g)的∆H>0,∆S>0
B.水解反应 NH+
4+H2O
NH3·H2O+H+ 达到平衡后,升高温度平衡逆向移动
C.铅蓄电池放电时的负极和充电时的阳极均发生还原反应
D.对于反应 2H2O2===2H2O+O2↑,加入 MnO2 或升高温度都能加快 O2 的生成速率
13.下列有关实验原理、方法和结论都正确的是
A.向饱和 FeCl3 溶液中滴加过量氨水,可制取 Fe(OH)3 胶体
B.取少量溶液 X,向其中加入适量新制氨水,再加几滴 KSCN 溶液,溶液变红,说明 X
溶液中一定含有 Fe2+
C.室温下向苯和少量苯酚的混合溶液中加入适量 NaOH 溶液,振荡、静置后分液,可除
去苯中少量苯酚
D.已知 I-
3
I2+I-,向盛有 KI3 溶液的试管中加入适量 CCl4,振荡静置后 CCl4 层显
紫色,说明 KI3 在 CCl4 中的溶解度比在水中的大
14.下列有关电解质溶液中微粒的物质的量浓度关系正确的是
A.在 0.1
mol·L-1 NaHCO3 溶液中:c(Na+)>c(HCO-
3 )>c(CO 2-
3 )>c(H2CO3)
B.在 0.1mol·L-1 Na2CO3 溶液中:c(OH-)-c(H+)=c(HCO-
C.向 0.2 mol·L-1 NaHCO3 溶液中加入等体积 0.1
3 )+2c(H2CO3)
mol·L-1 NaOH 溶液:
c(CO 2-
3 )>c(HCO-
3 )>c(OH-)>c(H+)
D.常温下,CH3COONa 和 CH3COOH 混合溶液 [ pH=7,c(Na+)=0.1
mol·L-1 ]:
c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-)
15.700 ℃时,向容积为 2
L 的密闭容器中充入一定量的 CO 和 H2O,发生反应:
CO(g)+H2O(g)
CO2(g)+H2(g)
�
反应过程中测定的部分数据见下表(表中 t2>t1):
反应时间/min
n(CO)/mol
n(H2O)/mol
0
t1
t2
1.20
0.80
0.60
0.20
下列说法正确的是
A.反应在 t1 min 内的平均速率为 v(H2)=
0.40
t1
mol·L-1·min-1
B.保持其他条件不变,起始时向容器中充入 0.60 mol CO 和 1.20 mol H2O,到达平衡时
n(CO2)=0.40 mol
C.保持其他条件不变,向平衡体系中再通入 0.20 mol H2O,与原平衡相比,达到新平衡
时 CO 转化率增大,H2O 的体积分数增大
D.温度升至 800 ℃,上述反应平衡常数为 0.64,则正反应为吸热反应
第Ⅱ卷(非选择题 共 80 分)
三、非选择题(本大题包括必考题和选考题两部分。第 16 题~第 20 题为必考题,每个试
题考生必须作答。第 21 题为选考题,考生按要求作答)
(一)必考题(本大题包括 5 小题,共 68 分)
16.(12 分)以硫铁矿(主要成分为 FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工
艺流程如下:
回答下列问题:
(1)在一定条件下,SO2 转化为 SO3 的反应为 2SO2(g)+O2(g)
2SO3(g),该反应的平
衡常数表达式为 K=
;过量的 SO2 与 NaOH 溶液反应的化学方程式
为
。
(2)酸溶及后续过程中均需保持盐酸过量,其目的是
(3)通氯气氧化后时,发生的主要反应的离子方程式为
。
、
;
该过程产生的尾气可用碱溶液吸收,尾气中污染空气的气体为
(写化学式)。
17.(15 分)敌草胺是一种除草剂。它的合成路线如下:
回答下列问题:
(1)在空气中久置,A 由无色转变为棕色,其原因是
。
�
(2)C 分子中有 2 个含氧官能团,分别为
和
填官能团名称)。
(3)写出同时满足下列条件的 C 的一种同分异构体的结构简式:
。
①能与金属钠反应放出 H2;②是萘(
)的衍生物,且取代基都在同一个苯环
上;③可发生水解反应,其中一种水解产物能发生银镜反应,另一种水解产物分子中有 5
种不同化学环境的氢。
(4)若 C 不经提纯,产物敌草胺中将混有少量副产物 E(分子式为 C23H18O3),E 是一种酯。
E 的结构简式为
。
(5)已知:RCH2COOH
Cl
∣
PCl3——→
R
CH COOH,写出以苯酚和乙醇为原料制备
△
OCH2COOCH2CH3
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
H2C=CH2
——→CH3CH2Br
HBr
NaOH 溶液
————→△ CH3CH2OH
18.(12 分)Ag2O2 是银锌碱性电池的正极活性物质,可通过下列方法制备:在 KOH 加入
适量 AgNO3 溶液,生成 Ag2O 沉淀,保持反应温度为 80 ℃,边搅拌边将一定量 K2S2O8 溶液
缓慢加到上述混合物中,反应完全后,过滤、洗涤、真空干燥得到固体样品。反应方程式为
2AgNO3+4KOH+K2S2O8
△
===Ag2O2↓+2KNO3+2K2SO4+2H2O
回答下列问题:
(1)上述制备过程中,检验洗涤是否完全的方法是
。
(2)银锌碱性电池的电解质溶液为 KOH 溶液,电池放电时正极的 Ag2O2 转化为 Ag,负极
的 Zn 转化为 K2Zn(OH)4,写出该电池反应方程式:
。
(3)准确称取上述制备的样品(设仅含 Ag2O2 和 Ag2O)2.558
g,在一定的条件下完全
分解为 Ag 和 O2,得到 224.0
mL O2(标准状况下)。计算样品中 Ag2O2 的质量分数(计算结
果精确到小数点后两位)。
�
19.(15 分)高氯酸铵(NH4ClO4)是复合火箭推进剂的重要成分,实验室可通过下列反
应制取:NaClO4(aq)+NH4Cl(aq)
90 ℃
===== NH4ClO4(aq)+NaCl(aq)
(1)若 NH4Cl 用氨气和浓盐酸代替,上述反应不需要外界供热就能进行,其原因是
。
(2)反应得到的混合溶液中 NH4ClO4 和 NaCl 的质量分数分别为 0.30 和 0.l5(相关
物质的溶解度曲线见图 9)。从混合溶液中获得较多 NH4ClO4 晶体的实验操作依次为(填操作
名称)
、干燥。
(3)样品中 NH4ClO4 的含量可用蒸馏法进行测定,蒸馏装置如上图乙所示(加热和仪器
固定装置已略去),实验步骤如下:
步骤 1:按图 10 所示组装仪器,检查装置气密性。
步骤 2:准确称取样品 a g(约 0.5
g)于蒸馏烧瓶中,加入约 150
mL 水溶解。
步骤 3:准确量取 40.00
mL 约 0.1 mol·L-¹ H2SO4 溶解于锥形瓶中。
步骤 4:经滴液漏斗向蒸馏瓶中加入 20
mL 3 mol·L-¹ NaOH 溶液。
步骤 5:加热蒸馏至蒸馏烧瓶中剩余约 100
mL 溶液。
步骤 6:用新煮沸过的水冲洗冷凝装置 2~3 次,洗涤液并入锥形瓶中。
步骤 7:向锥形瓶中加入酸碱指示剂,用 c mol·L-¹ NaOH 标准溶液滴定至终点,消耗
NaOH 标准溶液 V1 mL。
步骤 8:将实验步骤 1-7 重复 2 次。
①步骤 3 中,准确量取 40.00
mL H2SO4 溶液的玻璃仪器是________________。
②步骤 1~7 中确保生成的氨被稀硫酸完全吸收的实验是____________(填写步骤号)。
③为获得样品中 NH4ClO4 的含量,还需补充的实验是 _________________________。
20.(14 分)氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
已知:CH4(g)+H2O(g)===CO(g)+3H2(g) ∆H=206.2
kJ·mol-1
CH4(g)+CO2(g)===2CO(g)+2H2(g) ∆H=247.4
kJ·mol-1
H2S(g)===2H2(g)+S2(g)
∆H=69.8
kJ·mol-1
(1)以甲烷为原料制取氢气是工业上常用的制氢方法。CH4(g)与 H2O(g)反应生成 CO2(g)
�
和 H2(g)的热化学方程式为_____________________________________________________。
(2)H2S 热分解制氢时,常向反应器中通入一定比例空气,使部分 H2S 燃烧,其目的是
__________________________;燃烧生成的 SO2 与 H2S 进一步反应,生成物在常温下均非气
体,写出该反应的化学方程式:________________________________。
(3)H2O 的热分解也可得到 H2,高温下水分解体系中主要气体的体积分数与温度的关系
如图 11 所示。图中 A、B 表示的物质依次是__________________________。
(4)电解尿素 [
CO(NH2)2 ] 的碱性溶液制氢的装置示意图见图 12(电解池中隔膜仅
阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为________________。
(5)Mg2Cu 是一种储氢合金。350 ℃时,Mg2Cu 与 H2 反应,生成 MgCu2 和仅含一种金属
元素的氢化物(其中氢的质量分数为 0.077)。Mg2Cu 与 H2 反应的化学方程式为________
____________________。
(二)选考题
21.(12 分)本题包括 A、B 两小题,分别对应于“物质结构与性质”和“实验化学”
两个选修模块的内容。请选定其中一题,并在相应的答题区域内作答。若两题都做,则按 A
题评分。
A.原子序数小于 36 的 X、Y、Z、W 四种元素,其中 X 是形成化合物种最多的元素,Y
原子基态时最外层电子数是其内层电子数的 2 倍,Z 原子基态时 2p 原子轨道上有 3 个未成
对的电子,W 的原子序数为 29。
回答下列问题:
(1)Y2X2 分子中 Y 原子轨道的杂化类型为
,1
mol
Y2X2 含有σ键的数目
为
。
(2)化合物 ZX3 的沸点比化合物 YX4 的高,其主要原因是
。
(3)元素 Y 的一种氧化物与元素 Z 的一种氧化物互为等电子体,
元素 Z 的这种氧化物的分子式是
。
(4)元素 W 的一种氯化物晶体的晶胞结构如图 13 所示,该氯化
物的化学式是
,它可与浓盐酸发生非氧化还原反应,生成配合
物 HnWCl3,反应的化学方程式为
。
B.草酸是一种重要的化工产品。实验室用硝酸氧化淀粉水解液制备草酸的装置如图 14
所示(加热、搅拌和仪器固定装置均已略去)。
�
实验过程如下:
①将一定量的淀粉水解液加入三颈瓶中
②控制反应液温度在 55~60 ℃条件下,边搅
拌边缓慢滴加一定量含有适量催化剂的混酸
(65
%
HNO3 与 98
%
H2SO4 的质量比为 2∶1.5)溶液
③反应 3
h 左右,冷却,抽滤后再重结晶得
草酸晶体。
硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3 —→3H2C2O4+9NO2↑ +3NO↑ +9H2O
C6H12O6+8HNO3 —→6CO2↑+8NO↑ +10H2O
3H2C2O4+2HNO3 —→6CO2↑+2NO↑ +4H2O
(1)检验淀粉是否水解完全所需用的试剂为
。
(2)实验中若混酸滴加过快,将导致草酸产率下降,其原因是
。
(3)装置 C 用于尾气吸收,当尾气中 n(NO2):n(NO)=1:1 时,过量的 NaOH 溶液能将 NOx
全部吸收,原因是
(用化学方程式表示)。
(4)与用 NaOH 溶液吸收尾气相比较,若用淀粉水解液吸收尾气,其优、缺点是
(5)草酸重结晶的减压过滤操作中,除烧杯、玻璃棒外,还必须使用属于硅酸盐材料的
仪器有
。
。
�














 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc