2010 年海南普通高中会考化学考试真题
解题时可能用到的相对原子质量:H-1
O-16
S-32
Fe-56
1.对于易燃易爆有毒的化学物质,往往会在其包装上贴危险警告标签。下图所列物质,贴
错了包装标签的是:
白磷
A
高锰酸钾
过氧化钠
浓硫酸
B
C
D
2.20 世纪我国科学家在化学方面的突出贡献是
A、“嫦娥一号”成功发射
B、合成具有生命活性的结晶牛胰岛素
C、发明火药
D、提出元素周期律
3.下列各物质所属类别不正确的是
A.三聚氰胺[C3N3(NH2)3]属于有机物
B.Na2CO3 属于无机盐
C.神七升空所用燃料属于(C2H8N2)酸类
D.祥云火炬外壳(由镁铝组成)属于合金
4.2008 年 10 月,海南省保亭县罗葵洞发现大型钼矿,储量达 25.4 万吨。右图为元
素周期表中钼元素相关资料。下列说法不正确的是
A. 钼元素的元素符号为 Mo
B. 钼元素的原子序数为 42
C. 钼元素的相对原子质量为 95.94
D. 钼元素原子核内有 53 个中子
42 Mo
钼
4d55s1
95.94
�
5.配制 250mL2 .00mol/L 的 NaCl 溶液,需要用到下列哪些仪器:①试管、②烧杯、③量
筒、④锥形瓶、⑤容量瓶、⑥玻璃棒。
A、③④⑤⑥ B、②③④ C、②③⑤⑥ D、①②③④⑤⑥
6.下列对有关实验事实的解释正确的是
A.浓硝酸在光照条件下变黄,说明浓硝酸易分解生成有色产物且溶于浓硝酸
B.酸性高锰酸钾溶液中通入乙烯后,颜色褪去,说明乙烯具有漂白性
C.常温下,将铝片放入浓硫酸中无明显现象,说明铝不和冷的浓硫酸反应
D.向氯化铁溶液中滴入硫氰化钾溶液,显血红色,说明 Fe3+具有氧化性
7.对于某些离子的检验及结论一定正确的是
A.加入稀盐酸产生无色气体,一定有 CO 2
3
B.加入氯化钡溶液产生白色沉淀,一定有 SO 2
4
C.加入硫氰化钾溶液,显血红色,一定有 Fe3+
D.加入氢氧化钠溶液并加热,产生的气体,一定有 NH
4
8.右图所示实验非常有趣,想必给同学们留下了深刻印象。
它体现了氨的性质包括。
①氧化性 ②与水反应生成碱性物质 ③还原性
④极易溶解于水
A.②④ B. ②③ C.①③④ D. ①④
9.下列做法相关的化学原理不正确的是
选项
具体做法
相关原理
A
将食物储存在冰箱里
温度降低,反应速率减小
�
B
C
D
医院透视用硫酸钡作“钡餐”
硫酸钡既不溶于水也不溶于酸
实验室制备氢气用粗锌代替纯锌
形成微型原电池,加快反应速率
医疗上血液透析
利用了胶体的丁达尔效应
10.下列叙述不正确的是
A、氯化钠的摩尔质量是 36.5 g/ mol
B、5 molCO2 中所含的 CO2 分子数为 3.01×1024
C、将 0.1molNaOH 加入 1L 水中溶解,即配制得到 0.1mol/L 的 NaOH 溶液
D、49g H2SO4 的物质的量是 0.5 mol
11.下列物质中,既含有离子键,又含有共价键的是
A.H2O
B.NaOH
C.CaCl2
D.Cl2
12.对于可逆反应:N2 (g)+ 3H2(g)
2NH3(g)。下列判断不正确...的是
A.20s 内,H2 的浓度改变了 0.60mol/L,则平均反应速率υ(H2) = 0.030mol/(L·s)
B.当气体总压不随时间改变时,表明该反应达到平衡状态
C.使用催化剂可明显减少达到平衡的时间
D.达到化学平衡状态时,正、逆反应的速率都为 0
13.下列关于右图所示装置的叙述,正确的是(水果电池示意图)
A.铜是负极
B.电能转变为化学能
C.电子从铜片经导线流向锌片
D.水果汁起到导电作用
14.能正确表示下列反应的离子方程式的是
A.氢氧化钡溶液与硫酸反应:H+ + OH- = H2O
B.铁溶于氯化铁溶液:Fe3+ + Fe= 2Fe2+
C.氢氧化钠溶液与硫酸铜溶液反应:2OH-+ Cu2+ = Cu(OH)2↓
�
D.碳酸钙与盐酸反应:CO3
2- + 2H+ = CO2 ↑ + H2O
15.下列关于有机物的说法不正确的是
A.食醋的主要成分是乙酸,普通食醋中含有 3%—5%的乙酸
B.固体酒精是固体状态的纯酒精
C.苯是一种有机溶剂,常用于油漆等
D.医学上常用班氏试剂检验患者尿液中的葡萄糖含量
16.除去甲烷中混有的少量乙烯的正确方法是
A.将混合气体用导气管导出,在空气中点燃
B.将混合气体通过盛足量溴水的洗气瓶
C.将混合气体通过盛足量澄清石灰水的洗气瓶
D.将混合气体通过盛足量蒸馏水的洗气瓶
第Ⅱ卷 非选择题
17.(10 分)硫酸的工业制法的反应原理如下:
① 2FeS2 + 11O2 = 2Fe2O3 + 8SO2 ② 2SO2+O2
2SO3
③ SO3 + H2O = H2SO4
回答下列问题:(1)上述反应中,属于可逆反应的是
;(填序号)
(2)某化工厂用含杂质 28%的黄铁矿生产硫酸,假设生产过程中硫的损失不计,则 1t 黄铁
矿可制得 98%的浓硫酸
t。
(3)SO2 中硫元素处于中间价态,请写出符合下列要求的化学方程式。
① SO2 作氧化剂
;② SO2 作还原剂
;
③ SO2 既不作氧化剂,又不作还原剂
。
�
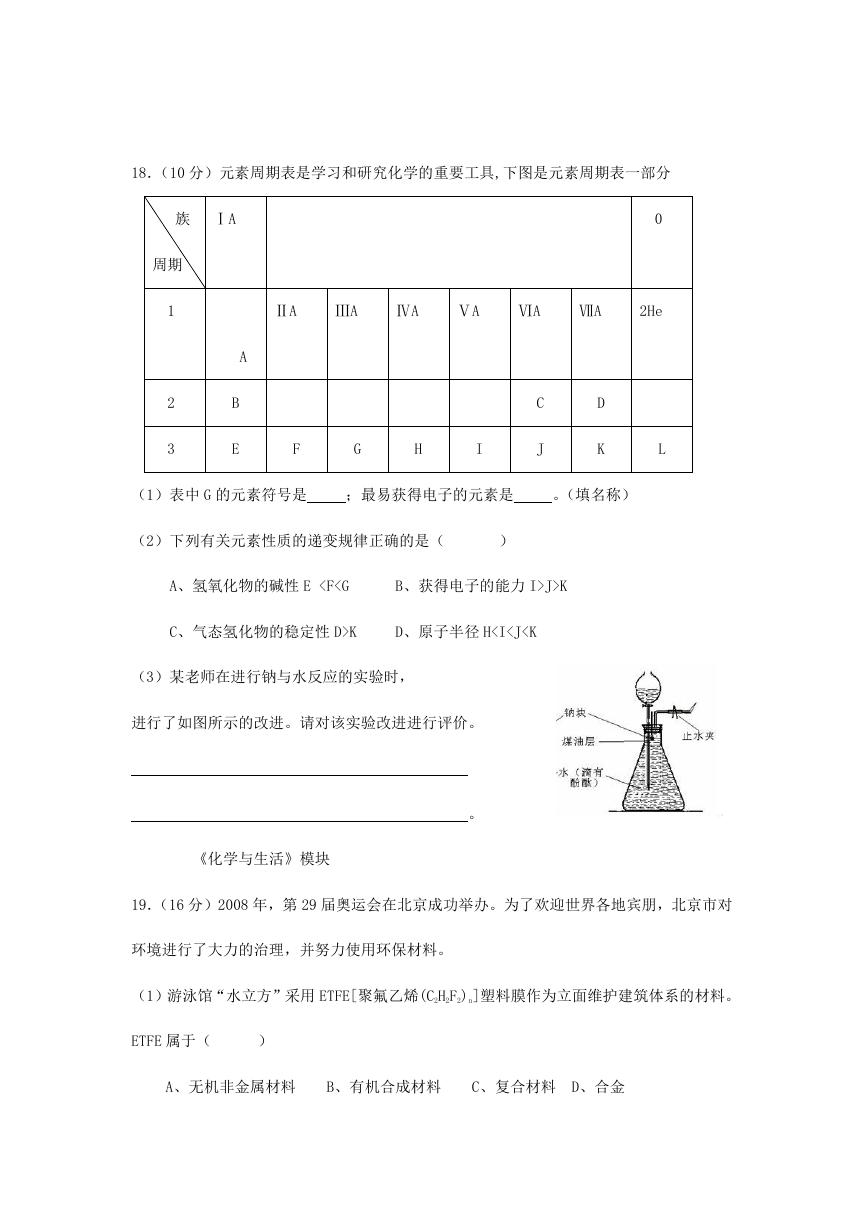
18.(10 分)元素周期表是学习和研究化学的重要工具,下图是元素周期表一部分
族
ⅠA
周期
1
2
3
A
B
E
0
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
2He
F
G
H
I
C
J
D
K
L
(1)表中 G 的元素符号是
;最易获得电子的元素是
。(填名称)
(2)下列有关元素性质的递变规律正确的是(
)
A、氢氧化物的碱性 E
J>K
C、气态氢化物的稳定性 D>K
D、原子半径 H(2)北京市环境监测部门密切关注空气质量。下列不属于监测内容的是(
)
A、一氧化碳
B、二氧化硫
C、二氧化碳
D、可吸入颗粒
(3)请提出治理空气污染的具体措施(至少 3 条)
20.(16 分)某果粒橙饮料的配料如下:水、白砂糖、橙肉、浓缩澄汁、食用香料、柠檬酸、
柠檬酸钠、维生素 C、β-胡萝卜素。请回答下列问题:
(1)本果粒橙饮料中,柠檬酸属于(
)
A、甜味剂
B、酸味剂
C、抗氧化剂
D、增稠剂
(2)本果粒橙饮料中,能为人体提供能量的物质是(
)
A、维生素 C
B、水
C、白砂糖
D、β-胡萝卜素
(3)某同学测定果汁中维生素 C 含量的多少,
实验如图所示。要得出正确的结论,实验过程中不需要进行控制的条件(
)
A、烧杯中溶液的体积
B.两个胶头滴管滴出的每滴果汁的体积
C、烧杯中淀粉-碘溶液的浓度
D、胶头滴管滴出的果汁的滴数
(4)盛装该果汁的塑料瓶底部有如图所示标志 。
它的含义是
。
�











 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc