2018年安徽省普通高中会考化学真题
1. 化学与生产、生活密切相关。下列说法不.正.确.的是
A. 自来水中可通入少量的氯气进行杀菌消毒
B.高纯度的硅单质可用于制作光导纤维
C. 过氧化钠可作为潜水艇里氧气的来源
D. 醋酸可除去暖水瓶中的水垢[主要成分是 CaCO3、Mg(OH)2]
2. 我国稀土资源丰富。150Sm 为稀土元素钐的一种核素,下列说法正确的是
62
A.质量数为 212
B.中子数为 150
C.核外电子数为 88
D.原子序数为 62
3. 实验是学习化学的重要途径。下列有关实验操作或仪器选择正确的是
A.收集二氧化碳
B.分离水和乙醇
C.转移液体
D.保存氢氧化钠溶液
4. 下列离子或分子在溶液中能大量共存的是
+
+
、CO2-
3
B.Mg2+
、SO2-
4
、K
A.H
-
、OH
+
C.Na
、NO
-
3
、Cl
-
D.Al3+
、Cl
-
、NH3·H2O
5. 下列化合物中只含有共价键的是
A.NaCl
B.CO2
C.KOH
D.Na2CO3
6. 下列与物质的量相关的说法正确的是
A.CH4 的摩尔质量为 16 g
B.常温常压下 1 mol CO2 的体积约为 22.4 L
C.16 g O2 含有的氧原子数约为 6.02×1023
D.1 mol·L-1H2SO4 溶液中 c(H
+
)为 1 mol·L-1
�
7.
FeCl3 溶液可作为印刷电路板的腐蚀液,发生的化学反应为:2FeCl3+Cu=2FeCl2+CuCl2。下列有关叙述正确
的是
A.该反应属于置换反应
B.该反应属于复分解反应
C.反应中 FeCl3 做氧化剂
D.反应中 Cu 得到电子
8. 右图是铜锌原电池的示意图。下列说法不.正.确.的是
A. Cu 片为正极
B.Zn 片上发生还原反应
C. 反应一段时间后溶液的 pH 值增大
D. 该装置将化学能转化为电能
9. 一定条件下,可逆反应 H2(g)+I2(g)=2HI(g)达到化学平衡状态。下列说法正确的是
A.该反应达到最大限度
B.各物质的浓度一定相等
C.正逆反应速率均为零
D.反应物全部转化为生成物
�
10.下列实验设计能达到实验目的的是
选项
实验目的
实验设计
A
B
C
D
检验 CO2-
3
检验 SO2-
4
检验 Cl
-
检验 Fe3+
取试样滴加稀盐酸,观察是否产生无色气体
取试样滴加 BaCl2 溶液,观察是否产生白色沉淀
取试样滴加 AgNO3 溶液,观察是否产生白色沉淀
取试样滴加 KSCN 溶液,观察溶液是否显红色
注意:11~15 小题有两组,你可以选做《化学与生活》模块或《有机化学基础》模块的任一组。
《化学与生活》模块
11.2018 年 6 月 5 日是世界环境日,我国的主题是“美丽中国,我是行动者”。下列做法符合这一主题的是
A.就地焚烧秸秆
B.少用一次性塑料袋
C.随意倾倒生活垃圾
D.任意排放工业废水
12. 微量元素对维持人体生命活动有重要的作用。下列措施与补充微量元素无.关.的是
A.食品中加糖
B.酱油中加铁
C.奶粉中加锌
D.食盐中加碘
13. 下列关于药物的说法正确的是
A.天然药物只来自于植物
B.使用青霉素前不必进行皮肤敏感试验
C.非处方药无毒副作用
D.阿司匹林具有解热镇痛作用
14. 下列物质属于天然高分子化合物的是
A.氨基酸
B.葡萄糖
C.淀粉
D.植物油
15. 下列材料不属于硅酸盐产品的是
A.玻璃
B.水泥
C.陶瓷
D.塑料
11.下列能鉴别甲烷和乙烯的试剂是
《有机化学基础》模块
�
A.氢氧化钾溶液
B.酸性高锰酸钾溶液
C.酒精
D.稀醋酸
12.下列物质不能发生水解反应的是
A.葡萄糖
B.卤代烃
C.油脂
D.蛋白质
13.下列各组物质互为同分异构体的是
A.CH3CH=CH2 和 CH3C≡CH
B.CH3CHBrCH2Br 和 CH2BrCHBrCH3
C.CH3CH2CHO 和 CH3OCH2CH3
14.加热条件下,下列物质能与新制的氢氧化铜悬浊液反应的是
A.CH3CH3
B.CH2=CH2
C.CH3CHO
15. 咖啡酸存在于野胡萝卜、荞麦等物质中,具有良好的止血作用,其结构简式如下图所示。下列关于咖啡酸的
说法正确的是
A. 分子式为 C9H10O
�
B.分子中含有两种官能团
C.1 mol 咖啡酸最多只能与 1 mol Br2 反应
D.分子中所有的碳原子可能在同一个平面上
16. (5 分)下表为元素周期表的一部分,请回答下列问题:
族
周期
ⅠA
一
二
三
○4
ⅡA
ⅢA
ⅥA
○1
ⅤA
○2
ⅣA
○3
0
ⅦA
○5
(1) 元素②的原子结构示意图是
。
(2) ④和⑤两种元素原子半径较小的是
(填元素符号),①和②两种元素最高价氧化物
对应的水化物酸性较强的是
(填化学式)。
(3) 元素④的单质在元素③的单质中燃烧的化学方程式为
。
17.(5 分)乙烯是一种基本化工原料,能发生如下转化(反应条件已略去)。请回答:
氯乙烷
HCl
乙烯(CH2=CH2)
H2O
O2
O2
←———
①
———→
乙醇
——→
乙醛(CH3CHO)
乙酸
——→
②
�
(1) 乙醇的结构简式为
。
(2) 乙酸分子中的官能团是
;反应②的反应类型是
。
(3) 写出一定条件下,反应①的化学方程式
。
18.(5 分)某化学兴趣小组探究铝与稀盐酸反应速率的影响因素,用等质量的铝和等体积、等浓度的足量稀盐
酸反应,得到的 3 组实验数据如下:
实验编号
铝的形态
反应温度/℃
收集 100 mL H2 所需时间/s
①
②
③
铝粉
铝片
铝片
20
20
30
回答下列问题:
21
82
35
(1) 写出铝与稀盐酸反应的化学方程式
。
(2) 探究温度对该反应速率影响的对比实验是③和(填实验编, 得出的
实验结论是
。
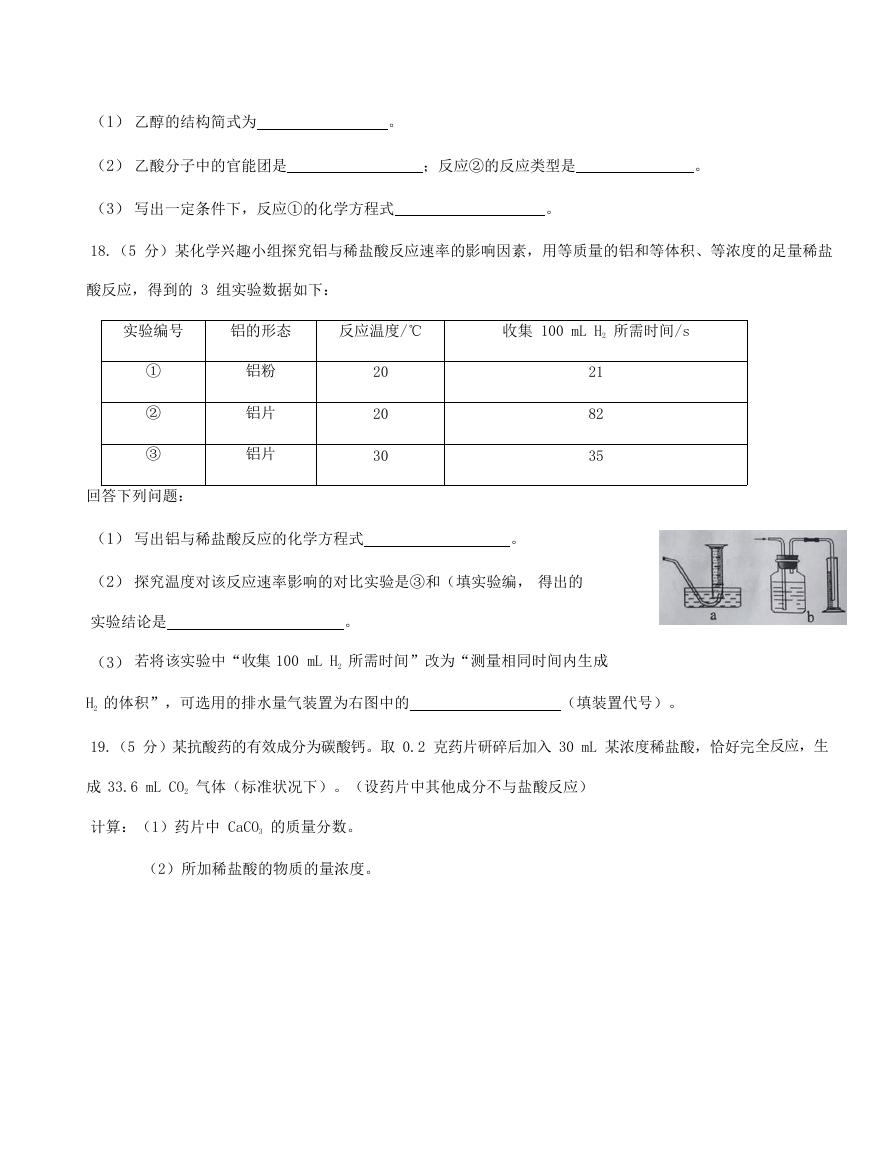
(3) 若将该实验中“收集 100 mL H2 所需时间”改为“测量相同时间内生成
H2 的体积”,可选用的排水量气装置为右图中的
(填装置代号)。
19.(5 分)某抗酸药的有效成分为碳酸钙。取 0.2 克药片研碎后加入 30 mL 某浓度稀盐酸,恰好完全反应,生
成 33.6 mL CO2 气体(标准状况下)。(设药片中其他成分不与盐酸反应)
计算:(1)药片中 CaCO3 的质量分数。
(2)所加稀盐酸的物质的量浓度。
�











 2023年江西萍乡中考道德与法治真题及答案.doc
2023年江西萍乡中考道德与法治真题及答案.doc 2012年重庆南川中考生物真题及答案.doc
2012年重庆南川中考生物真题及答案.doc 2013年江西师范大学地理学综合及文艺理论基础考研真题.doc
2013年江西师范大学地理学综合及文艺理论基础考研真题.doc 2020年四川甘孜小升初语文真题及答案I卷.doc
2020年四川甘孜小升初语文真题及答案I卷.doc 2020年注册岩土工程师专业基础考试真题及答案.doc
2020年注册岩土工程师专业基础考试真题及答案.doc 2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc
2023-2024学年福建省厦门市九年级上学期数学月考试题及答案.doc 2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc
2021-2022学年辽宁省沈阳市大东区九年级上学期语文期末试题及答案.doc 2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc
2022-2023学年北京东城区初三第一学期物理期末试卷及答案.doc 2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc
2018上半年江西教师资格初中地理学科知识与教学能力真题及答案.doc 2012年河北国家公务员申论考试真题及答案-省级.doc
2012年河北国家公务员申论考试真题及答案-省级.doc 2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc
2020-2021学年江苏省扬州市江都区邵樊片九年级上学期数学第一次质量检测试题及答案.doc 2022下半年黑龙江教师资格证中学综合素质真题及答案.doc
2022下半年黑龙江教师资格证中学综合素质真题及答案.doc